超分子笼PPC-2封装钌(Ru)纳米颗粒形成一种高效催化剂。PPC-2是由A、B、C三个组件拼装而成的正八面体超分子笼,结构示意如图。
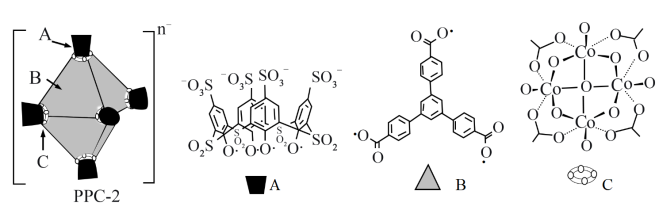
注:C组件中浅色原子由其他邻近组件提供。
(1)基态Co原子的价电子排布式为_______ 。
(2)组件A中所含四种元素的电负性由小到大的顺序为_______ 。
(3)组件B中碳原子的杂化类型为_______ 。
(4)组件C中Co原子位于相邻O原子构成的_______ 空隙中(填“四面体”或“八面体”)。
(5)每个组件C带一个单位负电荷,综合各组件所带电荷,计算PPC-2中n=_______ 。
(6)钌纳米颗粒进入PPC-2超分子笼后,钌晶体从六方堆积转化为面心立方堆积(晶胞参数为a pm)。超分子笼内钌晶体密度为_______ g·cm-3(用含a、NA的代数式表示)。

注:C组件中浅色原子由其他邻近组件提供。
(1)基态Co原子的价电子排布式为
(2)组件A中所含四种元素的电负性由小到大的顺序为
(3)组件B中碳原子的杂化类型为
(4)组件C中Co原子位于相邻O原子构成的
(5)每个组件C带一个单位负电荷,综合各组件所带电荷,计算PPC-2中n=
(6)钌纳米颗粒进入PPC-2超分子笼后,钌晶体从六方堆积转化为面心立方堆积(晶胞参数为a pm)。超分子笼内钌晶体密度为
更新时间:2022-03-04 20:13:43
|
相似题推荐
解答题-结构与性质
|
较易
(0.85)
解题方法
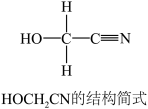
【推荐1】[Zn(CN)4]2-在水溶液中与HCHO发生如下反应:4HCHO+[Zn(CN)4]2-+4H++4H2O=[Zn(H2O)4]2++4HOCH2CN
(1)Zn2+基态核外电子排布式为__________________________ 。
(2)1mol HCHO分子中含有σ键的数目为__________ mol 。
(3)HOCH2CN分子中碳原子轨道的杂化类型是________________ 。
(4)与阴离子NH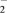 互为等电子体的分子为
互为等电子体的分子为__________________ 。
(5)尿素晶体的晶胞结构如图所示,该晶胞中有___________ 个尿素分子。


(1)Zn2+基态核外电子排布式为
(2)1mol HCHO分子中含有σ键的数目为
(3)HOCH2CN分子中碳原子轨道的杂化类型是
(4)与阴离子NH
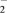 互为等电子体的分子为
互为等电子体的分子为(5)尿素晶体的晶胞结构如图所示,该晶胞中有

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】化合物YX2、ZX2中,X、Y、Z都是短周期元素,X与Y为同周期元素,Y与Z为同族元素,Y原子的最外层p能级电子数等于前一电子层电子总数。X原子最外层p能级中只有一个轨道填充了2个电子,则X的电子排布式为___________ ;Y的简化电子排布式为___________ ;Z的电子排布式为____________ ;YX2的化学式是________ ,电子式是________ ;ZX2的化学式是________ 。
您最近一年使用:0次
【推荐3】如表是部分短周期元素的性质或原子结构特点。
请回答下列问题:
(1)基态T原子的价电子排布式为_______
(2)比较Y元素,W元素的离子半径_______ (用离子符号表示)
(3)元素Z在元素周期表中的位置是_______ ,元素Z与元素T相比,非金属性较强的是_______ (用元素符号表示)。下列表述中能证明这一事实的是_______ (填序号)。
a.常温下Z的单质和T的单质状态不同
b.Z元素的简单气态氢化物比T元素的稳定
c.Z的最高价氧化物对应水化物的酸性比T的强
(4)T、X、Y、Z四种元素的最高价氧化物对应水化物中性质明显不同于其他三种的是_______ (填化学式)
(5)W的最高价氧化物对应水化物与NaOH溶液反应的离子方程式为_______ 。
| 元素编号 | 元素性质或原子结构 |
| T | M层上有6个电子 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 元素最高正价是+7价 |
| W | 其最高价氧化物对应水化物既能跟酸反应,又能跟强碱反应 |
(1)基态T原子的价电子排布式为
(2)比较Y元素,W元素的离子半径
(3)元素Z在元素周期表中的位置是
a.常温下Z的单质和T的单质状态不同
b.Z元素的简单气态氢化物比T元素的稳定
c.Z的最高价氧化物对应水化物的酸性比T的强
(4)T、X、Y、Z四种元素的最高价氧化物对应水化物中性质明显不同于其他三种的是
(5)W的最高价氧化物对应水化物与NaOH溶液反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
【推荐1】铬酸铅(PbCrO4)是黄色涂料“铬黄”的主要成分,实验室由某合金废料(主要成分为Fe、C、Cr2O3)制备PbCrO4的流程如图:
回答下列问题:
(1)基态82Pb2+的价层电子排布图为_______ 。
(2)“酸浸”时,加热可以加快反应速率,但温度不宜过高的原因是_______ (用化学方程式解释)。
(3)“滤渣2”中电负性最大的元素是_______ (填元素符号)。
(4)“氧化”时发生反应的离子方程式为_______ 。
(5)“调节pH=6”的目的是_______ 。
(6)二卤化铅(PbX2)是一类重要的含铅化合物,其熔点如下表所示:
①结合PbX2的熔点变化规律,可推断:依F、Cl、Br、I次序,PbX2中的化学键的离子性_______ (填“增强”“不变”或“减弱”,后同)、共价性_______ 。
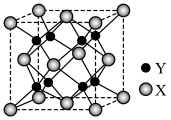
②PbF2的立方晶胞如图所示,其中X代表的离子是_______ (填离子符号);若该晶胞参数为anm,则正、负离子的最小核间距为_______ pm。
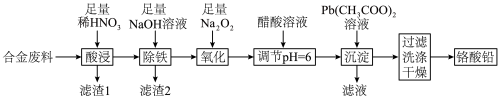
回答下列问题:
(1)基态82Pb2+的价层电子排布图为
(2)“酸浸”时,加热可以加快反应速率,但温度不宜过高的原因是
(3)“滤渣2”中电负性最大的元素是
(4)“氧化”时发生反应的离子方程式为
(5)“调节pH=6”的目的是
(6)二卤化铅(PbX2)是一类重要的含铅化合物,其熔点如下表所示:
| 二卤化铅 | PbF2 | PbCl2 | PbBr2 | PbI2 |
| 熔点/℃ | 824 | 501 | 373 | 402 |
②PbF2的立方晶胞如图所示,其中X代表的离子是
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
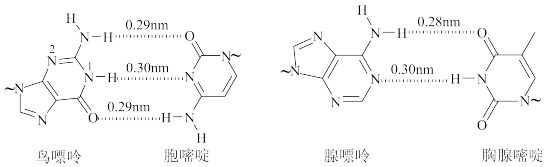
【推荐2】氢键对生命活动具有重要意义。DNA中四种碱基间的配对方式如下图。(~ 代表糖苷键)
(1)基态N的核外电子排布式为___________ ;N和O第一电离能较大的是___________ 。
(2)①碱基中的-NH2具有一定的碱性,可以结合H+形成-NH ,从结构角度解释可以结合的原因:
,从结构角度解释可以结合的原因:___________ 。
②写出甘氨酸(H2NCH2COOH)在pH=1和pH=13时的粒子存在形态:pH=1时___________ ,pH=13时___________ 。
(3)鸟嘌呤是一种常见的碱基。
①鸟嘌呤中2号N的杂化类型为___________ 。
②鸟嘌呤中N-H键的平均键长___________ (填“大于”“小于”或“等于”)0.29nm。
(4)氢键在DNA复制过程中起重要作用。
①碱基中,O、N能与H形成氢键而C不能,原因是___________ 。
②下列说法正确的是___________ (填序号)。
a.氢键的强度较小,在DNA解旋和复制时容易断裂和形成
b.鸟嘌呤与胞嘧啶之间的相互作用比鸟嘌呤与胸腺嘧啶之间的更强
c.碱基配对时,一个H可以同时与多个原子形成氢键
d.DNA在形成双螺旋结构时,碱基遵循互补配对原则,形成的氢键多,结构更稳定
(5)一定条件下鸟嘌呤会发生异构化,其1号N上的H会转移到O上形成-OH。
①鸟嘌呤异构化后的结构简式为___________ 。
②鸟嘌呤异构化后最有可能配对的嘧啶碱基是___________ 。
(1)基态N的核外电子排布式为
(2)①碱基中的-NH2具有一定的碱性,可以结合H+形成-NH
 ,从结构角度解释可以结合的原因:
,从结构角度解释可以结合的原因:②写出甘氨酸(H2NCH2COOH)在pH=1和pH=13时的粒子存在形态:pH=1时
(3)鸟嘌呤是一种常见的碱基。
①鸟嘌呤中2号N的杂化类型为
②鸟嘌呤中N-H键的平均键长
(4)氢键在DNA复制过程中起重要作用。
①碱基中,O、N能与H形成氢键而C不能,原因是
②下列说法正确的是
a.氢键的强度较小,在DNA解旋和复制时容易断裂和形成
b.鸟嘌呤与胞嘧啶之间的相互作用比鸟嘌呤与胸腺嘧啶之间的更强
c.碱基配对时,一个H可以同时与多个原子形成氢键
d.DNA在形成双螺旋结构时,碱基遵循互补配对原则,形成的氢键多,结构更稳定
(5)一定条件下鸟嘌呤会发生异构化,其1号N上的H会转移到O上形成-OH。
①鸟嘌呤异构化后的结构简式为
②鸟嘌呤异构化后最有可能配对的嘧啶碱基是
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
【推荐3】下表为元素周期表前三周期的一部分:
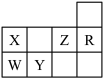
(1)Y的基态原子的电子排布式为___________ 。
(2)X的氢化物的沸点与W的氢化物的沸点比较:________ >_______ (填化学式),原因是________ 。
(3)选出X的基态原子的电子排布图___________ ,另一电子排布图不能作为基态原子的电子排布图是因为它不符合___________ (填序号)。

A.能量最低原理 B.泡利原理 C.洪特规则
(4)以上五种元素中,___________ (填元素符号)元素第一电离能最大,___________ 元素的电负性最大。
(5)由以上某种元素与氢元素组成的三角锥形分子E和由以上某种元素组成的直线分子G反应,生成两种直线形分子L和M(组成E、G、L、M分子的元素原子序数均小于10),反应如下图所示,则下列判断错误的是___________ 。
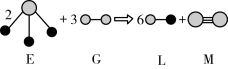
A.G是最活泼的非金属单质
B.L是极性分子
C.E的中心原子杂化轨道类型为sp2杂化
D.M的化学性质比同主族相邻元素单质的化学性质活泼
E.M分子中有1个σ键,2个π键

(1)Y的基态原子的电子排布式为
(2)X的氢化物的沸点与W的氢化物的沸点比较:
(3)选出X的基态原子的电子排布图

A.能量最低原理 B.泡利原理 C.洪特规则
(4)以上五种元素中,
(5)由以上某种元素与氢元素组成的三角锥形分子E和由以上某种元素组成的直线分子G反应,生成两种直线形分子L和M(组成E、G、L、M分子的元素原子序数均小于10),反应如下图所示,则下列判断错误的是

A.G是最活泼的非金属单质
B.L是极性分子
C.E的中心原子杂化轨道类型为sp2杂化
D.M的化学性质比同主族相邻元素单质的化学性质活泼
E.M分子中有1个σ键,2个π键
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐1】金属钛被誉为“二十一世纪金属”,有“生物金属,海洋金属,太空金属”的美称,具有广泛的应用前景。回答下列问题:
(1)钛原子核外电子有_____ 种空间运动状态;Ti2+电子占据的最高能层的电子排布式为______ 。
(2)磷酸钛铝锂可用作锂离子电池的正极材料,PO 的空间构型是
的空间构型是_____ ,第一电离能介于Al、P之间的第三周期元素为______ (填元素符号)。
(3)Ti(BH4)2是一种储氢材料,其中电负性最小的元素为______ ,B原子的杂化方式是_____ ,其中的 可由BH3和H-结合而成。
可由BH3和H-结合而成。 含有
含有______ 。(填序号)
①σ键 ②π键 ③氢键 ④配位键 ⑤离子键
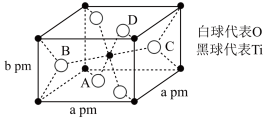
(4)TiO2在自然界中有三种同素异形态,即金红石型、锐钛型和斜钛型三种,其中金红石型是三种变体中最稳定的一种,其晶胞如图所示,该晶体的密度为_____ g•cm-3(设阿伏伽德罗常数的值为NA,用含a、b、NA的代数式表示)。
(1)钛原子核外电子有
(2)磷酸钛铝锂可用作锂离子电池的正极材料,PO
 的空间构型是
的空间构型是(3)Ti(BH4)2是一种储氢材料,其中电负性最小的元素为
 可由BH3和H-结合而成。
可由BH3和H-结合而成。 含有
含有①σ键 ②π键 ③氢键 ④配位键 ⑤离子键
(4)TiO2在自然界中有三种同素异形态,即金红石型、锐钛型和斜钛型三种,其中金红石型是三种变体中最稳定的一种,其晶胞如图所示,该晶体的密度为

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
【推荐2】当今社会,各国治理污染的压力都很大,如何变废为宝,合理利用资源,是摆在科学家面前的课题。科学家设计在催化剂表面利用 还原氮的氧化物的一种反应机理如图所示。
还原氮的氧化物的一种反应机理如图所示。
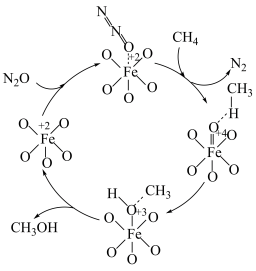
回答下列问题:
(1)基态Fe原子与基态 离子中未成对的电子数之比为
离子中未成对的电子数之比为__________ 。
(2)第二周期第一电离能比N大的主族元素为__________ (填化学式)。上述历程中涉及反应的非金属电负性由大到小的顺序为__________ (填化学式)。
(3)硝酸根离子的空间构型为__________ ,其中N的杂化轨道类型为__________ 。
(4) 中化学键类型有
中化学键类型有______ (填选项字母),甲醇易溶于水的原因是__________ 。
A.非极性共价键 B.氢键 C. 键 D.极性共价键
键 D.极性共价键
(5)铁的晶胞类型有多种,其中图甲中与一个铁原子等距离且最近的铁原子有_______ 个,图乙所示晶胞的密度为__________  (用含有a、
(用含有a、 的代数式表示)。
的代数式表示)。

 还原氮的氧化物的一种反应机理如图所示。
还原氮的氧化物的一种反应机理如图所示。
回答下列问题:
(1)基态Fe原子与基态
 离子中未成对的电子数之比为
离子中未成对的电子数之比为(2)第二周期第一电离能比N大的主族元素为
(3)硝酸根离子的空间构型为
(4)
 中化学键类型有
中化学键类型有A.非极性共价键 B.氢键 C.
 键 D.极性共价键
键 D.极性共价键(5)铁的晶胞类型有多种,其中图甲中与一个铁原子等距离且最近的铁原子有
 (用含有a、
(用含有a、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐3】A.[物质结构与性质]
Cu2O广泛应用于太阳能电池领域。以CuSO4、NaOH和抗坏血酸为原料,可制备Cu₂O。
(1)Cu2+基态核外电子排布式为____ 。
(2) 的空间构型为
的空间构型为____ (用文字描述);Cu2+与OH−反应能生成[Cu(OH)4]2−,[Cu(OH)4]2−中的配位原子为____ (填元素符号)。
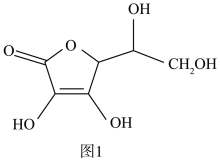
(3)抗坏血酸的分子结构如图1所示,分子中碳原子的轨道杂化类型为____ ;推测抗坏血酸在水中的溶解性:____ (填“难溶于水”或“易溶于水”)。
(4)一个Cu2O晶胞(见图2)中,Cu原子的数目为____ 。
Cu2O广泛应用于太阳能电池领域。以CuSO4、NaOH和抗坏血酸为原料,可制备Cu₂O。
(1)Cu2+基态核外电子排布式为
(2)
 的空间构型为
的空间构型为(3)抗坏血酸的分子结构如图1所示,分子中碳原子的轨道杂化类型为


(4)一个Cu2O晶胞(见图2)中,Cu原子的数目为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐1】Fe、Cu、Cr都是第四周期过渡元素,回答下列问题。
(1)FeCl3是一种常用的净水剂,则Cl元素的原子核外有___________ 种不同能级的电子,基态Fe3+的电子排布式为___________ 。
(2)实验室中可用KSCN或K4[Fe(CN)6]来检验Fe3+,其中K4[Fe(CN)6]与Fe3+反应可得到一种蓝色沉淀KFe[Fe(CN)6],该物质晶胞的 结构如图所示(K+未画出),则一个晶胞中的K+个数为
结构如图所示(K+未画出),则一个晶胞中的K+个数为___________ 。

(3)Cu2+能与乙二胺(H2N—CH2—CH2—NH2)形成配离子如图,则该配离子中含有的化学键类型有___________ (填字母)。

a.配位键 b.极性键 c.离子键 d.非极性键
一个乙二胺分子中共有___________ 个σ键,C原子的杂化方式为___________ 。
(4)铜的晶胞为面心立方最密堆积,边长为 pm。则铜原子直径约为
pm。则铜原子直径约为___________ pm。
(1)FeCl3是一种常用的净水剂,则Cl元素的原子核外有
(2)实验室中可用KSCN或K4[Fe(CN)6]来检验Fe3+,其中K4[Fe(CN)6]与Fe3+反应可得到一种蓝色沉淀KFe[Fe(CN)6],该物质晶胞的
 结构如图所示(K+未画出),则一个晶胞中的K+个数为
结构如图所示(K+未画出),则一个晶胞中的K+个数为
(3)Cu2+能与乙二胺(H2N—CH2—CH2—NH2)形成配离子如图,则该配离子中含有的化学键类型有

a.配位键 b.极性键 c.离子键 d.非极性键
一个乙二胺分子中共有
(4)铜的晶胞为面心立方最密堆积,边长为
 pm。则铜原子直径约为
pm。则铜原子直径约为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】三明清流“天芳悦潭”温泉富含珍稀“锗”元素。其中锗石含有人体所需的硒、锌、镍、钴、锰、镁、钙等30多种对人体有益的微量元素。回答下列问题:
(1)基态Ge原子价电子排布图为_______ 、属于_______ 区。
(2)锗与碳同族,性质和结构有一定的相似性,锗元素能形成无机化合物(如锗酸钠: ;二锗酸钠:
;二锗酸钠: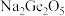 等),也能形成类似于烷烃的锗烷(
等),也能形成类似于烷烃的锗烷( )。
)。
① 中阴离子的空间结构是
中阴离子的空间结构是_______ 。
②推测1mol 中含有的σ键的数目是
中含有的σ键的数目是_______ (用 表示阿伏加德罗常数值)。
表示阿伏加德罗常数值)。
(3)利用离子液体[EMIM][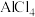 ]可电沉积还原金属Ge,其熔点只有7℃,其中
]可电沉积还原金属Ge,其熔点只有7℃,其中 结构如图所示。
结构如图所示。
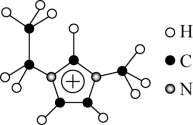
①该物质的晶体类型是_______ 。
② 离子中组成元素的电负性由小到大的顺序是
离子中组成元素的电负性由小到大的顺序是_______ 。
(4)独立的 分子中H−N−H的键角为107.3°,
分子中H−N−H的键角为107.3°, 离子中H−N−H的键角
离子中H−N−H的键角_______ 107.3°(填“大于”、“小于”或“等于”)。
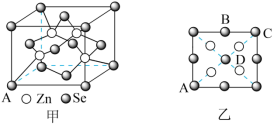
(5)硒化锌(ZnSe)是一种重要的半导体材料,其晶胞结构如图甲所示,已知晶胞边长为apm,该晶胞中两个Zn原子之间的间距是_______ ;乙图为甲图的俯视图,A点坐标为(0,0,0),B点坐标为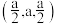 ,则D点坐标为
,则D点坐标为_______ ;若该晶胞密度为 ,则阿伏加德罗常数
,则阿伏加德罗常数 为
为_______ (只列出计算式)。
(1)基态Ge原子价电子排布图为
(2)锗与碳同族,性质和结构有一定的相似性,锗元素能形成无机化合物(如锗酸钠:
 ;二锗酸钠:
;二锗酸钠: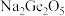 等),也能形成类似于烷烃的锗烷(
等),也能形成类似于烷烃的锗烷( )。
)。①
 中阴离子的空间结构是
中阴离子的空间结构是②推测1mol
 中含有的σ键的数目是
中含有的σ键的数目是 表示阿伏加德罗常数值)。
表示阿伏加德罗常数值)。(3)利用离子液体[EMIM][
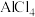 ]可电沉积还原金属Ge,其熔点只有7℃,其中
]可电沉积还原金属Ge,其熔点只有7℃,其中 结构如图所示。
结构如图所示。
①该物质的晶体类型是
②
 离子中组成元素的电负性由小到大的顺序是
离子中组成元素的电负性由小到大的顺序是(4)独立的
 分子中H−N−H的键角为107.3°,
分子中H−N−H的键角为107.3°, 离子中H−N−H的键角
离子中H−N−H的键角(5)硒化锌(ZnSe)是一种重要的半导体材料,其晶胞结构如图甲所示,已知晶胞边长为apm,该晶胞中两个Zn原子之间的间距是
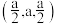 ,则D点坐标为
,则D点坐标为 ,则阿伏加德罗常数
,则阿伏加德罗常数 为
为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】氮及其化合物,在工农业生产中作用巨大。
(1)下列有关氮的化合物的说法,正确的是___________。
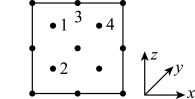
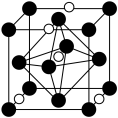
(2)氮和碳组成的一种新型材料,硬度超过金刚石,其部分结构如下图所示。它的化学式为___________ ,它的硬度超过金刚石的主要原因是___________ 。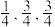 ),则原子2和4的原子分数坐标为
),则原子2和4的原子分数坐标为___________ 、___________ 。___________ ,氮化钼晶胞边长为a pm,晶体的密度ρ=___________ g·cm-3(列出计算式,设NA为阿伏加德罗常数的值)。
(1)下列有关氮的化合物的说法,正确的是___________。
| A.肼(N2H4)的沸点低于乙烷(C2H6) |
| B.NH3极易溶于水,原因之一是NH3能够与水分子形成分子间氢键 |
| C.NF3和NH3空间构型均为三角锥形,分子中键角:NH3>NF3 |
D.尿素(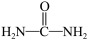 )中σ键与π键的比例为7:1 )中σ键与π键的比例为7:1 |
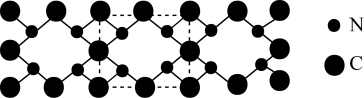
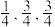 ),则原子2和4的原子分数坐标为
),则原子2和4的原子分数坐标为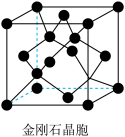
您最近一年使用:0次



