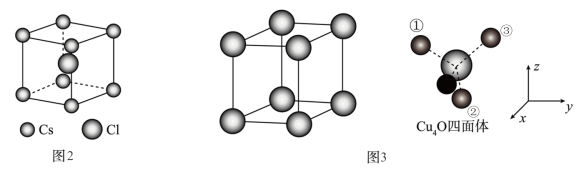
| I1 | I2 | I3 | I4 | |
| 电离能(kJ·mol-1) | 578 | 1817 | 2745 | 11578 |
(2)NH4Al(SO4)2中,电负性最大的元素是
Ⅱ.如图所示为高温超导领域里的一种化合物-钙钛矿晶体结构,该结构是具有代表性的最小重复单位。
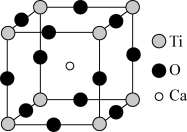
(3)在该物质的晶体结构中,每个钛离子周围与它最接近且距离相等的氧离子、钙离子各有
(4)该晶体结构中,氧、钛、钙的离子个数比是
(5)若钙、钛、氧三种元素的相对质量分别为a、b、c,晶体结构图中正方体边长(钛离子之间的距离)为d nm(1 nm=10-9 m),则该晶体的密度为
相似题推荐
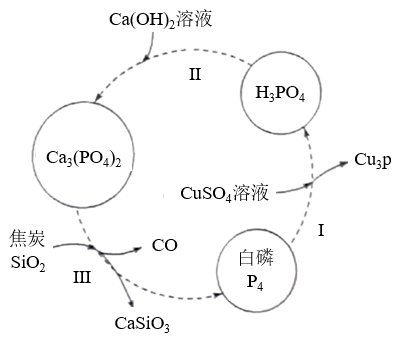
(1)过程III的化学方程式为
(2)基态Cu原子价层电子排布式为
(3)元素铜与镍的第二电离能分别为ICu=1958kJ·mol-1、INi=1753kJ·mol-1,ICu>INi的原因是
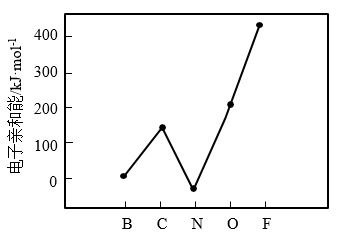
(4)元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(E1)。第二周期部分元素的E1变化趋势如图所示,氮元素的E1呈现异常的原因是
 )是一种常见的食盐抗结剂,其三水合物(
)是一种常见的食盐抗结剂,其三水合物( )是黄色晶体,俗称黄血盐,遇
)是黄色晶体,俗称黄血盐,遇 立即产生深蓝色沉淀(
立即产生深蓝色沉淀( )。回答下列问题。
)。回答下列问题。(1)O元素位于
(2)Fe在元素周期表中的位置
(3)黄血盐(
 )中四种非金属元素的第一电离能最大的是
)中四种非金属元素的第一电离能最大的是(4)亚铁氰化钾(
 )中四种元素的电负性由大到小的顺序为
)中四种元素的电负性由大到小的顺序为(5)普鲁士蓝(
 )中C的杂化方式为
)中C的杂化方式为【推荐3】Ⅰ.蒙脱石散对消化道内的病毒、病菌及其产生的毒素、气体等有极强的固定、抑制作用,常用于成人及儿童急性、慢性腹泻。蒙脱石散的有效成分可表示为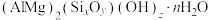 。
。
(1)基态
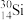 原子的核外电子排布式为
原子的核外电子排布式为(2)O、Mg、Al、Si四种元素的第一电离能从大到小的顺序为
(3)
 是无色透明液体,可以与N-甲基咪唑
是无色透明液体,可以与N-甲基咪唑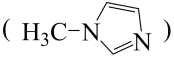 等物质反应。
等物质反应。①将用毛皮摩擦过的橡胶棒靠近 液流,液体流
液流,液体流
②一个N-甲基咪唑分子中含有
(4)硅酸盐与二氧化硅一样,都是以硅氧四面体作为基本结构单元。硅氧四面体可以表示成
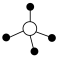 :其中●表示氧原子,中心◯表示硅原子,其俯视图为
:其中●表示氧原子,中心◯表示硅原子,其俯视图为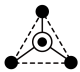 。
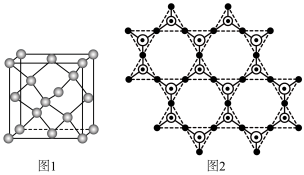
。① 晶胞可理解成将金刚石晶胞(如图1所示)中的C原子置换成Si原子,然后在
晶胞可理解成将金刚石晶胞(如图1所示)中的C原子置换成Si原子,然后在 之间插入O原子而形成。
之间插入O原子而形成。
推测 晶胞中含有
晶胞中含有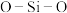 的键角为
的键角为
②蒙脱石散中的“(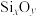 )”是一种大片层状的多硅酸根,其可能结构如图2所示,则
)”是一种大片层状的多硅酸根,其可能结构如图2所示,则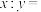
Ⅱ.以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标。四方晶系的晶胞结构如图所示,晶胞棱边夹角均为90°,晶胞中部分原子的分数坐标如下表所示。
坐标原子 | x | y | z |
Cd | 0 | 0 | 0 |
Sn | 0 | 0 | 0.5 |
As | 0.25 | 0.25 | 0.125 |
(5)一个晶胞中有
 最近的Sn
最近的Sn 晶体中与Sn距离最近的As有
晶体中与Sn距离最近的As有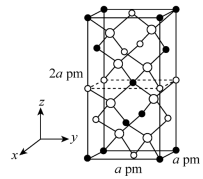
【推荐1】科学家合成一种新化合物(如图所示)。其中W、X、Y、Z为短周期元素,且位于同一周期,W是所在周期中第一电离能最小的元素,Y元素基态原子的未成对电子数等于其电子层数,Z元素的原子核外最外层电子数是X元素原子核外电子数的一半。回答下列问题:
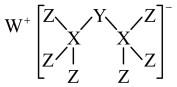
(1)W、X、Y、Z原子半径由大到小的顺序为
(2)Z的核外电子排布式为
(3)基态X原子价电子轨道表示式为
(4)W元素基态原子核外电子有
(5)X的电负性
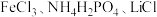 和苯胺等作为原料制备。回答下列问题:
和苯胺等作为原料制备。回答下列问题:(1)在周期表中,与Li的化学性质最相似的邻族元素是
(2)
 中的化学键具有明显的共价性,蒸汽状态下以双聚分子存在的
中的化学键具有明显的共价性,蒸汽状态下以双聚分子存在的 的结构式为
的结构式为(3)苯胺(
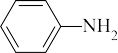 )的晶体类型是
)的晶体类型是(4)
 中,电负性最高的元素是
中,电负性最高的元素是(5)
 和
和 属于简单磷酸盐,而直链的多磷酸盐则是一种复杂磷酸盐,如:焦磷酸钠、三磷酸钠等。焦磷酸根离子、三磷酸根离子如图所示:
属于简单磷酸盐,而直链的多磷酸盐则是一种复杂磷酸盐,如:焦磷酸钠、三磷酸钠等。焦磷酸根离子、三磷酸根离子如图所示:
这类磷酸根离子的化学式可用通式表示为
 ;C元素为最活泼的非金属元素;D元素核外有三个电子层,最外层电子数是核外电子总数的
;C元素为最活泼的非金属元素;D元素核外有三个电子层,最外层电子数是核外电子总数的 ;E元素基态原子核外有7个能级且有4个未成对电子;F元素在元素周期表第11列;G元素与A元素位于同一主族,其某种氧化物有剧毒。
;E元素基态原子核外有7个能级且有4个未成对电子;F元素在元素周期表第11列;G元素与A元素位于同一主族,其某种氧化物有剧毒。(1)D、C两种元素形成的化合物的电子式为
(2)A、B、C三种元素的电负性由小到大的顺序为
(3)C元素的电子排布图为
(4)E元素位于元素周期表的第
(5)F元素位于元素周期表的
(6)G可能的性质有___________(填字母)。
| A.其最高价氧化物对应水化物是弱酸 | B.其第一电离能小于磷小于硒 |
| C.其原子半径大于锗 | D.氢化物的稳定性G大于A |

(1)酞菁和酞菁铜的结构如图:
①酞菁如图一中N原子的杂化方式为
②酞菁铜如图二中元素的电负性由大到小的顺序为
③用箭头标记出酞菁铜中铜原子周围的配位键:
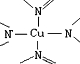 。
。(2)图三所示的物质结构中的B和O原子第一电离能较小是
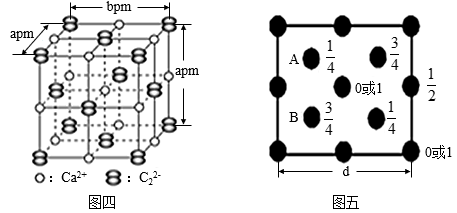
(3)如图四CaC2晶体中C
 与O
与O 互为等电子体,O
互为等电子体,O 的电子式可表示为
的电子式可表示为 中含有的π键数目为
中含有的π键数目为 的存在,使晶胞沿一个方向拉长。CaC2晶体中1个Ca2+周围距离最近的C
的存在,使晶胞沿一个方向拉长。CaC2晶体中1个Ca2+周围距离最近的C 数目为
数目为(4)SiO2的硬度较大的主要原因是
(1)基态铁原子的电子排布式为
(2)我国菱铁矿FeCO3储量较为丰富。其中CO
 的空间结构为
的空间结构为(3)草酸亚铁可作为电池正极材料磷酸铁锂的原料,其结构简式如下,碳原子的杂化方式是
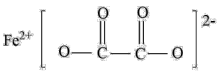
(4)Fe(CO)5溶于汽油、苯、丙酮等有机溶剂,熔点、沸点分别在-20 ℃、103.6℃左右。因此可知Fe(CO)5属于
(5)铁与氨气反应生成一种如图所示晶胞结构的产物,N周围最近的Fe数目是
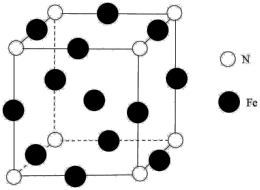
(1)基态F原子核外电子的运动状态有
(2)O、F、
 电负性由大到小的顺序为
电负性由大到小的顺序为 分子的空间结构为
分子的空间结构为 的熔、沸点
的熔、沸点 ,原因是
,原因是(3)
 是第五周期的稀有气体元素,与F形成的
是第五周期的稀有气体元素,与F形成的 室温下易升华。
室温下易升华。 中心原子的价层电子对数为
中心原子的价层电子对数为 中心原子杂化方式推断合理的是
中心原子杂化方式推断合理的是A.
 B.
B. C.
C. D.
D.
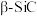 的晶胞结构如图所示,若碳和硅的原子半径分别为apm和bpm,密度为
的晶胞结构如图所示,若碳和硅的原子半径分别为apm和bpm,密度为 ,其原子的空间利用率(即晶胞中原子体积占空间体积的百分率)为
,其原子的空间利用率(即晶胞中原子体积占空间体积的百分率)为 ,
, 的代数式表示,
的代数式表示, 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。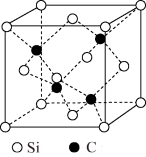

(1)在该晶胞中,Zn的配位数为
(2)原子坐标参数可表示晶胞内部各原子的相对位置。如图晶胞中,原子坐标参数a为(0,0,0);b为(
 ,0,
,0, );c为(
);c为( ,
, ,0)。则d的坐标参数为
,0)。则d的坐标参数为(3)已知该晶胞的密度为ρg·cm-3,则其中两个S原子之间的距离为
(1)
 的立体构型是
的立体构型是(2)第四周期元素中,与基态As原子核外未成对电子数目相同的元素符号为
(3)抗坏血酸(
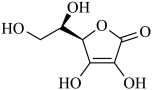 )常被用作碳包覆的碳源,以增强电极导电性,其易溶于水的原因是
)常被用作碳包覆的碳源,以增强电极导电性,其易溶于水的原因是(4)电池工作时,Li⁺沿聚乙二醇分子中的碳氧链迁移的过程如图甲所示(图中阴离子未画出),电解质LiPF6或LiAsF6的阴离子结构如图乙所示(X=P、As)。
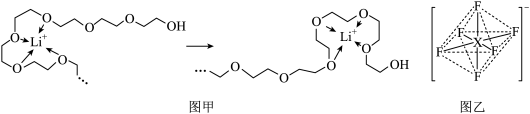
①从化学键角度看,Li⁺迁移过程发生
②已知相同条件下,锂离子的迁移速率与离子键的强弱有关,则Li⁺在
③图乙中X的杂化方式最可能是
a.sp3 b.sp3d c.sp3d2 d.sp3d3
(5)Cu2O晶体结构与CsCl(图2)相似,只是利用Cu4O占据CsCl晶体中Cl的位置,而Cs位置由O原子占据,如图3所示,每个Cu2O晶胞中有
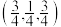 ,②处Cu原子坐标为
,②处Cu原子坐标为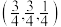 ,则③处Cu原子坐标为(___________,
,则③处Cu原子坐标为(___________,