明代科学家宋应星在《天工开物》中写道:“凡玉入中国,贵者尽出于田葱岭”。和田玉的主要化学成分是含水的钙镁硅酸盐。回答下列问题:
(1)元素镁能形成很多简单微粒,下面是镁原子形成的微粒的电子排布式,其中再电离出一个电子所需能量最大的是______ (填标号),当从C状态变到B状态,形成的是______ 光谱(选填“发射”或“吸收”)。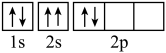 ,该电子排布图违背了
,该电子排布图违背了______ 。
(3)元素钙、镁和氯三种元素形成的最高价氧化物的水化物中,碱性最强的是______ (填化学式,下同),酸性最强的是______ 。
(4) 中中心原子Si的杂化类型是
中中心原子Si的杂化类型是______ ,离子空间结构为______ 。
(5)在 中不存在的化学键类型有
中不存在的化学键类型有______ 。
A.非极性共价键 B.极性共价键 C. 键 D.
键 D. 键
键
碳酸( )的酸性比硅酸(
)的酸性比硅酸( )
)______ (填“强”或“弱”),用离子方程式证明______ 。
(6)羧基( )能电离出
)能电离出 ,使溶液呈现酸性,已知
,使溶液呈现酸性,已知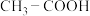 的酸性小于
的酸性小于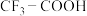 ,则推电子能力较强的是
,则推电子能力较强的是______ (填“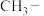 ”或“
”或“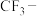 ”)
”)
(1)元素镁能形成很多简单微粒,下面是镁原子形成的微粒的电子排布式,其中再电离出一个电子所需能量最大的是
A. 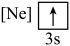 B.
B.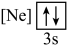 C.
C. 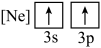 D.
D.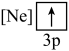
 ,该电子排布图违背了
,该电子排布图违背了(3)元素钙、镁和氯三种元素形成的最高价氧化物的水化物中,碱性最强的是
(4)
 中中心原子Si的杂化类型是
中中心原子Si的杂化类型是(5)在
 中不存在的化学键类型有
中不存在的化学键类型有A.非极性共价键 B.极性共价键 C.
 键 D.
键 D. 键
键碳酸(
 )的酸性比硅酸(
)的酸性比硅酸( )
)(6)羧基(
 )能电离出
)能电离出 ,使溶液呈现酸性,已知
,使溶液呈现酸性,已知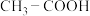 的酸性小于
的酸性小于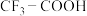 ,则推电子能力较强的是
,则推电子能力较强的是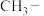 ”或“
”或“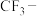 ”)
”)
更新时间:2024/03/28 19:57:06
|
相似题推荐
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐1】不锈钢是由铁、铬、碳及众多不同元素所组成的合金。目前铬被广泛应用于冶金、化工、铸铁、耐火等领域。
(1)Cr基态原子价层电子的轨道表示式为______ 。其核外有______ 种能量状态的电子。
(2)金属铬的第二电离能(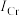 )和锰的第二电离能(
)和锰的第二电离能(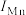 )分别为11590.6 kJ⋅mol
)分别为11590.6 kJ⋅mol 、1509.0 kJ⋅mol
、1509.0 kJ⋅mol ,
,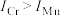 的原因是
的原因是____________ 。
(3)过氧化铬( )中Cr的化合价为
)中Cr的化合价为 ,则分子中σ键、π键的数目之比为
,则分子中σ键、π键的数目之比为______ 。
(4) 的熔点(83℃)比
的熔点(83℃)比 的熔点(1100℃)低得多,这是因为
的熔点(1100℃)低得多,这是因为____________ 。
(5)Cr的一种配合物结构如图所示,该配合物中碳原子的杂化方式是______ ,阳离子中Cr的配位数为______ ,阴离子 的空间构型为
的空间构型为______ 。
(1)Cr基态原子价层电子的轨道表示式为
(2)金属铬的第二电离能(
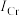 )和锰的第二电离能(
)和锰的第二电离能(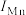 )分别为11590.6 kJ⋅mol
)分别为11590.6 kJ⋅mol 、1509.0 kJ⋅mol
、1509.0 kJ⋅mol ,
,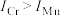 的原因是
的原因是(3)过氧化铬(
 )中Cr的化合价为
)中Cr的化合价为 ,则分子中σ键、π键的数目之比为
,则分子中σ键、π键的数目之比为(4)
 的熔点(83℃)比
的熔点(83℃)比 的熔点(1100℃)低得多,这是因为
的熔点(1100℃)低得多,这是因为(5)Cr的一种配合物结构如图所示,该配合物中碳原子的杂化方式是
 的空间构型为
的空间构型为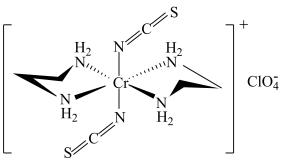
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐2】完成下列问题。
(1)下列状态的N原子或离子在跃迁时;用光谱仪可捕捉到发射光谱的是_______ 。
a. b.
b.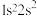 c.
c. d.
d.
(2)已知下图均与第三周期的主族元素有关。
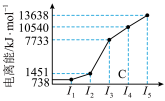
图甲
图甲表示第一至第五电离能数据,则该元素的原子有_______ 种不同运动状态的电子,基态原子未成对电子数为_______ 。
(3)以 燃料电池为电源电解法制取
燃料电池为电源电解法制取 ,二氧化氯(
,二氧化氯( )为一稀黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。
)为一稀黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。
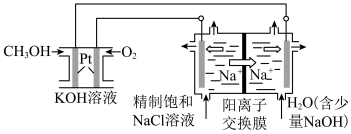
①图中电解池用石墨作电极,在一定条件下电解饱和食盐水制取 ,阳极产生
,阳极产生 的反应式为
的反应式为_______ 。
②电解一段时间,从阴极处收集到的气体比阳极处收集到气体多1.12L时(标准状况,忽略生成的气体溶解),停止电解,通过阳离子交换膜的阳离子为_______ mol(精确到小数点后两位)。
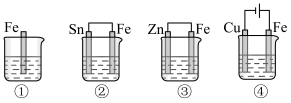
(4)下图所示的各容器中均盛有海水,铁在其中被腐蚀时由快到慢的顺序是_______。
(1)下列状态的N原子或离子在跃迁时;用光谱仪可捕捉到发射光谱的是
a.
 b.
b.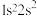 c.
c. d.
d.
(2)已知下图均与第三周期的主族元素有关。

图甲
图甲表示第一至第五电离能数据,则该元素的原子有
(3)以
 燃料电池为电源电解法制取
燃料电池为电源电解法制取 ,二氧化氯(
,二氧化氯( )为一稀黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。
)为一稀黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。
①图中电解池用石墨作电极,在一定条件下电解饱和食盐水制取
 ,阳极产生
,阳极产生 的反应式为
的反应式为②电解一段时间,从阴极处收集到的气体比阳极处收集到气体多1.12L时(标准状况,忽略生成的气体溶解),停止电解,通过阳离子交换膜的阳离子为
(4)下图所示的各容器中均盛有海水,铁在其中被腐蚀时由快到慢的顺序是_______。

| A.④>②>③>① | B.②>①>③>④ | C.④>②>①>③ | D.③>②>④>① |
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】铁是地球上分布最广泛的金属之一,约占地壳质量的 ,仅次于氧、硅、铝,位居地壳含量第四位。蛋白琥珀酸铁
,仅次于氧、硅、铝,位居地壳含量第四位。蛋白琥珀酸铁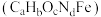 口服液可以用来治疗缺铁性贫血的治疗。请回答以下相关问题:
口服液可以用来治疗缺铁性贫血的治疗。请回答以下相关问题:
(1)写出基态铁原子的价层电子排布式___________ 。
(2)给出蛋白琥珀酸铁含有的 三种元素的第一电离能从小到大排序
三种元素的第一电离能从小到大排序___________ ,并解释原因___________ 。
(3)将 三种元素最简单氢化物按照键角从大到小排序
三种元素最简单氢化物按照键角从大到小排序___________ 。
(4)已知 在元素周期表中位于同主族,将这四种元素的最简单氢化物按照沸点从大到小排序
在元素周期表中位于同主族,将这四种元素的最简单氢化物按照沸点从大到小排序___________ 。
(5)金属羰基化合物在催化反应中有着重要的作用,其本质是金属原子与一氧化碳中的碳原子形成配位键。金属原子在形成最稳定的羰基化合物时要遵守18电子规则,即每个金属原子的价层都满足18电子结构。若金属价层电子数为奇数,则可以通过两个金属原子之间形成共价单键实现价层电子数为偶数。根据以上信息,写出 原子最稳定的羰基化合物的分子式
原子最稳定的羰基化合物的分子式___________ 。
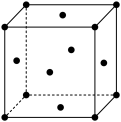
(6)铁有多种同素异形体,在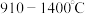 范围内,铁以面心立方最密堆积存在,如图为面心立方堆积的铁的晶胞。已知铁的摩尔质量为
范围内,铁以面心立方最密堆积存在,如图为面心立方堆积的铁的晶胞。已知铁的摩尔质量为 ,铁原子的半径为
,铁原子的半径为 ,给出铁晶胞密度的表达式
,给出铁晶胞密度的表达式___________  。
。
 ,仅次于氧、硅、铝,位居地壳含量第四位。蛋白琥珀酸铁
,仅次于氧、硅、铝,位居地壳含量第四位。蛋白琥珀酸铁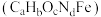 口服液可以用来治疗缺铁性贫血的治疗。请回答以下相关问题:
口服液可以用来治疗缺铁性贫血的治疗。请回答以下相关问题:(1)写出基态铁原子的价层电子排布式
(2)给出蛋白琥珀酸铁含有的
 三种元素的第一电离能从小到大排序
三种元素的第一电离能从小到大排序(3)将
 三种元素最简单氢化物按照键角从大到小排序
三种元素最简单氢化物按照键角从大到小排序(4)已知
 在元素周期表中位于同主族,将这四种元素的最简单氢化物按照沸点从大到小排序
在元素周期表中位于同主族,将这四种元素的最简单氢化物按照沸点从大到小排序(5)金属羰基化合物在催化反应中有着重要的作用,其本质是金属原子与一氧化碳中的碳原子形成配位键。金属原子在形成最稳定的羰基化合物时要遵守18电子规则,即每个金属原子的价层都满足18电子结构。若金属价层电子数为奇数,则可以通过两个金属原子之间形成共价单键实现价层电子数为偶数。根据以上信息,写出
 原子最稳定的羰基化合物的分子式
原子最稳定的羰基化合物的分子式(6)铁有多种同素异形体,在
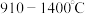 范围内,铁以面心立方最密堆积存在,如图为面心立方堆积的铁的晶胞。已知铁的摩尔质量为
范围内,铁以面心立方最密堆积存在,如图为面心立方堆积的铁的晶胞。已知铁的摩尔质量为 ,铁原子的半径为
,铁原子的半径为 ,给出铁晶胞密度的表达式
,给出铁晶胞密度的表达式 。
。
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
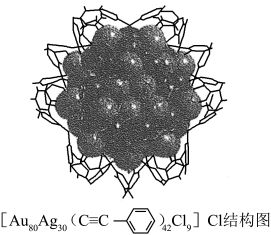
【推荐1】腐蚀、防腐以及催化等化学化工过程都涉及金属纳米团簇的研究,团簇已经成为化学和材料研究的前沿和热点。金属纳米团簇最外层需要配体来稳定,常见有硫醇配体、磷配体和炔配体。卤素作为第二配体或第三配体,其体积比硫醇配体、磷配体和炔配体更小,在形成纳米团簇的过程中空间位阻更小,而且卤素与金、银具有较好的配位能力。
(1)银位于元素周期表第五周期第ⅠB族元素,其价电子排布式为______ 。
(2)金(Au)溶于王水的原理是金与强氧化性的硝酸生成微量的Au3+和NO,盐酸提供的Cl-与Au3+形成[AuCl4]-配离子,写出总反应的离子方程式:______ 。
(3)[Au80Ag30(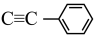 )42Cl9]Cl结构中非金属元素的电负性由大到小的顺序是
)42Cl9]Cl结构中非金属元素的电负性由大到小的顺序是______ 。
(4)第三周期部分主族元素的氟化物的熔点(见表)。
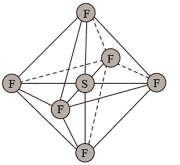
由表中数值可以判断AlF3晶体类型为_______ ,SiF4比SF6熔点低的原因______ ;SF6分子的空间构型为正八面体,如图所示,该分子的键角分别为______ ,它的二氯代物SF4Cl2有______ 种。
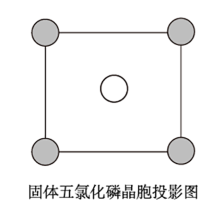
(5)固态五氯化磷为离子晶体,结构单元可以写作PCl 、PCl
、PCl ,晶胞与CsCl相同,该晶胞沿x、y或z轴的投影如图。阳离子中的P杂化方式为:
,晶胞与CsCl相同,该晶胞沿x、y或z轴的投影如图。阳离子中的P杂化方式为:______ ,若密度为dg/cm3,则晶胞参数a=_______ cm(已知阿伏加德罗常数的值为NA,列出计算式即可)
(1)银位于元素周期表第五周期第ⅠB族元素,其价电子排布式为
(2)金(Au)溶于王水的原理是金与强氧化性的硝酸生成微量的Au3+和NO,盐酸提供的Cl-与Au3+形成[AuCl4]-配离子,写出总反应的离子方程式:
(3)[Au80Ag30(
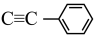 )42Cl9]Cl结构中非金属元素的电负性由大到小的顺序是
)42Cl9]Cl结构中非金属元素的电负性由大到小的顺序是
(4)第三周期部分主族元素的氟化物的熔点(见表)。
| 化合物 | NaF | AlF3 | SiF4 | SF6 |
| 熔点/℃ | 993 | 1040 | -90 | -50.5 |

(5)固态五氯化磷为离子晶体,结构单元可以写作PCl
 、PCl
、PCl ,晶胞与CsCl相同,该晶胞沿x、y或z轴的投影如图。阳离子中的P杂化方式为:
,晶胞与CsCl相同,该晶胞沿x、y或z轴的投影如图。阳离子中的P杂化方式为:
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐2】碳是形成单质和化合物种类最多的元素,其单质及化合物有独特的性质和用途。请回答下列问题。
(1)碳有多种单质,其中石墨烯与金刚石的晶体结构如图1、图2所示。
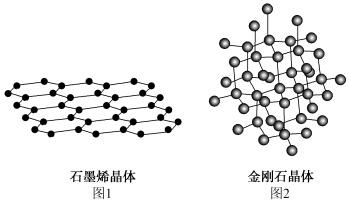
①石墨烯是石墨分离出的单独一层,石墨烯非常稳定,属于厚度只有一个直径大小的“二维材料”,写出一个石墨烯所拥有的特性_____ 。
②求出12g金刚石中含σ键数目为_____ 。
(2)碳的主要氧化物有CO,能与金属Fe形成一种浅黄色液体Fe(CO)5,Fe(CO)5是配合物其熔点为−20℃,沸点为103℃,热稳定性较高,易溶于苯等有机溶剂,不溶于水。据此判断:
①该化合物的晶体中涉及的作用力有_____ 。
A.离子键 B.极性键 C.非极性键 D.范德华力 E.配位键
②算出1molFe(CO)5配合物中含有σ键数目_____ 。
(3)CH 是重要的有机反应中间体,其空间构型为
是重要的有机反应中间体,其空间构型为______ 。
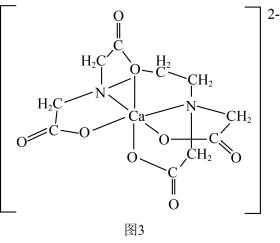
(4)碳的有机物常作为金属有机化合物的配体,如EDTA(乙二胺四乙酸)。EDTA与Ca2+形成的配离子如图3所示。配位体中碳原子的杂化方式有______ 。
(1)碳有多种单质,其中石墨烯与金刚石的晶体结构如图1、图2所示。

①石墨烯是石墨分离出的单独一层,石墨烯非常稳定,属于厚度只有一个直径大小的“二维材料”,写出一个石墨烯所拥有的特性
②求出12g金刚石中含σ键数目为
(2)碳的主要氧化物有CO,能与金属Fe形成一种浅黄色液体Fe(CO)5,Fe(CO)5是配合物其熔点为−20℃,沸点为103℃,热稳定性较高,易溶于苯等有机溶剂,不溶于水。据此判断:
①该化合物的晶体中涉及的作用力有
A.离子键 B.极性键 C.非极性键 D.范德华力 E.配位键
②算出1molFe(CO)5配合物中含有σ键数目
(3)CH
 是重要的有机反应中间体,其空间构型为
是重要的有机反应中间体,其空间构型为(4)碳的有机物常作为金属有机化合物的配体,如EDTA(乙二胺四乙酸)。EDTA与Ca2+形成的配离子如图3所示。配位体中碳原子的杂化方式有

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
【推荐3】砷化铟(InAs)是一种优良的半导体化合物,有广泛用途。
(1)基态In的价层电子排布式为5s25p1,In在周期表中的位置是____________ 。
(2)在Ar保护下分别将InCl3和AsCl3在气化室中加热转化为蒸气,在反应室中混合反应,即可得到橘黄色的InAs晶体。已知:AsCl3和InCl3均为分子晶体。AsCl3沸点为130℃,InCl3沸点为500℃
①33As简化的电子排布式为___________ 。
②AsCl3分子的空间结构为___________ 。
③AsCl3沸点低于InCl3沸点的原因是___________ 。
④InCl3晶体中分子间存在配位键,配位原子是___________ 。
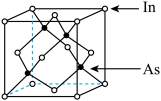
(3)InAs为原子之间以共价键的成键方式结合而成的晶体,其晶胞结构如图所示。已知该晶胞棱长为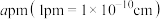 ,阿伏加德罗常数为
,阿伏加德罗常数为 ,InAs的摩尔质量为Mg·mol-1,则该晶体的密度
,InAs的摩尔质量为Mg·mol-1,则该晶体的密度
___________ g·cm-3。
(1)基态In的价层电子排布式为5s25p1,In在周期表中的位置是
(2)在Ar保护下分别将InCl3和AsCl3在气化室中加热转化为蒸气,在反应室中混合反应,即可得到橘黄色的InAs晶体。已知:AsCl3和InCl3均为分子晶体。AsCl3沸点为130℃,InCl3沸点为500℃

①33As简化的电子排布式为
②AsCl3分子的空间结构为
③AsCl3沸点低于InCl3沸点的原因是
④InCl3晶体中分子间存在配位键,配位原子是
(3)InAs为原子之间以共价键的成键方式结合而成的晶体,其晶胞结构如图所示。已知该晶胞棱长为
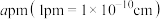 ,阿伏加德罗常数为
,阿伏加德罗常数为 ,InAs的摩尔质量为Mg·mol-1,则该晶体的密度
,InAs的摩尔质量为Mg·mol-1,则该晶体的密度
您最近一年使用:0次



