锑白( ,性质类似
,性质类似 )可用作白色颜料和阻燃剂。一种从含锑工业废渣(主要成分是
)可用作白色颜料和阻燃剂。一种从含锑工业废渣(主要成分是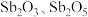 ,含有CuO、
,含有CuO、 和
和 等杂质)中制取
等杂质)中制取 的工业流程如下图所示:
的工业流程如下图所示:
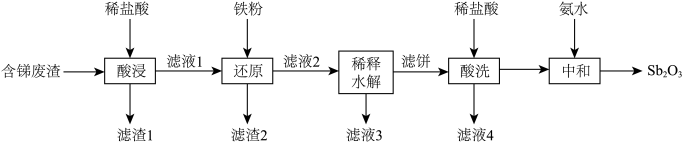
回答下列问题:
(1)锑元素原子序数为51,基态锑原子的价电子轨道表示式为___________ 。
(2)“还原”加入过量铁粉的目的是___________ (填序号)。
a.将 转化为
转化为 b.将
b.将 转化为
转化为 c.将铜离子转化为铜单质
c.将铜离子转化为铜单质
(3)“滤饼”的成分是SbOCl,“稀释水解”主要反应的离子方程式为___________ ;该操作中需要搅拌的原因是___________ 。
(4)“酸洗”后检验沉淀是否洗净的试剂是___________ (填名称)。
(5)“中和”时生成 的化学方程式为
的化学方程式为___________ ,“中和”时不宜将氨水换成氢氧化钠溶液,原因是___________ 。
(6)我国锑的蕴藏量占世界第一位,而锑的化合物也用途广泛。
氟锑酸化学式为 ,酸性比纯硫酸强
,酸性比纯硫酸强 倍,称为超强酸,其与HF作用生成
倍,称为超强酸,其与HF作用生成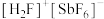 ,则其阳离子的空间结构为
,则其阳离子的空间结构为___________ ,阴离子中心原子的杂化方式合理的是___________ 。
a. b.
b. c.
c. d.
d.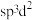
 ,性质类似
,性质类似 )可用作白色颜料和阻燃剂。一种从含锑工业废渣(主要成分是
)可用作白色颜料和阻燃剂。一种从含锑工业废渣(主要成分是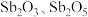 ,含有CuO、
,含有CuO、 和
和 等杂质)中制取
等杂质)中制取 的工业流程如下图所示:
的工业流程如下图所示:
回答下列问题:
(1)锑元素原子序数为51,基态锑原子的价电子轨道表示式为
(2)“还原”加入过量铁粉的目的是
a.将
 转化为
转化为 b.将
b.将 转化为
转化为 c.将铜离子转化为铜单质
c.将铜离子转化为铜单质(3)“滤饼”的成分是SbOCl,“稀释水解”主要反应的离子方程式为
(4)“酸洗”后检验沉淀是否洗净的试剂是
(5)“中和”时生成
 的化学方程式为
的化学方程式为(6)我国锑的蕴藏量占世界第一位,而锑的化合物也用途广泛。
氟锑酸化学式为
 ,酸性比纯硫酸强
,酸性比纯硫酸强 倍,称为超强酸,其与HF作用生成
倍,称为超强酸,其与HF作用生成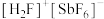 ,则其阳离子的空间结构为
,则其阳离子的空间结构为a.
 b.
b. c.
c. d.
d.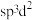
2023·重庆沙坪坝·模拟预测 查看更多[2]
更新时间:2023-05-31 07:07:51
|
相似题推荐
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐1】某火电厂收捕到的粉煤灰的主要成分为SiO2、Al2O3、FeO、Fe2O3、MgO、TiO2等。研究小组对其进行综合处理的流程如下:
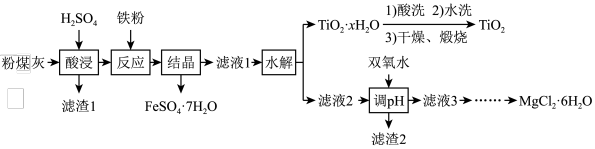
已知:①“酸浸”后钛主要以TiOSO4形式存在,强电解质TiOSO4在溶液中仅能电离SO 和一种阳离子。
和一种阳离子。
②常温下,Ksp[Al(OH)3]=8.0×10−35,Ksp[Fe(OH)3]=4.0×10−38,Ksp[Mg(OH)2]=5.61×10−12。
③滤液1中仍有Fe2+剩余
(1)为了提高粉煤灰浸出速率,在“酸浸”时可采取的措施有___________ (任写一种)。
(2)钛元素发生“水解”反应的离子方程式为___________ 。
(3)加入双氧水的目的是___________ 。滤渣2中的成分分别为Al(OH)3和___________ ,Al(OH)3沉淀完全时(溶液中离子浓度小于10−5mol/L),溶液中的c(OH−)为___________ 。
(4)将MgCl2·6H2O制成无水MgCl2时应注意___________ 。
(5)某同学以石墨为两个电极,电解MgCl2溶液以制取金属镁。你认为他能否获得成功?并用化学方程式解释原因___________ 。

已知:①“酸浸”后钛主要以TiOSO4形式存在,强电解质TiOSO4在溶液中仅能电离SO
 和一种阳离子。
和一种阳离子。②常温下,Ksp[Al(OH)3]=8.0×10−35,Ksp[Fe(OH)3]=4.0×10−38,Ksp[Mg(OH)2]=5.61×10−12。
③滤液1中仍有Fe2+剩余
(1)为了提高粉煤灰浸出速率,在“酸浸”时可采取的措施有
(2)钛元素发生“水解”反应的离子方程式为
(3)加入双氧水的目的是
(4)将MgCl2·6H2O制成无水MgCl2时应注意
(5)某同学以石墨为两个电极,电解MgCl2溶液以制取金属镁。你认为他能否获得成功?并用化学方程式解释原因
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐2】下图中的实线表示元素周期表的边界。①~⑧分别表示元素周期表中对应位置的元素。
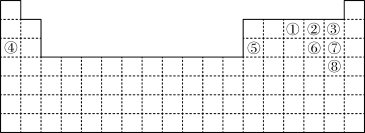
(1)元素周期表体现了元素周期律。元素周期律的本质是________ 。在元素周期表中,元素的位置与结构的关系是______ 。
(2)在上表中画出金属区和非金属区的分界线_______
(3)上述元素所能形成的简单离子中半径最小的是________ (填离子符号),最高价氧化物对应水化物酸性最强的是________ (填分子式)。
(4)④与⑥形成的化合物溶于水后,溶液的pH________ 7。原因________________ (用离子方程式表示),若使其熔化,需破坏的作用力有________________ 。
(5)元素①的氢化物电子式为________________ ,该分子属于________ 晶体。
(6)⑥⑦两元素非金属性较强的是(写元素符号)________ 。写出能证明这一结论的一个实验事实____ 。
(7)⑤、⑦各自的最高价氧化物对应的水化物可以反应生成盐和水,该反应的离子方程式为____ 。
(8)⑦的氢化物的还原性比元素⑥的氢化物的还原性________ (填“强”或“弱”)。

(1)元素周期表体现了元素周期律。元素周期律的本质是
(2)在上表中画出金属区和非金属区的分界线
(3)上述元素所能形成的简单离子中半径最小的是
(4)④与⑥形成的化合物溶于水后,溶液的pH
(5)元素①的氢化物电子式为
(6)⑥⑦两元素非金属性较强的是(写元素符号)
(7)⑤、⑦各自的最高价氧化物对应的水化物可以反应生成盐和水,该反应的离子方程式为
(8)⑦的氢化物的还原性比元素⑥的氢化物的还原性
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐3】按照要求书写方程式。
(1)盐碱地(含较多NaCl、Na2CO3)不利于作物生长,通过施加适量石膏(CaSO4)可以降低土壤的碱性。
用离子方程式表示盐碱地产生碱性的原因:____________________________________ ;
用化学方程式表示用石膏降低其碱性的反应原理:_________________________________ 。
(2)SOCl2是一种液态化合物。向盛有10 ml水的锥形瓶中,小心滴加8~10滴SOCl2,可观察到剧烈反应,液面上有白雾形成,并有带刺激性气味的气体逸出。
请写出SOCl2与水反应的化学方程式:___________________________________________ 。
(3)铅蓄电池是最常见的二次电池,使用方便,安全可靠,在生活中有广泛的应用。
请写出铅蓄电池放电时电池反应的离子方程式:_________________________________ 。
(4)制备像钠、镁、铝这样活泼的金属,电解法几乎是唯一可行的工业方法。
请写出工业上冶炼铝的化学方程式:_____________________________________________ 。
(1)盐碱地(含较多NaCl、Na2CO3)不利于作物生长,通过施加适量石膏(CaSO4)可以降低土壤的碱性。
用离子方程式表示盐碱地产生碱性的原因:
用化学方程式表示用石膏降低其碱性的反应原理:
(2)SOCl2是一种液态化合物。向盛有10 ml水的锥形瓶中,小心滴加8~10滴SOCl2,可观察到剧烈反应,液面上有白雾形成,并有带刺激性气味的气体逸出。
请写出SOCl2与水反应的化学方程式:
(3)铅蓄电池是最常见的二次电池,使用方便,安全可靠,在生活中有广泛的应用。
请写出铅蓄电池放电时电池反应的离子方程式:
(4)制备像钠、镁、铝这样活泼的金属,电解法几乎是唯一可行的工业方法。
请写出工业上冶炼铝的化学方程式:
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
【推荐1】电气石是一种具有保健作用的天然石材,其中含有的主要元素为 等元素。
等元素。
(1)上述元素中,原子半径最小的是_______ (用元素符号表示),与硫同周期的元素中简单离子半径最小的是_______ (用离子符号表示);
(2)用轨道表示式表示氧元素原子核外电子的运动状态_______ ;氧元素原子核外有_______ 种不同能量的电子;
(3) 分子中
分子中 为
为_______ 杂化,键角等于_______ ,可以判断出 分子为
分子为_______ 分子(选填“极性”或“非极性”); 晶体的熔点比
晶体的熔点比 晶体
晶体_______ (选填“高”、“低”),原因为_______ 。
 等元素。
等元素。(1)上述元素中,原子半径最小的是
(2)用轨道表示式表示氧元素原子核外电子的运动状态
(3)
 分子中
分子中 为
为 分子为
分子为 晶体的熔点比
晶体的熔点比 晶体
晶体
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】回答下列问题
(1)Na原子核外共有______ 种不同运动状态的电子,有_____ 种不同能量的电子。
(2)相同压强下,部分元素氟化物的熔点见下表:
试解释上表中氟化物熔点差异的原因:_______ 。
(3)SiF4分子的空间构型为_______ 。
(4)热稳定性:NH3______PH3(填“>”“<”)。沸点:Br2>Cl2,试分析原因__________ 。
(5)试配平该反应的化学方程式,并用短线标出电子转移方向及总数__________ 。
NaIO3+ NaHSO3→ NaHSO4+ Na2SO4+ I2+ H2O
(1)Na原子核外共有
(2)相同压强下,部分元素氟化物的熔点见下表:
| 氟化物 | NaF | MgF2 | SiF4 |
| 熔点/℃ | 1266 | 1534 | 183 |
(3)SiF4分子的空间构型为
(4)热稳定性:NH3______PH3(填“>”“<”)。沸点:Br2>Cl2,试分析原因
(5)试配平该反应的化学方程式,并用短线标出电子转移方向及总数
NaIO3+ NaHSO3→ NaHSO4+ Na2SO4+ I2+ H2O
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】已知  和
和 可以形成
可以形成  和
和  两种化合物,试根据有关信息完成下列问题:
两种化合物,试根据有关信息完成下列问题:
① 内的
内的 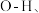 水分子间的范德华力和氢键,从强到弱依次为
水分子间的范德华力和氢键,从强到弱依次为___________ ;
②用球棍模型表示的水分子结构是 ; 可与
可与  形成
形成 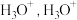 中的
中的 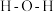 键角比
键角比  的键角
的键角___________ 。(填“大”或“小”)
(2)已知 分子的结构如图所示:
分子的结构如图所示: 分子不是直线形的,两个氢原子犹如在半展开的书的两面上,两个氧原子在书脊位置上,书页夹角
分子不是直线形的,两个氢原子犹如在半展开的书的两面上,两个氧原子在书脊位置上,书页夹角 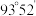 ,而两个
,而两个  键与
键与  键的夹角均为
键的夹角均为 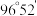 。
。
请回答下列问题:
① 子的电子式是
子的电子式是___________ ,结构式是___________ 。
② 分子是含有
分子是含有___________ 键和___________ 键的___________ (填“极性”或“非极性”)分子。
③ 能与水混溶,却不溶于
能与水混溶,却不溶于  试剂,请予以解释:
试剂,请予以解释:___________ 。
 和
和 可以形成
可以形成  和
和  两种化合物,试根据有关信息完成下列问题:
两种化合物,试根据有关信息完成下列问题: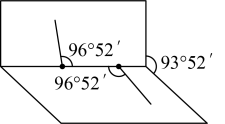
①
 内的
内的 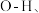 水分子间的范德华力和氢键,从强到弱依次为
水分子间的范德华力和氢键,从强到弱依次为②用球棍模型表示的水分子结构是 ;
A. 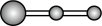 B.
B. 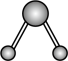 C.
C.  D.
D.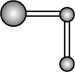
 可与
可与  形成
形成 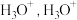 中的
中的 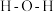 键角比
键角比  的键角
的键角(2)已知
 分子的结构如图所示:
分子的结构如图所示: 分子不是直线形的,两个氢原子犹如在半展开的书的两面上,两个氧原子在书脊位置上,书页夹角
分子不是直线形的,两个氢原子犹如在半展开的书的两面上,两个氧原子在书脊位置上,书页夹角 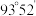 ,而两个
,而两个  键与
键与  键的夹角均为
键的夹角均为 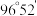 。
。请回答下列问题:
①
 子的电子式是
子的电子式是②
 分子是含有
分子是含有③
 能与水混溶,却不溶于
能与水混溶,却不溶于  试剂,请予以解释:
试剂,请予以解释:
您最近一年使用:0次
【推荐1】⑴已知在周期表的某一周期,其零族元素的价层电子排布式为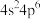 ,同周期的A、B两种元素,最外层电子数为2、7,次外层电子数为8、18,则元素A为
,同周期的A、B两种元素,最外层电子数为2、7,次外层电子数为8、18,则元素A为________ ,B为________ (写元素符号)。若周期表有第8周期,则其最终的零族元素的原子序数为____________ 。
⑵稀有气体的化合物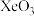 分子的空间构型是
分子的空间构型是__________ ,写出与其互为等电子体的一种阴离子的化学式___________ 。
⑶硼酸能形成类似于石墨的层状结构,单层的结构如图所示
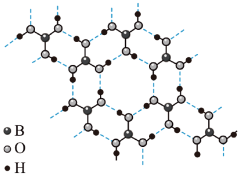
则硼酸晶体中存在的作用力除共价键外,还有_____________ 。
⑷稀土资源是重要的战略资源,下图为某稀土元素A的氧化物晶体的立方晶胞结构示意图,其中氧离子占据顶点、面心、棱心、体心的位置,A离子占据半数的立方体空隙

写出A氧化物的化学式______ ,A离子的配位数为______ 。已知晶胞参数为 ,则
,则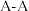 间距为
间距为________ 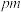 ,设A的摩尔质量为
,设A的摩尔质量为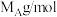 ,晶体的密度为
,晶体的密度为_______  。
。
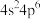 ,同周期的A、B两种元素,最外层电子数为2、7,次外层电子数为8、18,则元素A为
,同周期的A、B两种元素,最外层电子数为2、7,次外层电子数为8、18,则元素A为⑵稀有气体的化合物
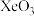 分子的空间构型是
分子的空间构型是⑶硼酸能形成类似于石墨的层状结构,单层的结构如图所示

则硼酸晶体中存在的作用力除共价键外,还有
⑷稀土资源是重要的战略资源,下图为某稀土元素A的氧化物晶体的立方晶胞结构示意图,其中氧离子占据顶点、面心、棱心、体心的位置,A离子占据半数的立方体空隙

写出A氧化物的化学式
 ,则
,则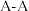 间距为
间距为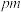 ,设A的摩尔质量为
,设A的摩尔质量为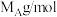 ,晶体的密度为
,晶体的密度为 。
。
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】75号元素铼Re,熔点仅次于钨,是制造航空发动机的必需元素。地壳中铼的含量极低,多伴生于钼、铜、锌、铅等矿物中。回答下列问题:
(1)锰原子价层电子的轨道表示式为__ ,锰处于周期表的__ 区。
(2)与铼伴生的铜能形成多种配合物。如:醋酸二氨合铜(I)[Cu(NH3)2]Ac可用于吸收合成氨中对催化剂有害的CO气体:[Cu(NH3)2]Ac+CO+NH3 [Cu(NH3)3]Ac·CO。(Ac表示醋酸根)
[Cu(NH3)3]Ac·CO。(Ac表示醋酸根)
①与铜离子形成配合物的分子或离子应具备的结构特征是__ 。
②醋酸根中C原子的杂化类型为__ ,1mol配离子[Cu(NH3)2]+中含有σ键的数目为__ 。
③写出与NH3互为等电子体的一种离子的化学式__ 。
(3)锰与铼处于同一族,金属铼的熔点高于锰,原因是___ 。
(4)三氧化铼为立方晶胞,晶胞参数为apm,三氧化铼的摩尔质量为Mg/mol;铼原子占据顶点,氧原子占据所有棱心。则铼原子的配位数为__ ,铼原子填在了氧原子围成的空隙中___ (填“四面体”“立方体”或“八面体”),三氧化铼的密度为__ g/cm3。(用NA表示阿伏加 德罗常数的值)
(1)锰原子价层电子的轨道表示式为
(2)与铼伴生的铜能形成多种配合物。如:醋酸二氨合铜(I)[Cu(NH3)2]Ac可用于吸收合成氨中对催化剂有害的CO气体:[Cu(NH3)2]Ac+CO+NH3
 [Cu(NH3)3]Ac·CO。(Ac表示醋酸根)
[Cu(NH3)3]Ac·CO。(Ac表示醋酸根)①与铜离子形成配合物的分子或离子应具备的结构特征是
②醋酸根中C原子的杂化类型为
③写出与NH3互为等电子体的一种离子的化学式
(3)锰与铼处于同一族,金属铼的熔点高于锰,原因是
(4)三氧化铼为立方晶胞,晶胞参数为apm,三氧化铼的摩尔质量为Mg/mol;铼原子占据顶点,氧原子占据所有棱心。则铼原子的配位数为
您最近一年使用:0次
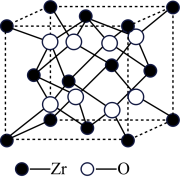
【推荐3】研究发现,在 低压合成甲醇的反应(
低压合成甲醇的反应(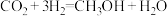 )中,钴氧化物负载的锰氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。回答下列问题:
)中,钴氧化物负载的锰氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。回答下列问题:
(1)基态 原子的价电子排布式为
原子的价电子排布式为___________ 。
(2)基态 原子核外一共有
原子核外一共有___________ 种不同运动状态的电子。
(3) 和
和 分子中
分子中 原子的杂化类型分别为
原子的杂化类型分别为___________ 和___________ 。
(4) 是制备上述反应催化剂的原料,
是制备上述反应催化剂的原料, 的空间构型为
的空间构型为___________ ,与 互为等电子体的分子为
互为等电子体的分子为___________ (任写一种)。
(5)在 、
、 、
、 三种物质中,沸点从高到低的顺序为
三种物质中,沸点从高到低的顺序为___________ ,原因是___________ 。
(6)我国科学家发明了高选择性的二氧化碳加氢合成甲醇的催化剂,其组成为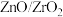 固溶体。四方
固溶体。四方 晶胞如图所示。
晶胞如图所示。 离子在晶胞中的配位数是
离子在晶胞中的配位数是___________ ,晶胞参数为 、
、 、
、 ,该晶体密度为
,该晶体密度为___________  (写出表达式即可)。在
(写出表达式即可)。在 中掺杂少量
中掺杂少量 后形成的催化剂,化学式可表示为
后形成的催化剂,化学式可表示为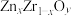 ,则y=
,则y=___________ (用含x的代数式表达)。
 低压合成甲醇的反应(
低压合成甲醇的反应(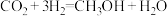 )中,钴氧化物负载的锰氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。回答下列问题:
)中,钴氧化物负载的锰氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。回答下列问题:(1)基态
 原子的价电子排布式为
原子的价电子排布式为(2)基态
 原子核外一共有
原子核外一共有(3)
 和
和 分子中
分子中 原子的杂化类型分别为
原子的杂化类型分别为(4)
 是制备上述反应催化剂的原料,
是制备上述反应催化剂的原料, 的空间构型为
的空间构型为 互为等电子体的分子为
互为等电子体的分子为(5)在
 、
、 、
、 三种物质中,沸点从高到低的顺序为
三种物质中,沸点从高到低的顺序为(6)我国科学家发明了高选择性的二氧化碳加氢合成甲醇的催化剂,其组成为
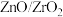 固溶体。四方
固溶体。四方 晶胞如图所示。
晶胞如图所示。 离子在晶胞中的配位数是
离子在晶胞中的配位数是 、
、 、
、 ,该晶体密度为
,该晶体密度为 (写出表达式即可)。在
(写出表达式即可)。在 中掺杂少量
中掺杂少量 后形成的催化剂,化学式可表示为
后形成的催化剂,化学式可表示为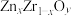 ,则y=
,则y=
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐1】纳米级超细碳酸钙是一种新型超细固体材料,是橡胶、塑料制品、造纸、涂料、油墨等工业重要填料。工业上用石灰石来制备纳米级超细碳酸钙的流程如图,请回答下列问题:
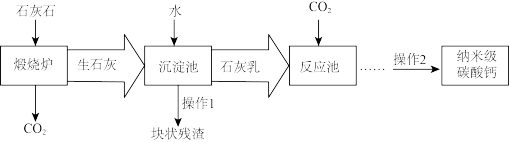
(1)煅烧炉中发生反应的化学方程式是___ 。
(2)沉淀池中反应的基本类型属于___ 。操作1、2与实验室___ 操作类似,需要用到的玻璃仪器有___ 。
(3)上述流程中可循环使用的物质的化学式为___ 。

(1)煅烧炉中发生反应的化学方程式是
(2)沉淀池中反应的基本类型属于
(3)上述流程中可循环使用的物质的化学式为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐2】孔雀石的主要成分为 ,还含有
,还含有 、
、 、
、 ,工业上以孔雀石为原料制备
,工业上以孔雀石为原料制备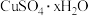 晶体的流程如下图:
晶体的流程如下图:
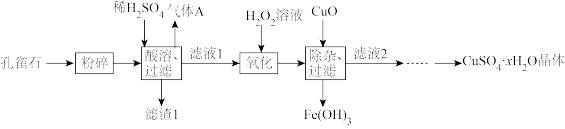
(1)粉碎孔雀石的目的为___________ 。
(2)滤渣1为___________ (填化学式)。
(3)气体A可用于制备 ,应先将
,应先将___________ (填化学式)通入饱和食盐水,再通入___________ (同上)。
(4)写出“氧化”过程中发生的离子反应方程式___________ ,该过程需在室温下进行,温度过高,反应速率变慢,原因是___________ 。
(5)从滤液2中得到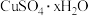 晶体的操作为
晶体的操作为___________ 、过滤、乙醇洗涤、干燥。乙醇洗涤的目的为:①洗去晶体表面的杂质;②___________ ;③___________ 。
(6)蓝铜矿是孔雀石的共生矿,其主要成分为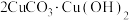 ,将它与焦炭一起加热时,可以冶炼铜,同时生成气体A,写出该过程的化学反应方程式
,将它与焦炭一起加热时,可以冶炼铜,同时生成气体A,写出该过程的化学反应方程式___________ 。
 ,还含有
,还含有 、
、 、
、 ,工业上以孔雀石为原料制备
,工业上以孔雀石为原料制备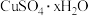 晶体的流程如下图:
晶体的流程如下图:
(1)粉碎孔雀石的目的为
(2)滤渣1为
(3)气体A可用于制备
 ,应先将
,应先将(4)写出“氧化”过程中发生的离子反应方程式
(5)从滤液2中得到
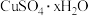 晶体的操作为
晶体的操作为(6)蓝铜矿是孔雀石的共生矿,其主要成分为
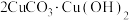 ,将它与焦炭一起加热时,可以冶炼铜,同时生成气体A,写出该过程的化学反应方程式
,将它与焦炭一起加热时,可以冶炼铜,同时生成气体A,写出该过程的化学反应方程式
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
【推荐3】重铬酸钠(Na2Cr2O7)广泛用于合成颜料、媒染剂等。以铬铁矿(主要成分为Cr2O3,还含有FeO、Al2O3、SiO2等杂质)为原料制取重铬酸钠的流程图如下:

请回答下列问题:
(1)若步骤Ⅰ中只用一种试剂调节溶液的pH,应选用______ (填标号)。
A 稀硫酸 B 氢氧化钠固体 C 氢氧化钾溶液
(2)步骤Ⅰ中,调节溶液pH后,如果溶液的pH过小,可能导致W沉淀部分溶解,原因是:_____________ (用离子方程式表示)。
(3)步骤Ⅱ中,Na2CrO4转化为Na2Cr2O7的离子反应如下:2 (黄色)+2H+
(黄色)+2H+
 (橙红色)+H2O
(橙红色)+H2O
①该反应________ 氧化还原反应(填“是”或“不是”),反应的平衡常数表达式:K=________ 。
②若向Na2Cr2O7溶液(橙红色)中加入足量NaOH固体,溶液________ (填标号)。
A.变黄色 B.颜色不变 C.橙红色变深
③已知:25 ℃时,Ag2CrO4的Ksp=1.12×10-12,Ag2Cr2O7的Ksp=2×10-7。25℃时,向Na2Cr2O7溶液中加入AgNO3溶液,最终只生成一种砖红色沉淀,该沉淀的化学式是_______ 。

请回答下列问题:
(1)若步骤Ⅰ中只用一种试剂调节溶液的pH,应选用
A 稀硫酸 B 氢氧化钠固体 C 氢氧化钾溶液
(2)步骤Ⅰ中,调节溶液pH后,如果溶液的pH过小,可能导致W沉淀部分溶解,原因是:
(3)步骤Ⅱ中,Na2CrO4转化为Na2Cr2O7的离子反应如下:2
 (黄色)+2H+
(黄色)+2H+
 (橙红色)+H2O
(橙红色)+H2O①该反应
②若向Na2Cr2O7溶液(橙红色)中加入足量NaOH固体,溶液
A.变黄色 B.颜色不变 C.橙红色变深
③已知:25 ℃时,Ag2CrO4的Ksp=1.12×10-12,Ag2Cr2O7的Ksp=2×10-7。25℃时,向Na2Cr2O7溶液中加入AgNO3溶液,最终只生成一种砖红色沉淀,该沉淀的化学式是
您最近一年使用:0次



