按照要求书写方程式。
(1)盐碱地(含较多NaCl、Na2CO3)不利于作物生长,通过施加适量石膏(CaSO4)可以降低土壤的碱性。
用离子方程式表示盐碱地产生碱性的原因:____________________________________ ;
用化学方程式表示用石膏降低其碱性的反应原理:_________________________________ 。
(2)SOCl2是一种液态化合物。向盛有10 ml水的锥形瓶中,小心滴加8~10滴SOCl2,可观察到剧烈反应,液面上有白雾形成,并有带刺激性气味的气体逸出。
请写出SOCl2与水反应的化学方程式:___________________________________________ 。
(3)铅蓄电池是最常见的二次电池,使用方便,安全可靠,在生活中有广泛的应用。
请写出铅蓄电池放电时电池反应的离子方程式:_________________________________ 。
(4)制备像钠、镁、铝这样活泼的金属,电解法几乎是唯一可行的工业方法。
请写出工业上冶炼铝的化学方程式:_____________________________________________ 。
(1)盐碱地(含较多NaCl、Na2CO3)不利于作物生长,通过施加适量石膏(CaSO4)可以降低土壤的碱性。
用离子方程式表示盐碱地产生碱性的原因:
用化学方程式表示用石膏降低其碱性的反应原理:
(2)SOCl2是一种液态化合物。向盛有10 ml水的锥形瓶中,小心滴加8~10滴SOCl2,可观察到剧烈反应,液面上有白雾形成,并有带刺激性气味的气体逸出。
请写出SOCl2与水反应的化学方程式:
(3)铅蓄电池是最常见的二次电池,使用方便,安全可靠,在生活中有广泛的应用。
请写出铅蓄电池放电时电池反应的离子方程式:
(4)制备像钠、镁、铝这样活泼的金属,电解法几乎是唯一可行的工业方法。
请写出工业上冶炼铝的化学方程式:
更新时间:2021-08-17 19:49:42
|
相似题推荐
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐1】铝是一种应用广泛的金属。以铝土矿(主要成分为 ,含
,含 和
和 等杂质)为原料制备铝的一种工艺流程如图:
等杂质)为原料制备铝的一种工艺流程如图:
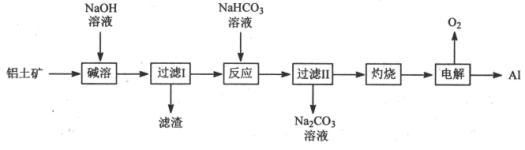
注: 在“碱溶”时转化为铝硅酸钠沉淀。
在“碱溶”时转化为铝硅酸钠沉淀。
(1)“碱溶”时生成偏铝酸钠的离子方程式为_______ 。
(2)“过滤Ⅰ”中产生的滤渣除铝硅酸钠外还有_______ 。(填化学式)。
(3)“反应”流程中的化学方程式为_______ 。
(4)下列仪器可用于实验室进行灼烧实验的是_______(填字母)。
(5)“电解”流程中的能量转化形式为_______ (填“化学能转化成电能”或“电能转化成化学能”)。
 ,含
,含 和
和 等杂质)为原料制备铝的一种工艺流程如图:
等杂质)为原料制备铝的一种工艺流程如图:
注:
 在“碱溶”时转化为铝硅酸钠沉淀。
在“碱溶”时转化为铝硅酸钠沉淀。(1)“碱溶”时生成偏铝酸钠的离子方程式为
(2)“过滤Ⅰ”中产生的滤渣除铝硅酸钠外还有
(3)“反应”流程中的化学方程式为
(4)下列仪器可用于实验室进行灼烧实验的是_______(填字母)。
A.酒精灯 | B.试管 | C.蒸发皿 | D.坩埚 |
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐2】高铝粉煤灰提取铝既能缓解我国缺铝矿的现状,又能减少煤燃烧产生的污染。高铝粉煤灰含55.22% Al2O3、32.58% SiO2、5.08% CaO、2.09% Fe2O3和5.03%其他杂质。活化焙烧法从高铝粉煤灰中提取铝的工艺流程如图所示,回答下列问题:

(1)碱石灰烧结法是利用高铝粉煤灰与纯碱、焦炭1220℃烧结,Al2O3转化为易溶的偏铝酸钠,从而将铝元素分离出来,烧结过程无污染,氧化铝发生反应的化学方程式是_______ 。
(2)活化焙烧过程中,不同活化剂对铝、钙浸出率的影响不同(如下表),应选择_______ 做活化剂。
(3)酸浸使用的酸是_______ ,酸的浓度与氧化铝溶出率的关系如图1,酸浓度为36%时达到最大溶出率,但实际工业使用32%的酸浓度,原因是_______ 。酸溶温度与氧化铝溶出率的关系如图2,选择的最佳温度是_______ 。
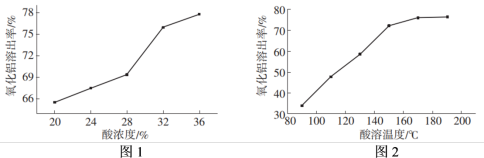
(4)流程图中的一系列操作应包括_______ 、过滤、洗涤、干燥,粗氧化铝的主要杂质是_______ 。
(5)电解过程中阴极的电极反应式为_______ ,现有102 t高铝粉煤灰,如果总转化率为75%,可以得到_______ t铝(计算结果保留四位有效数字)。

(1)碱石灰烧结法是利用高铝粉煤灰与纯碱、焦炭1220℃烧结,Al2O3转化为易溶的偏铝酸钠,从而将铝元素分离出来,烧结过程无污染,氧化铝发生反应的化学方程式是
(2)活化焙烧过程中,不同活化剂对铝、钙浸出率的影响不同(如下表),应选择
活化剂 | Na3PO4 | Na2HPO4 | NaF | Na2SO4 | CH3COONa |
Al浸出率 | 83.82% | 83.62% | 85.64% | 77.55% | 90.96% |
Ca浸出率 | 97.10% | 97.75% | 98.26% | 96.79% | 90.96% |
(3)酸浸使用的酸是

(4)流程图中的一系列操作应包括
(5)电解过程中阴极的电极反应式为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
【推荐3】石墨在材料领域有重要应用,某初级石墨中含 (7.8%)、
(7.8%)、 (5.1%)和
(5.1%)和 (3.1%)等杂质,提纯与综合利用工艺流程如下:
(3.1%)等杂质,提纯与综合利用工艺流程如下:
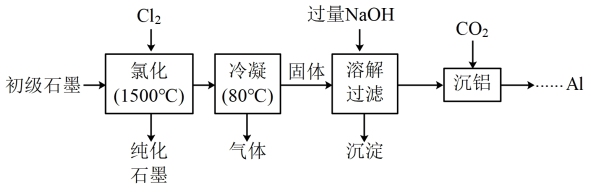
已知:①氯化后,石墨中氧化物杂质均转变为相应的氯化物;
② 的沸点为57.6℃,金属氯化物的沸点均高于150℃。
的沸点为57.6℃,金属氯化物的沸点均高于150℃。
(1)“氯化”时,先向反应器中通入 一段时间,再加热,主要目的是
一段时间,再加热,主要目的是_______ 。
(2)“冷凝”后,所得“气体"的成分有 和
和_______ (填化学式)。
(3)“溶解过滤”时,加过量NaOH溶液的目的是_______ ;取少量滤液于试管中,_______ (实验操作及现象),证明沉淀已完全。
(4)“沉铝”得到的产物为 ,工业上由
,工业上由 得到Al,需发生两步反应,写出方程式:
得到Al,需发生两步反应,写出方程式: 、
、_______ 。
(5)写出Al的一种用途_______ 。
(6)100kg初级石墨最多可获得Al的质量为_______ kg。
 (7.8%)、
(7.8%)、 (5.1%)和
(5.1%)和 (3.1%)等杂质,提纯与综合利用工艺流程如下:
(3.1%)等杂质,提纯与综合利用工艺流程如下:
已知:①氯化后,石墨中氧化物杂质均转变为相应的氯化物;
②
 的沸点为57.6℃,金属氯化物的沸点均高于150℃。
的沸点为57.6℃,金属氯化物的沸点均高于150℃。(1)“氯化”时,先向反应器中通入
 一段时间,再加热,主要目的是
一段时间,再加热,主要目的是(2)“冷凝”后,所得“气体"的成分有
 和
和(3)“溶解过滤”时,加过量NaOH溶液的目的是
(4)“沉铝”得到的产物为
 ,工业上由
,工业上由 得到Al,需发生两步反应,写出方程式:
得到Al,需发生两步反应,写出方程式: 、
、(5)写出Al的一种用途
(6)100kg初级石墨最多可获得Al的质量为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐1】下列框图中的字母分别代表一种常见的物质或其溶液,相互之间的转化关系如下图所示(部分产物及反应条件已略去)。已知A、B为气态单质,F是地壳中含量最多的金属元素的单质;E、H、I均为氧化物,E为黑色固体,I为红棕色气体;M为红褐色沉淀。

请回答下列问题:
(1)B中所含元素位于周期表中第________ 周期,________ 族。
(2)A在B中燃烧的现象是_____________________________ 。
(3)D+E→B的反应中,被氧化与被还原的物质的物质的量之比是________ 。
(4)G+J→M的离子方程式是__________________________ 。

请回答下列问题:
(1)B中所含元素位于周期表中第
(2)A在B中燃烧的现象是
(3)D+E→B的反应中,被氧化与被还原的物质的物质的量之比是
(4)G+J→M的离子方程式是
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐2】铬合金具有高硬度、耐腐蚀特性,广泛应用于精密仪器制造,由高碳铬铁合金废料制取铬的简单流程如下:
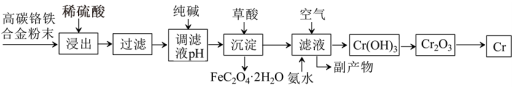
已知:Cr+H2SO4=CrSO4+H2↑
请回答下列问题:
(1)稀硫酸酸浸过程中,提高“浸出率”的措施有___________ (写一条即可)
(2)用纯碱调节溶液酸度,若纯碱过量,则可能导致的后果是___________ ,副产物中两种主要物质的化学式为___________ 。
(3)加入草酸发生反应的离子方程式为____ ;
(4)向滤液中通入空气,加入氨水后发生反应的化学方程式为____
(5)已知高碳铬铁度料中铁铬元素质量比为14:13,上述流程中铁元素转化草酸亚铁的利用率为80%。废料中提取金属铬的总转化率为95%,如果得到草酸亚铁晶体(FeC2O4·2H2O)质量为18.00吨,则可以冶炼铬的质量为___________ 吨(结果保留 1位小数)。

已知:Cr+H2SO4=CrSO4+H2↑
请回答下列问题:
(1)稀硫酸酸浸过程中,提高“浸出率”的措施有
(2)用纯碱调节溶液酸度,若纯碱过量,则可能导致的后果是
(3)加入草酸发生反应的离子方程式为
(4)向滤液中通入空气,加入氨水后发生反应的化学方程式为
(5)已知高碳铬铁度料中铁铬元素质量比为14:13,上述流程中铁元素转化草酸亚铁的利用率为80%。废料中提取金属铬的总转化率为95%,如果得到草酸亚铁晶体(FeC2O4·2H2O)质量为18.00吨,则可以冶炼铬的质量为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐3】以红土镍矿(主要成分为NiO、FeO、Fe2O3、MgO和SiO2等)为原料制备Ni(OH)2的工艺流程如图:

(1)“酸浸”时,可以加快化学反应速率的措施___________ (写一条即可)。滤渣Ⅰ的成分为___________ (填化学式)。
(2)“氧化”时,Fe2+发生反应的离子方程式为___________ 。
(3)结合方程式为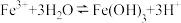 ,说明加入MgO可以达到沉铁目的的原因
,说明加入MgO可以达到沉铁目的的原因___________ 。
(4)要使Fe3+沉淀完全,根据表中的数据,用MgO调节溶液pH的范围是_______ 。

(1)“酸浸”时,可以加快化学反应速率的措施
(2)“氧化”时,Fe2+发生反应的离子方程式为
(3)结合方程式为
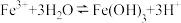 ,说明加入MgO可以达到沉铁目的的原因
,说明加入MgO可以达到沉铁目的的原因(4)要使Fe3+沉淀完全,根据表中的数据,用MgO调节溶液pH的范围是
| 金属离子 | Fe2+ | Fe3+ | Mg2+ | Ni2+ |
| 开始沉淀的pH | 6.3 | 1.5 | 8.9 | 6.9 |
| 沉淀完全的pH | 8.3 | 2.8 | 10.9 | 8.9 |
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】在生活中亚硝酸钠(NaNO2)应用十分广泛,少量可做食品的护色剂,可防止肉毒杆菌在肉类食品中生长,还可用于治疗氰化物中毒等。某化学兴趣小组利用下列装置设计制备干燥的亚硝酸钠(夹持及加热装置略去,部分仪器可重复使用)。
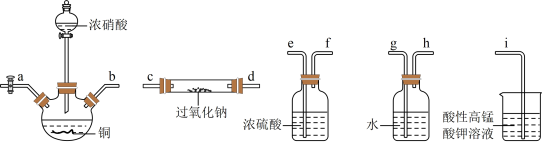
已知:①2NO+Na2O2=2NaNO2
②NO能被酸性高锰酸钾氧化为NO ,但不能被浓硫酸氧化。
,但不能被浓硫酸氧化。
回答下列问题:
(1)盛装浓硝酸的仪器名称是___________ ;铜元素位于元素周期表的________ 区。
(2)上述仪器连接顺序为______________ (气流方向从左向右,用小写字母表示)。
(3)若没有盛装浓硫酸的洗气瓶,硬质玻璃管中可能发生的副反应的化学方程式为___________ 。
(4)反应结束后需要打开止水夹a,继续通入一段时间氮气,目的是____________ 。
(5)酸性高锰酸钾溶液中发生反应的离子方程式为__________________ 。
(6)NaNO2溶液呈碱性,原因是_____________ (用离子方程式表示)。
(7)为测定产品的纯度,需配制体积为200mL的一定物质的量浓度的样品溶液,配制过程中,必须使用的玻璃仪器有烧杯、玻璃棒、_____________________ 。

已知:①2NO+Na2O2=2NaNO2
②NO能被酸性高锰酸钾氧化为NO
 ,但不能被浓硫酸氧化。
,但不能被浓硫酸氧化。回答下列问题:
(1)盛装浓硝酸的仪器名称是
(2)上述仪器连接顺序为
(3)若没有盛装浓硫酸的洗气瓶,硬质玻璃管中可能发生的副反应的化学方程式为
(4)反应结束后需要打开止水夹a,继续通入一段时间氮气,目的是
(5)酸性高锰酸钾溶液中发生反应的离子方程式为
(6)NaNO2溶液呈碱性,原因是
(7)为测定产品的纯度,需配制体积为200mL的一定物质的量浓度的样品溶液,配制过程中,必须使用的玻璃仪器有烧杯、玻璃棒、
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
【推荐2】锑白( ,性质类似
,性质类似 )可用作白色颜料和阻燃剂。一种从含锑工业废渣(主要成分是
)可用作白色颜料和阻燃剂。一种从含锑工业废渣(主要成分是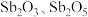 ,含有CuO、
,含有CuO、 和
和 等杂质)中制取
等杂质)中制取 的工业流程如下图所示:
的工业流程如下图所示:
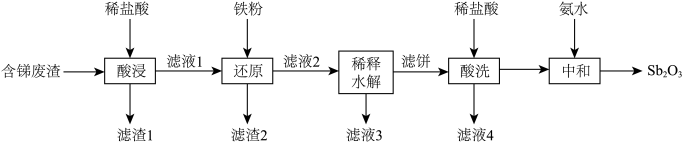
回答下列问题:
(1)锑元素原子序数为51,基态锑原子的价电子轨道表示式为___________ 。
(2)“还原”加入过量铁粉的目的是___________ (填序号)。
a.将 转化为
转化为 b.将
b.将 转化为
转化为 c.将铜离子转化为铜单质
c.将铜离子转化为铜单质
(3)“滤饼”的成分是SbOCl,“稀释水解”主要反应的离子方程式为___________ ;该操作中需要搅拌的原因是___________ 。
(4)“酸洗”后检验沉淀是否洗净的试剂是___________ (填名称)。
(5)“中和”时生成 的化学方程式为
的化学方程式为___________ ,“中和”时不宜将氨水换成氢氧化钠溶液,原因是___________ 。
(6)我国锑的蕴藏量占世界第一位,而锑的化合物也用途广泛。
氟锑酸化学式为 ,酸性比纯硫酸强
,酸性比纯硫酸强 倍,称为超强酸,其与HF作用生成
倍,称为超强酸,其与HF作用生成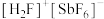 ,则其阳离子的空间结构为
,则其阳离子的空间结构为___________ ,阴离子中心原子的杂化方式合理的是___________ 。
a. b.
b. c.
c. d.
d.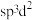
 ,性质类似
,性质类似 )可用作白色颜料和阻燃剂。一种从含锑工业废渣(主要成分是
)可用作白色颜料和阻燃剂。一种从含锑工业废渣(主要成分是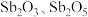 ,含有CuO、
,含有CuO、 和
和 等杂质)中制取
等杂质)中制取 的工业流程如下图所示:
的工业流程如下图所示:
回答下列问题:
(1)锑元素原子序数为51,基态锑原子的价电子轨道表示式为
(2)“还原”加入过量铁粉的目的是
a.将
 转化为
转化为 b.将
b.将 转化为
转化为 c.将铜离子转化为铜单质
c.将铜离子转化为铜单质(3)“滤饼”的成分是SbOCl,“稀释水解”主要反应的离子方程式为
(4)“酸洗”后检验沉淀是否洗净的试剂是
(5)“中和”时生成
 的化学方程式为
的化学方程式为(6)我国锑的蕴藏量占世界第一位,而锑的化合物也用途广泛。
氟锑酸化学式为
 ,酸性比纯硫酸强
,酸性比纯硫酸强 倍,称为超强酸,其与HF作用生成
倍,称为超强酸,其与HF作用生成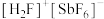 ,则其阳离子的空间结构为
,则其阳离子的空间结构为a.
 b.
b. c.
c. d.
d.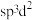
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】甲、乙、丙三种物质都含有A元素,只有甲是单质,其转化关系如下:
甲 乙
乙 丙
丙
(1)若乙是目前世界倡导需减少排放的温室气体,丁也含有A元素。则含有7个中子的核素A可用符号表示为___________ ,丁溶液呈碱性的原因用离子方程式表示为___________ ;已知:在常温常压下,1mol甲和一氧化碳分别与充足的氧气反应放出的热量分别是393.5kJ、283.0kJ。试写出甲与乙相互反应的热化学方程式___________ 。
(2)若A是非金属元素,其次外层电子是最外层电子数的2倍,则乙在现代通讯中可用于制造___________ ,写出一个有丙参加的、能证明碳的非金属性强于A的化学方程式___________ ;
(3)若甲是生活中最常用的过渡金属单质,其在点燃条件与氧气反应生成乙。若丁是稀盐酸,则乙→丙的化学方程式为___________ 。
甲
 乙
乙 丙
丙(1)若乙是目前世界倡导需减少排放的温室气体,丁也含有A元素。则含有7个中子的核素A可用符号表示为
(2)若A是非金属元素,其次外层电子是最外层电子数的2倍,则乙在现代通讯中可用于制造
(3)若甲是生活中最常用的过渡金属单质,其在点燃条件与氧气反应生成乙。若丁是稀盐酸,则乙→丙的化学方程式为
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
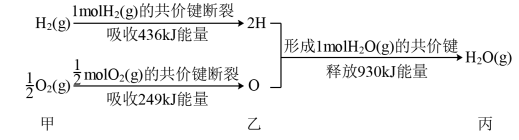
【推荐1】(1)根据下列信息判断氢气燃烧生成水时的热量变化:
①H2(g)与O2(g)反应生成1molH2O(g)时放出的热量为_________ kJ;
②图中甲、乙、丙中物质所具有的总能量由大到小顺序为:_____________ ;
(2)铅蓄电池是最常见的二次电池,放电时的化学方程式为:Pb(s)+PbO2(s)+2H2SO4(aq)=2PbSO4(s)+2H2O。负极反应式为________ ,一段时间后,负极增重48克,转移电子_______ mol。

①H2(g)与O2(g)反应生成1molH2O(g)时放出的热量为
②图中甲、乙、丙中物质所具有的总能量由大到小顺序为:
(2)铅蓄电池是最常见的二次电池,放电时的化学方程式为:Pb(s)+PbO2(s)+2H2SO4(aq)=2PbSO4(s)+2H2O。负极反应式为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】(I)用如图所示装置进行中和反应反应热的测定实验,请回答下列问题:
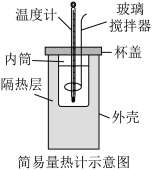
(1)取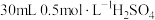 溶液与
溶液与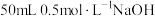 溶液在小烧杯中进行中和反应,三次实验后通过计算可得生成
溶液在小烧杯中进行中和反应,三次实验后通过计算可得生成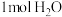 时放出的热量为54.8
时放出的热量为54.8 。其结果与理论数据有偏差,产生此偏差的原因可能是
。其结果与理论数据有偏差,产生此偏差的原因可能是_______ (填字母序号)。
A. 实验装置保温、隔热效果差
B. 用温度计测定 溶液起始温度后直接测定
溶液起始温度后直接测定 溶液的温度
溶液的温度
C. 一次性把 溶液倒入盛有硫酸的小烧杯中
溶液倒入盛有硫酸的小烧杯中
(2)实验中若改用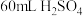
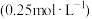 溶液与
溶液与 溶液进行反应,与上述实验相比,通过计算可得生成
溶液进行反应,与上述实验相比,通过计算可得生成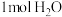 时所放出的热量
时所放出的热量_______ (填“相等”、“不相等”)。若用 醋酸代替
醋酸代替 溶液进行上述实验,测得反应前后温度的变化值会
溶液进行上述实验,测得反应前后温度的变化值会_______ 。(“偏大”、“偏小”、“不受影响)
(II)铅蓄电池是化学电源,它工作时的电池反应为:PbO2+Pb+2H2SO4=2PbSO4+2H2O。试回答:
(3)铅蓄电池正极的电极材料是_______ 。
(4)工作时该铅蓄电池负极的电极反应是_______ 。
(5)铅蓄电池工作时,电解质溶液的浓度_______ (填“减小”“增大”或“不变”,下同),pH_______ 。

(1)取
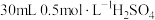 溶液与
溶液与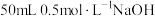 溶液在小烧杯中进行中和反应,三次实验后通过计算可得生成
溶液在小烧杯中进行中和反应,三次实验后通过计算可得生成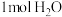 时放出的热量为54.8
时放出的热量为54.8 。其结果与理论数据有偏差,产生此偏差的原因可能是
。其结果与理论数据有偏差,产生此偏差的原因可能是A. 实验装置保温、隔热效果差
B. 用温度计测定
 溶液起始温度后直接测定
溶液起始温度后直接测定 溶液的温度
溶液的温度C. 一次性把
 溶液倒入盛有硫酸的小烧杯中
溶液倒入盛有硫酸的小烧杯中(2)实验中若改用
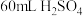
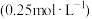 溶液与
溶液与 溶液进行反应,与上述实验相比,通过计算可得生成
溶液进行反应,与上述实验相比,通过计算可得生成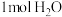 时所放出的热量
时所放出的热量 醋酸代替
醋酸代替 溶液进行上述实验,测得反应前后温度的变化值会
溶液进行上述实验,测得反应前后温度的变化值会(II)铅蓄电池是化学电源,它工作时的电池反应为:PbO2+Pb+2H2SO4=2PbSO4+2H2O。试回答:
(3)铅蓄电池正极的电极材料是
(4)工作时该铅蓄电池负极的电极反应是
(5)铅蓄电池工作时,电解质溶液的浓度
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐3】铅蓄电池是化学电源,其电极材料分别是Pb和PbO2,电解质溶液为稀硫酸,工作(放电)时该电池的总反应为Pb+PbO2+2H2SO4 2PbSO4+2H2O。试根据上述信息判断:
2PbSO4+2H2O。试根据上述信息判断:
(1)铅蓄电池充电时和电源负极相连的材料是_____ 。
(2)工作时,正极反应为_____ 。
(3)工作时,电解质溶液的pH_____ (填“增大”“减小”或“不变”)。
(4)工作时,电解质溶液中阴离子移向_____ 极。
(5)电流从_____ (填化学式,下同)极流向_____ 极。
 2PbSO4+2H2O。试根据上述信息判断:
2PbSO4+2H2O。试根据上述信息判断:(1)铅蓄电池充电时和电源负极相连的材料是
(2)工作时,正极反应为
(3)工作时,电解质溶液的pH
(4)工作时,电解质溶液中阴离子移向
(5)电流从
您最近一年使用:0次



