题型:解答题-结构与性质
难度:0.85
引用次数:136
题号:10416840
⑴已知在周期表的某一周期,其零族元素的价层电子排布式为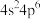 ,同周期的A、B两种元素,最外层电子数为2、7,次外层电子数为8、18,则元素A为
,同周期的A、B两种元素,最外层电子数为2、7,次外层电子数为8、18,则元素A为________ ,B为________ (写元素符号)。若周期表有第8周期,则其最终的零族元素的原子序数为____________ 。
⑵稀有气体的化合物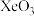 分子的空间构型是
分子的空间构型是__________ ,写出与其互为等电子体的一种阴离子的化学式___________ 。
⑶硼酸能形成类似于石墨的层状结构,单层的结构如图所示
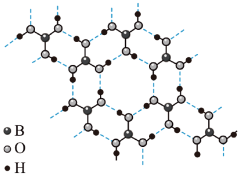
则硼酸晶体中存在的作用力除共价键外,还有_____________ 。
⑷稀土资源是重要的战略资源,下图为某稀土元素A的氧化物晶体的立方晶胞结构示意图,其中氧离子占据顶点、面心、棱心、体心的位置,A离子占据半数的立方体空隙

写出A氧化物的化学式______ ,A离子的配位数为______ 。已知晶胞参数为 ,则
,则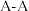 间距为
间距为________ 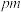 ,设A的摩尔质量为
,设A的摩尔质量为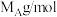 ,晶体的密度为
,晶体的密度为_______  。
。
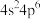 ,同周期的A、B两种元素,最外层电子数为2、7,次外层电子数为8、18,则元素A为
,同周期的A、B两种元素,最外层电子数为2、7,次外层电子数为8、18,则元素A为⑵稀有气体的化合物
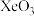 分子的空间构型是
分子的空间构型是⑶硼酸能形成类似于石墨的层状结构,单层的结构如图所示

则硼酸晶体中存在的作用力除共价键外,还有
⑷稀土资源是重要的战略资源,下图为某稀土元素A的氧化物晶体的立方晶胞结构示意图,其中氧离子占据顶点、面心、棱心、体心的位置,A离子占据半数的立方体空隙

写出A氧化物的化学式
 ,则
,则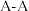 间距为
间距为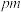 ,设A的摩尔质量为
,设A的摩尔质量为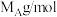 ,晶体的密度为
,晶体的密度为 。
。
更新时间:2020/06/18 10:46:50
|
相似题推荐
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐1】锌在工业中有重要作用,也是人体必需的微量元素。请完成下列空白:
(1)Zn的核外电子排布式为___________ 。
(2)《中华本草》等中医典籍中,记载了炉甘石( )入药,可用于治疗皮肤炎症或表面创伤。
)入药,可用于治疗皮肤炎症或表面创伤。 中阴离子空间结构为
中阴离子空间结构为___________ ,C的杂化方式为___________ 。
(1)Zn的核外电子排布式为
(2)《中华本草》等中医典籍中,记载了炉甘石(
 )入药,可用于治疗皮肤炎症或表面创伤。
)入药,可用于治疗皮肤炎症或表面创伤。 中阴离子空间结构为
中阴离子空间结构为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐2】用价层电子对互斥理论(VSEPR)判断下列分子或离子的空间构型
| 分子或离子 | PbCl2 | XeF4 | SnCl | PF3Cl2 | HgCl | ClO |
| 空间构型 |
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】(1)臭氧(O3)在 催化下能将烟气中的
催化下能将烟气中的 、
、 分别氧化为
分别氧化为 和
和 ,
, 也可在其他条件下被还原为
也可在其他条件下被还原为 。
。 中心原子轨道的杂化类型为
中心原子轨道的杂化类型为______ ; 的空间结构为
的空间结构为______ (用文字描述)。
(2)钒(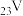 )是我国的丰产元素,广泛用于催化及钢铁工业。
)是我国的丰产元素,广泛用于催化及钢铁工业。
① 常用作
常用作 转化为
转化为 的催化剂。
的催化剂。 分子中S原子价电子对数是
分子中S原子价电子对数是______ ,分子的空间结构为______ ; 气态为单分子,该分子中S原子的杂化轨道类型为
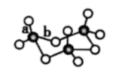
气态为单分子,该分子中S原子的杂化轨道类型为______ ; 的三聚体环状结构如图所示,该结构中S原子的杂化轨道类型为
的三聚体环状结构如图所示,该结构中S原子的杂化轨道类型为___ ;该结构中 键长有两类,一类键长约为
键长有两类,一类键长约为 ,另一类键长约为
,另一类键长约为 ,较短的键为
,较短的键为______ (填图中字母),该分子中含有______ 个σ键。
② 溶解在
溶解在 溶液中,可得到钒酸钠(
溶液中,可得到钒酸钠(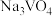 ),该盐阴离子的空间结构为
),该盐阴离子的空间结构为______ 。
 催化下能将烟气中的
催化下能将烟气中的 、
、 分别氧化为
分别氧化为 和
和 ,
, 也可在其他条件下被还原为
也可在其他条件下被还原为 。
。 中心原子轨道的杂化类型为
中心原子轨道的杂化类型为 的空间结构为
的空间结构为(2)钒(
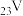 )是我国的丰产元素,广泛用于催化及钢铁工业。
)是我国的丰产元素,广泛用于催化及钢铁工业。①
 常用作
常用作 转化为
转化为 的催化剂。
的催化剂。 分子中S原子价电子对数是
分子中S原子价电子对数是 气态为单分子,该分子中S原子的杂化轨道类型为
气态为单分子,该分子中S原子的杂化轨道类型为 的三聚体环状结构如图所示,该结构中S原子的杂化轨道类型为
的三聚体环状结构如图所示,该结构中S原子的杂化轨道类型为 键长有两类,一类键长约为
键长有两类,一类键长约为 ,另一类键长约为
,另一类键长约为 ,较短的键为
,较短的键为
②
 溶解在
溶解在 溶液中,可得到钒酸钠(
溶液中,可得到钒酸钠(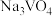 ),该盐阴离子的空间结构为
),该盐阴离子的空间结构为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐1】化合物Ⅲ也是一种汞解毒剂。化合物Ⅳ是一种强酸。下列说法正确的有_______ 。
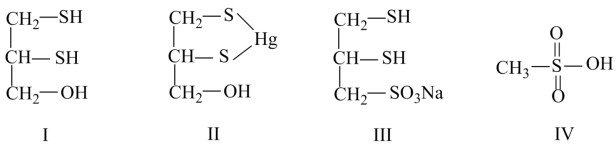
A.在I中S原子采取sp3杂化
B.在Ⅱ中S元素的电负性最大
C.在Ⅲ中C-C-C键角是180°
D.在Ⅲ中存在离子键与共价键
E. 在Ⅳ中硫氧键的键能均相等

A.在I中S原子采取sp3杂化
B.在Ⅱ中S元素的电负性最大
C.在Ⅲ中C-C-C键角是180°
D.在Ⅲ中存在离子键与共价键
E. 在Ⅳ中硫氧键的键能均相等
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
【推荐2】LiFePO4、LiPF6、LiAsF6、LiCl等常用于锂离子聚合物电池。请回答:
(1) 的立体构型是
的立体构型是___________ 。
(2)第四周期元素中,与基态As原子核外未成对电子数目相同的元素符号为___________ 。
(3)抗坏血酸(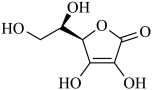 )常被用作碳包覆的碳源,以增强电极导电性,其易溶于水的原因是
)常被用作碳包覆的碳源,以增强电极导电性,其易溶于水的原因是___________ 。
(4)电池工作时,Li⁺沿聚乙二醇分子中的碳氧链迁移的过程如图甲所示(图中阴离子未画出),电解质LiPF6或LiAsF6的阴离子结构如图乙所示(X=P、As)。
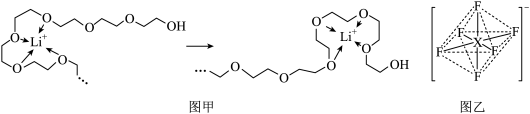
①从化学键角度看,Li⁺迁移过程发生___________ (填“物理”或“化学”)变化。
②已知相同条件下,锂离子的迁移速率与离子键的强弱有关,则Li⁺在___________ (选填“LiPF6”或“LiAsF6”)中迁移较快。
③图乙中X的杂化方式最可能是___________ (填字母编号)。
a.sp3 b.sp3d c.sp3d2 d.sp3d3
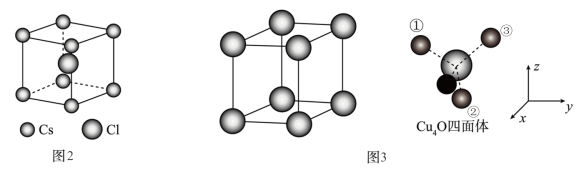
(5)Cu2O晶体结构与CsCl(图2)相似,只是利用Cu4O占据CsCl晶体中Cl的位置,而Cs位置由O原子占据,如图3所示,每个Cu2O晶胞中有___________ 个“Cu2O”;Cu2O晶胞中Cu的配位数是___________ ;若①处Cu原子坐标为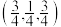 ,②处Cu原子坐标为
,②处Cu原子坐标为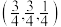 ,则③处Cu原子坐标为(___________,
,则③处Cu原子坐标为(___________,___________ ,)。
(1)
 的立体构型是
的立体构型是(2)第四周期元素中,与基态As原子核外未成对电子数目相同的元素符号为
(3)抗坏血酸(
 )常被用作碳包覆的碳源,以增强电极导电性,其易溶于水的原因是
)常被用作碳包覆的碳源,以增强电极导电性,其易溶于水的原因是(4)电池工作时,Li⁺沿聚乙二醇分子中的碳氧链迁移的过程如图甲所示(图中阴离子未画出),电解质LiPF6或LiAsF6的阴离子结构如图乙所示(X=P、As)。

①从化学键角度看,Li⁺迁移过程发生
②已知相同条件下,锂离子的迁移速率与离子键的强弱有关,则Li⁺在
③图乙中X的杂化方式最可能是
a.sp3 b.sp3d c.sp3d2 d.sp3d3
(5)Cu2O晶体结构与CsCl(图2)相似,只是利用Cu4O占据CsCl晶体中Cl的位置,而Cs位置由O原子占据,如图3所示,每个Cu2O晶胞中有
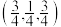 ,②处Cu原子坐标为
,②处Cu原子坐标为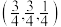 ,则③处Cu原子坐标为(___________,
,则③处Cu原子坐标为(___________,
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
【推荐3】电气石是一种具有保健作用的天然石材,其中含有的主要元素为 等元素。
等元素。
(1)上述元素中,原子半径最小的是_______ (用元素符号表示),与硫同周期的元素中简单离子半径最小的是_______ (用离子符号表示);
(2)用轨道表示式表示氧元素原子核外电子的运动状态_______ ;氧元素原子核外有_______ 种不同能量的电子;
(3) 分子中
分子中 为
为_______ 杂化,键角等于_______ ,可以判断出 分子为
分子为_______ 分子(选填“极性”或“非极性”); 晶体的熔点比
晶体的熔点比 晶体
晶体_______ (选填“高”、“低”),原因为_______ 。
 等元素。
等元素。(1)上述元素中,原子半径最小的是
(2)用轨道表示式表示氧元素原子核外电子的运动状态
(3)
 分子中
分子中 为
为 分子为
分子为 晶体的熔点比
晶体的熔点比 晶体
晶体
您最近一年使用:0次
【推荐1】铁及其化合物是日常生活生产中应用广泛的材料,钛铁合金具有吸氢特性,在制造以氢为能源的热泵和蓄电池等方面有广阔的应用前景。请回答下列问题:
(1)基态铁原子的价层电子的轨道表示式(电子排布图)为__ 。
(2)铁元素常见的离子有Fe2+和Fe3+两种,稳定性:Fe2+__ Fe3+ (填“强于”或“弱于”),原因是__ 。
(3)氮化钛熔点高,硬度大,具有典型的NaCl型晶体结构,其晶胞结构如图所示。
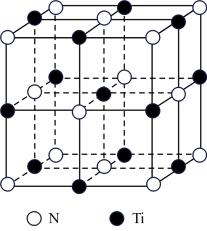
①设氮化钛晶体中Ti原子与跟它最邻近的N原子之间的距离为r,则晶胞内与该Ti原子最邻近的Ti原子的数目为__ ;Ti原子与跟它次邻近的N原子之间的距离为___ 。
②碳氮化钛化合物在汽车制造和航天航空领域有广泛的应用,其结构是用碳原子代替氮化钛晶胞顶点的氮原子,则这种碳氮化钛化合物的化学式为__ 。
(1)基态铁原子的价层电子的轨道表示式(电子排布图)为
(2)铁元素常见的离子有Fe2+和Fe3+两种,稳定性:Fe2+
(3)氮化钛熔点高,硬度大,具有典型的NaCl型晶体结构,其晶胞结构如图所示。

①设氮化钛晶体中Ti原子与跟它最邻近的N原子之间的距离为r,则晶胞内与该Ti原子最邻近的Ti原子的数目为
②碳氮化钛化合物在汽车制造和航天航空领域有广泛的应用,其结构是用碳原子代替氮化钛晶胞顶点的氮原子,则这种碳氮化钛化合物的化学式为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】过渡金属元素铬 是不锈钢的重要成分,在工农业生产和国防建设中有着广泛应用。回答下列问题:在金属材料中添加
是不锈钢的重要成分,在工农业生产和国防建设中有着广泛应用。回答下列问题:在金属材料中添加 颗粒,可以增强材料的耐腐蚀性、硬度和机械性能。
颗粒,可以增强材料的耐腐蚀性、硬度和机械性能。 具有体心四方结构,如图所示,处于顶角位置的是
具有体心四方结构,如图所示,处于顶角位置的是_______ 原子。设Cr和Al原子半径分别为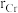 和
和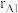 ,则金属原子空间占有率为
,则金属原子空间占有率为_______ %(列出计算表达式)。

 是不锈钢的重要成分,在工农业生产和国防建设中有着广泛应用。回答下列问题:在金属材料中添加
是不锈钢的重要成分,在工农业生产和国防建设中有着广泛应用。回答下列问题:在金属材料中添加 颗粒,可以增强材料的耐腐蚀性、硬度和机械性能。
颗粒,可以增强材料的耐腐蚀性、硬度和机械性能。 具有体心四方结构,如图所示,处于顶角位置的是
具有体心四方结构,如图所示,处于顶角位置的是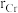 和
和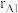 ,则金属原子空间占有率为
,则金属原子空间占有率为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】填空。
(1)X、Y、Z、R代表四种短周期元素,X元素的基态原子电子排布式为1s1,Y元素的原子价电子排布为nsnnpn,Z元素位于第二周期且原子中p能级与所有s能级电子总数相等,R原子M电子层的p能级中有3个未成对电子。
①Z的基态原子的价电子排布式为_______ ;化合物X2Z分子的空间构型为_______ 形。
②Y2X2分子中,中心原子采用_______ 杂化,分子中σ键和π键个数之比为_______ ;按价层电子对互斥理论,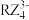 离子的VSEPR模型和立体构型均为
离子的VSEPR模型和立体构型均为_______ 形。
(2)金属氢化物是具有良好发展前景的储氢材料。
①LiH中,离子半径:Li+_______ H-(填“<”“>”或“=”)
②某储氢材料是短周期金属元素M的氢化物。M的部分电离能如下表所示,M的最高正价是_______ 。
③NaH具有NaCl型晶体结构,Na+的配位数为_______ ,Na+的堆积方式为_______ ,已知NaH晶体的晶胞参数;a=488pm,Na+半径为102pm,H-的半径为_______ cm。
(1)X、Y、Z、R代表四种短周期元素,X元素的基态原子电子排布式为1s1,Y元素的原子价电子排布为nsnnpn,Z元素位于第二周期且原子中p能级与所有s能级电子总数相等,R原子M电子层的p能级中有3个未成对电子。
①Z的基态原子的价电子排布式为
②Y2X2分子中,中心原子采用
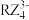 离子的VSEPR模型和立体构型均为
离子的VSEPR模型和立体构型均为(2)金属氢化物是具有良好发展前景的储氢材料。
①LiH中,离子半径:Li+
②某储氢材料是短周期金属元素M的氢化物。M的部分电离能如下表所示,M的最高正价是
| I₁/kJ·mol-1 | I₂/kJ·mol-1 | I₃/kJ·mol-1 | I₄/kJ·mol-1 | Is/kJ·mol-1 |
| 738 | 1451 | 7733 | 10540 | 13630 |
③NaH具有NaCl型晶体结构,Na+的配位数为
您最近一年使用:0次



