下图中的实线表示元素周期表的边界。①~⑧分别表示元素周期表中对应位置的元素。
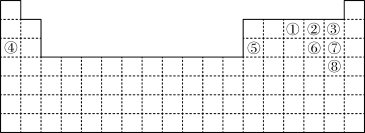
(1)元素周期表体现了元素周期律。元素周期律的本质是________ 。在元素周期表中,元素的位置与结构的关系是______ 。
(2)在上表中画出金属区和非金属区的分界线_______
(3)上述元素所能形成的简单离子中半径最小的是________ (填离子符号),最高价氧化物对应水化物酸性最强的是________ (填分子式)。
(4)④与⑥形成的化合物溶于水后,溶液的pH________ 7。原因________________ (用离子方程式表示),若使其熔化,需破坏的作用力有________________ 。
(5)元素①的氢化物电子式为________________ ,该分子属于________ 晶体。
(6)⑥⑦两元素非金属性较强的是(写元素符号)________ 。写出能证明这一结论的一个实验事实____ 。
(7)⑤、⑦各自的最高价氧化物对应的水化物可以反应生成盐和水,该反应的离子方程式为____ 。
(8)⑦的氢化物的还原性比元素⑥的氢化物的还原性________ (填“强”或“弱”)。

(1)元素周期表体现了元素周期律。元素周期律的本质是
(2)在上表中画出金属区和非金属区的分界线
(3)上述元素所能形成的简单离子中半径最小的是
(4)④与⑥形成的化合物溶于水后,溶液的pH
(5)元素①的氢化物电子式为
(6)⑥⑦两元素非金属性较强的是(写元素符号)
(7)⑤、⑦各自的最高价氧化物对应的水化物可以反应生成盐和水,该反应的离子方程式为
(8)⑦的氢化物的还原性比元素⑥的氢化物的还原性
更新时间:2019/11/07 16:08:57
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】原子序数依次增大的短周期主族元素X、Y、Z、W、R,其中X、Y两种元素的核电荷数之差等于它们的原子最外层电子数之和;Y、Z位于相邻主族;Z是地壳中含量最高的元素;X、W是同主族元素。上述五种元素两两间能形成四种常见的化合物甲、乙、丙、丁,这四种化合物中原子个数比如下表:
(1)写出下列元素符号:Y_____________ ,Z_______________ ,W_____________ ,R________________ 。
(2)写出下列化合物的电子式:乙_______________ ,丙__________________ 。
(3)向甲的水溶液中加入丁,有淡黄色沉淀生成,请写出反应的化学方程式:__________________ 。
(4)甲和乙反应能放出大量的热,同时生成两种无污染的物质,请写出该反应的化学方程式:______________________________ 。
| 甲 | 乙 | 丙 | 丁 | |
| 化合物中各元素原子个数比 | 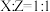 | 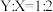 |  | 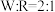 |
(2)写出下列化合物的电子式:乙
(3)向甲的水溶液中加入丁,有淡黄色沉淀生成,请写出反应的化学方程式:
(4)甲和乙反应能放出大量的热,同时生成两种无污染的物质,请写出该反应的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】硫化氢的转化是资源利用和环境保护的重要研究课题。将 和空气的混合气体通入
和空气的混合气体通入 、
、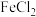 、
、 的混合酸性溶液中反应回收S,其物质转化如图所示。
的混合酸性溶液中反应回收S,其物质转化如图所示。
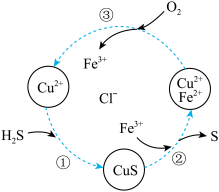
(1)用合适的化学用语表示硫化氢溶于水显弱酸性的原因:_______ ,过程① 吸收
吸收 生成
生成 沉淀,溶液的酸性
沉淀,溶液的酸性_______ (选填“增强”或“减弱”或“不变”)。
(2)在图示过程②中:被氧化的元素是:_______ ;在图示过程③中: 转化为
转化为 ,写出反应的离子方程式:
,写出反应的离子方程式:_______ ;
(3)某兴趣小组为探究 和
和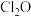 的性质,将两种气体同时通入水中,实验装置如图:
的性质,将两种气体同时通入水中,实验装置如图:
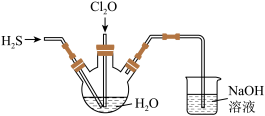
①三颈瓶中出现淡黄色沉淀,溶液呈强酸性。写出反应的化学方程式:_______ ;
②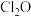 易溶于水并生成次氯酸。设计实验方案检验通入水中的
易溶于水并生成次氯酸。设计实验方案检验通入水中的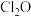 是否已过量:
是否已过量:_______ ;
③写出 溶液吸收足量
溶液吸收足量 气体的化学方程式:
气体的化学方程式:_______ 。
(4)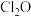 分子中每个原子都达到8电子稳定结构,它的电子式为
分子中每个原子都达到8电子稳定结构,它的电子式为_______ 。
 和空气的混合气体通入
和空气的混合气体通入 、
、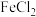 、
、 的混合酸性溶液中反应回收S,其物质转化如图所示。
的混合酸性溶液中反应回收S,其物质转化如图所示。
(1)用合适的化学用语表示硫化氢溶于水显弱酸性的原因:
 吸收
吸收 生成
生成 沉淀,溶液的酸性
沉淀,溶液的酸性(2)在图示过程②中:被氧化的元素是:
 转化为
转化为 ,写出反应的离子方程式:
,写出反应的离子方程式:(3)某兴趣小组为探究
 和
和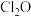 的性质,将两种气体同时通入水中,实验装置如图:
的性质,将两种气体同时通入水中,实验装置如图:
①三颈瓶中出现淡黄色沉淀,溶液呈强酸性。写出反应的化学方程式:
②
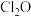 易溶于水并生成次氯酸。设计实验方案检验通入水中的
易溶于水并生成次氯酸。设计实验方案检验通入水中的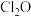 是否已过量:
是否已过量:③写出
 溶液吸收足量
溶液吸收足量 气体的化学方程式:
气体的化学方程式:(4)
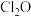 分子中每个原子都达到8电子稳定结构,它的电子式为
分子中每个原子都达到8电子稳定结构,它的电子式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】A、B、C、D四种元素均为短周期元素,A的最外层电子数为B最外层电子数的2倍,C的最高正价与最低负价的绝对值之差为2,A、B两元素形成的物质具有两性,C的最高价氧化物对应的水化物是强酸,D的最高价氧化物对应的水化物的碱性是短周期中碱性最强的,则:
(1)A的气态氢化物的电子式为_______________ B离子的离子结构示意图为_____________
(2)D的最高价氧化物对应的水化物的化学式为__________ ,含有____________ 键和_____
键。
(3)C单质的结构式___________ 。
(1)A的气态氢化物的电子式为
(2)D的最高价氧化物对应的水化物的化学式为
键。
(3)C单质的结构式
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐1】废旧锌锰电池中的黑锰粉含有MnO2、MnO(OH)、NH4Cl和少量ZnCl2、Fe2O3及炭黑等,为了保护环境、充分利用锰资源,通过如下流程制备MnSO4。

回答下列问题:
(1)Mn的原子结构示意图为___________ 。
(2)“滤液a”的主要成分为NH4Cl,另外还含有少量ZnCl2等。
①用离子方程式表示“滤液a”呈酸性的原因___________ 。
②根据下图所示的溶解度曲线,将“滤液a”蒸发结晶、___________ 、洗涤、干燥,得NH4Cl固体。

(3)“焙炒”的目的是除炭、氧化MnO(OH)等。空气中O2氧化MnO(OH)的化学方程式为___________ 。
(4)探究“酸浸”中MnO2溶解的适宜操作。
实验I.向MnO2中加入H2O2溶液,产生大量气泡;再加入稀H2SO4,固体未明显溶解。
实验II.向MnO2中加入稀H2SO4,固体未溶解;再加入H2O2溶液,产生大量气泡,固体完全溶解。
①实验I中MnO2的作用是___________ ,实验II中H2O2的作用是___________ 。
②由实验可知,“酸浸”溶解MnO2时加入试剂的顺序是___________ 。
(5)加入MnO调pH时,证明MnSO4溶液中Fe3+沉淀完全的实验步骤及现象:取少量溶液,滴加___________ (填试剂),观察到___________ (填现象)。

回答下列问题:
(1)Mn的原子结构示意图为
(2)“滤液a”的主要成分为NH4Cl,另外还含有少量ZnCl2等。
①用离子方程式表示“滤液a”呈酸性的原因
②根据下图所示的溶解度曲线,将“滤液a”蒸发结晶、

(3)“焙炒”的目的是除炭、氧化MnO(OH)等。空气中O2氧化MnO(OH)的化学方程式为
(4)探究“酸浸”中MnO2溶解的适宜操作。
实验I.向MnO2中加入H2O2溶液,产生大量气泡;再加入稀H2SO4,固体未明显溶解。
实验II.向MnO2中加入稀H2SO4,固体未溶解;再加入H2O2溶液,产生大量气泡,固体完全溶解。
①实验I中MnO2的作用是
②由实验可知,“酸浸”溶解MnO2时加入试剂的顺序是
(5)加入MnO调pH时,证明MnSO4溶液中Fe3+沉淀完全的实验步骤及现象:取少量溶液,滴加
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
【推荐2】锑白( ,性质类似
,性质类似 )可用作白色颜料和阻燃剂。一种从含锑工业废渣(主要成分是
)可用作白色颜料和阻燃剂。一种从含锑工业废渣(主要成分是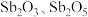 ,含有CuO、
,含有CuO、 和
和 等杂质)中制取
等杂质)中制取 的工业流程如下图所示:
的工业流程如下图所示:
(1)锑元素原子序数为51,基态锑原子的价电子轨道表示式为___________ 。
(2)“还原”加入过量铁粉的目的是___________ (填序号)。
a.将 转化为
转化为 b.将
b.将 转化为
转化为 c.将铜离子转化为铜单质
c.将铜离子转化为铜单质
(3)“滤饼”的成分是SbOCl,“稀释水解”主要反应的离子方程式为___________ ;该操作中需要搅拌的原因是___________ 。
(4)“酸洗”后检验沉淀是否洗净的试剂是___________ (填名称)。
(5)“中和”时生成 的化学方程式为
的化学方程式为___________ ,“中和”时不宜将氨水换成氢氧化钠溶液,原因是___________ 。
(6)我国锑的蕴藏量占世界第一位,而锑的化合物也用途广泛。
氟锑酸化学式为 ,酸性比纯硫酸强
,酸性比纯硫酸强 倍,称为超强酸,其与HF作用生成
倍,称为超强酸,其与HF作用生成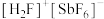 ,则其阳离子的空间结构为
,则其阳离子的空间结构为___________ ,阴离子中心原子的杂化方式合理的是___________ 。
a. b.
b. c.
c. d.
d.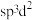
 ,性质类似
,性质类似 )可用作白色颜料和阻燃剂。一种从含锑工业废渣(主要成分是
)可用作白色颜料和阻燃剂。一种从含锑工业废渣(主要成分是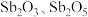 ,含有CuO、
,含有CuO、 和
和 等杂质)中制取
等杂质)中制取 的工业流程如下图所示:
的工业流程如下图所示: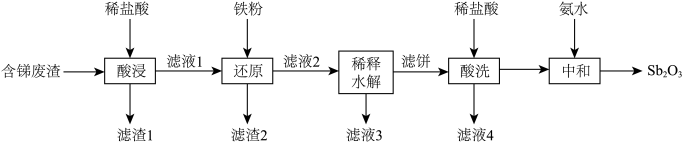
(1)锑元素原子序数为51,基态锑原子的价电子轨道表示式为
(2)“还原”加入过量铁粉的目的是
a.将
 转化为
转化为 b.将
b.将 转化为
转化为 c.将铜离子转化为铜单质
c.将铜离子转化为铜单质(3)“滤饼”的成分是SbOCl,“稀释水解”主要反应的离子方程式为
(4)“酸洗”后检验沉淀是否洗净的试剂是
(5)“中和”时生成
 的化学方程式为
的化学方程式为(6)我国锑的蕴藏量占世界第一位,而锑的化合物也用途广泛。
氟锑酸化学式为
 ,酸性比纯硫酸强
,酸性比纯硫酸强 倍,称为超强酸,其与HF作用生成
倍,称为超强酸,其与HF作用生成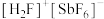 ,则其阳离子的空间结构为
,则其阳离子的空间结构为a.
 b.
b. c.
c. d.
d.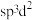
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】A、B、C、D、E是中学常见的五种化合物,它们之间有下列转化关系:
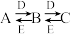
已知A溶液显碱性,焰色反应为黄色,且可促进水的电离。
(1)若A、B、C中含有相同的金属元素,且B为白色沉淀物,则A的化学式为____ ,D的化学式为_____ ;A、C反应生成B的离子方程式为___________ 。
(2)若C是一种无色无味的气体,用离子方程式表示A溶液显碱性的原因___________ ,C与E反应生成B的化学方程式为________ 。
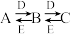
已知A溶液显碱性,焰色反应为黄色,且可促进水的电离。
(1)若A、B、C中含有相同的金属元素,且B为白色沉淀物,则A的化学式为
(2)若C是一种无色无味的气体,用离子方程式表示A溶液显碱性的原因
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐1】如表是元素周期表主族元素的一部分,短周期元素X的最高正价是+5价,Y单质可在空气中燃烧。
(1)Z的元素符号是________ ,原子结构示意图是_________ 。
(2)W的最高价氧化物不溶于水,但能溶于烧碱溶液,反应的化学方程式为_________ 。
(3)探寻同一族元素性质的一些共同规律,是学习化学的重要方法之一。在下表中列出对H2ZO3各种不同化学性质的推测,举例并写出相应的化学方程式。
| W | X | Y |
| Z |
(1)Z的元素符号是
(2)W的最高价氧化物不溶于水,但能溶于烧碱溶液,反应的化学方程式为
(3)探寻同一族元素性质的一些共同规律,是学习化学的重要方法之一。在下表中列出对H2ZO3各种不同化学性质的推测,举例并写出相应的化学方程式。
| 编号 | 性质推测 | 化学方程式 |
| 示例 | 氧化性 | H2ZO3+4HI=Z↓+2I2+3H2O |
| 1 | ||
| 2 |
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】如图为元素周期表的一部分,请参照元素①~②在图中的位置,回答下列问题。
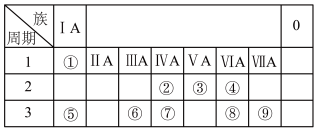
(1)第三周期元素中非金属性最强的元素的原子结构示意图是______ 。
(2)②③⑦最高价氧化物对应水化物的酸性由强到弱的顺序是______ (填化学式)。
(3)下列可以判断⑤和⑥金属性强弱的是______ (填序号)。
a.单质的熔点:⑤<⑥
b.化合价:⑤<⑥
c.单质与水反应的剧烈程度:⑤>⑥
d.最高价氧化物对应水化物的碱性:⑤>⑥
(4)为验证第Ⅵ 族部分元素非金属性的递变规律,设计如图装置进行实验,请回答:
族部分元素非金属性的递变规律,设计如图装置进行实验,请回答:
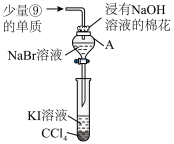
①仪器 的名称是
的名称是______ , 中发生反应的离子方程式是
中发生反应的离子方程式是__________________ 。
②棉花中浸有 溶液的作用是
溶液的作用是__________________ (用离子方程式表示)。
③验证溴与碘的非金属性强弱:通入少量⑨的单质,充分反应后,将 中液体滴入试管内,取下试管,充分振荡、静置,可观察到
中液体滴入试管内,取下试管,充分振荡、静置,可观察到______ 。该实验必须控制②单质的加入量,否则得不出溴的非金属性比碘强的结论,理由是__________________ 。
④第Ⅵ 族元素非金属性随元素核电荷数的增加而逐渐减弱的原因:同主族元素从上到下原子半径逐渐
族元素非金属性随元素核电荷数的增加而逐渐减弱的原因:同主族元素从上到下原子半径逐渐______ (填“增大”或“减小”),得电子能力逐渐减弱。

(1)第三周期元素中非金属性最强的元素的原子结构示意图是
(2)②③⑦最高价氧化物对应水化物的酸性由强到弱的顺序是
(3)下列可以判断⑤和⑥金属性强弱的是
a.单质的熔点:⑤<⑥
b.化合价:⑤<⑥
c.单质与水反应的剧烈程度:⑤>⑥
d.最高价氧化物对应水化物的碱性:⑤>⑥
(4)为验证第Ⅵ
 族部分元素非金属性的递变规律,设计如图装置进行实验,请回答:
族部分元素非金属性的递变规律,设计如图装置进行实验,请回答:
①仪器
 的名称是
的名称是 中发生反应的离子方程式是
中发生反应的离子方程式是②棉花中浸有
 溶液的作用是
溶液的作用是③验证溴与碘的非金属性强弱:通入少量⑨的单质,充分反应后,将
 中液体滴入试管内,取下试管,充分振荡、静置,可观察到
中液体滴入试管内,取下试管,充分振荡、静置,可观察到④第Ⅵ
 族元素非金属性随元素核电荷数的增加而逐渐减弱的原因:同主族元素从上到下原子半径逐渐
族元素非金属性随元素核电荷数的增加而逐渐减弱的原因:同主族元素从上到下原子半径逐渐
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】现有表格中短周期元素的数据(已知 的原子半径为0.089nm):
的原子半径为0.089nm):
1.⑧号元素在元素周期表中的位置是。_______ 。
2.①④⑦元素的简单气态氢化物中,热稳性定由高到低排序_______ (写化学式)。
3.结合原子结构解释③⑥元素的最高价氧化物对应的水化物的碱性强弱_______ 。
 的原子半径为0.089nm):
的原子半径为0.089nm):① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
原子半径(nm) | 0.074 | 0.160 | 0.152 | 0.110 | 0.099 | 0.186 | 0.075 | 0.082 |
最高正价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
最低负价 | -2 | -3 | -1 | -3 |
2.①④⑦元素的简单气态氢化物中,热稳性定由高到低排序
3.结合原子结构解释③⑥元素的最高价氧化物对应的水化物的碱性强弱
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】短周期元素A、B、C、D、E、F的原子序数依次增大。其中A与D、C与E分别是同主族元素;B与C同周期;B原子最外层电子数为其电子层数的2倍;A、B两元素的核电荷数之差等于它们的原子最外层电子数之和;F元素是同周期元素中原子半径最小的主族元素。化合物甲、乙、丙、丁、戊、己的组成如表所示:
回答下列问题:
(1)以上六种化合物中属于离子化合物有____ 种,化合物丙的电子式为____ ,化合物丁晶体内存在的化学键类型是____ 。
(2)甲与戊分子的热稳定性大小顺序为____ (用化学式表示)。
(3)向含有0.2mol乙的水溶液中加入少量MnO2粉末,使乙完全反应,则该反应中转移的电子总数为____ 。
| 化合物 | 甲 | 乙 | 丙 | 丁 | 戊 | 己 |
| 化学式 | A2C | A2C2 | B2A2 | D2C2 | A2E | DF |
回答下列问题:
(1)以上六种化合物中属于离子化合物有
(2)甲与戊分子的热稳定性大小顺序为
(3)向含有0.2mol乙的水溶液中加入少量MnO2粉末,使乙完全反应,则该反应中转移的电子总数为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
【推荐2】随着原子序数的递增,A~G七种短周期元素的最高正价或最低负价与原子序数的关系如图所示。

(1)在A、B、F、G四种元素中,非金属性最弱的元素在周期表中的位置为_______ 。
(2)A、B、F三种元素的原子半径由大到小的顺序是_______ (填元素符号)。
(3)E元素的最高价氧化物与氢氧化钠溶液反应的离子方程式是_______ 。
(4)元素A与C形成的电子总数为22的分子的结构式为_______ 。
(5)元素C与D按原子个数比1∶1形成的化合物的电子式为_______ ,其所含的化学键有_______ (填化学键类型)。
(6)C的简单氢化物在通常状况下,加热到100℃时由液态变为气态,加热到2000℃时发生分解反应,请从物质的构成微粒及相互作用的角度解释这两种变化过程中所需温度差异的原因_______ 。

(1)在A、B、F、G四种元素中,非金属性最弱的元素在周期表中的位置为
(2)A、B、F三种元素的原子半径由大到小的顺序是
(3)E元素的最高价氧化物与氢氧化钠溶液反应的离子方程式是
(4)元素A与C形成的电子总数为22的分子的结构式为
(5)元素C与D按原子个数比1∶1形成的化合物的电子式为
(6)C的简单氢化物在通常状况下,加热到100℃时由液态变为气态,加热到2000℃时发生分解反应,请从物质的构成微粒及相互作用的角度解释这两种变化过程中所需温度差异的原因
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】几种主族元素(过渡元素略去)在周期表中的位置如图:

(1)A的元素符号是_____ 。
(2)D在周期表中的位置是____ 。
(3)E、G、T的原子半径由大到小的顺序是_____ (填元素符号)。
(4)硒元素(34Se)与D同主族,其非金属性比D_____ (填“强”或“弱”)。
(5)R元素的原子结构示意图为____ 。
(6)E、D两元素能形成原子个数比2:1和1:1的两种化合物。2:1型化合物的电子式为_____ 。1:1型化合物的化学式所含化学键类型____ 。

(1)A的元素符号是
(2)D在周期表中的位置是
(3)E、G、T的原子半径由大到小的顺序是
(4)硒元素(34Se)与D同主族,其非金属性比D
(5)R元素的原子结构示意图为
(6)E、D两元素能形成原子个数比2:1和1:1的两种化合物。2:1型化合物的电子式为
您最近一年使用:0次



