如图是元素周期表的一部分,根据元素在周期表中的位置,回答下列问题:
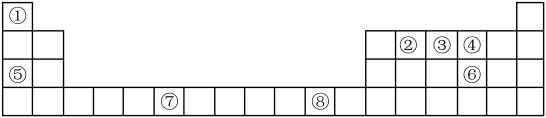
(1)⑧号元素在周期表中的位置是___________ ,其最高能层的电子占据的原子轨道电于云轮廓为___________ 形。
(2)④、⑤、⑥的简单离子的离子半径由小到大的顺序为___________ (用元素符号表示、下同)。
(3)元素①②③可形成原子个数比为1:1:1的共价化合物,分子中各原子最外层均达到8电子或2电子的稳定结构,试写出其电子式___________ ,该分子为___________ (填“极性分子”或“非极性分子”)。
(4)画出⑦的基态原子价层电子轨道表示式___________ 。
(5)④的简单氢化物比⑥的简单氢化物沸点更高,原因是___________ 。

(1)⑧号元素在周期表中的位置是
(2)④、⑤、⑥的简单离子的离子半径由小到大的顺序为
(3)元素①②③可形成原子个数比为1:1:1的共价化合物,分子中各原子最外层均达到8电子或2电子的稳定结构,试写出其电子式
(4)画出⑦的基态原子价层电子轨道表示式
(5)④的简单氢化物比⑥的简单氢化物沸点更高,原因是
更新时间:2024-02-04 18:18:10
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】如图是元素周期表的一部分,表中列出了八种元素的位置:
请回答下列问题:
(1)①元素的简单氢化物的电子式为______ 。
(2)在元素①-⑧中,金属性最强的元素是______ (填元素符号),最高价含氧酸酸性最强的是_____ (填化学式)。
(3)②、③、④三种元素的原子半径由大到小的顺序是_____ (填元素符号),③和⑦的简单氢化物的稳定性较强的是_____ (填化学式)。
(4)用电子式表示④和⑤所形成化合物的形成过程_________ 。
(5)⑤和⑥的最高价氧化物对应的水化物之间发生反应的离子方程式为_____ 。
| 族/周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
1 | ||||||||
2 | ① | ② | ③ | ④ | ||||
3 | ⑤ | ⑥ | ⑦ | ⑧ |
(1)①元素的简单氢化物的电子式为
(2)在元素①-⑧中,金属性最强的元素是
(3)②、③、④三种元素的原子半径由大到小的顺序是
(4)用电子式表示④和⑤所形成化合物的形成过程
(5)⑤和⑥的最高价氧化物对应的水化物之间发生反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐2】元素周期表是指导化学学习的重要工具。下图为元素周期表的一部分。请按要求填空:
(1)N元素形成的单质的电子式_________ ;N元素的气态氢化物含有化学键属于_______ (“离子键”或“共价键”)。
(2)Mg和Al中,金属性较强的是_______ (写元素符号),写出一条能说明该结论的事实(用文字描述)___________
(3)S和Cl中,非金属性较强的是___________ (写元素符号),不能说明该结论的事实是________ (填字母符号)。
a. 单质硫难溶于水,氯气能溶于水
b. 通入
通入 溶液中,溶液变浑浊
溶液中,溶液变浑浊
c. 受热时 易分解,HCl不易分解
易分解,HCl不易分解
d. 氯气与铁反应生成 ,硫与铁反应生成FeS
,硫与铁反应生成FeS
(4)O和S中,非金属性较强的是_________ (写元素符号),写出能说明该结论的化学方程式______________
| N | O | F | |||||
| Mg | Al | S | Cl | ||||
(2)Mg和Al中,金属性较强的是
(3)S和Cl中,非金属性较强的是
a. 单质硫难溶于水,氯气能溶于水
b.
 通入
通入 溶液中,溶液变浑浊
溶液中,溶液变浑浊c. 受热时
 易分解,HCl不易分解
易分解,HCl不易分解d. 氯气与铁反应生成
 ,硫与铁反应生成FeS
,硫与铁反应生成FeS(4)O和S中,非金属性较强的是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐3】如图是元素周期表的一部分,请回答下列问题:
(1)g元素在元素周期表中位置为_______ 。
(2)f、h的最高价氧化物对应水化物相互反应的离子方程式为_______ (用元素符号作答,下同)。
(3)用电子式表示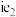 的形成过程
的形成过程_______ 。
(4)a、b、c、d形成的盐中含有的化学键类型为_______ 。
(5)用化学方程式说明d、g的简单氢化物的稳定性强弱的原因_____
| a | |||||||||||||||||
| b | c | d | e | ||||||||||||||
| f | g | ||||||||||||||||
| h | i | j | |||||||||||||||
(2)f、h的最高价氧化物对应水化物相互反应的离子方程式为
(3)用电子式表示
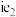 的形成过程
的形成过程(4)a、b、c、d形成的盐中含有的化学键类型为
(5)用化学方程式说明d、g的简单氢化物的稳定性强弱的原因
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐1】X、Y、Z、Q、E五种元素中,X原子核外的M层中只有两对成对电子,Y原子核外的L层电子数是K层的两倍,Z是地壳内含量最高的元素,Q的核电荷数是X与Z的核电荷数之和, E在元素周期表的各元素中电负性最大。请回答下列问题:
(1)X、Y的元素符号依次为___________ 、____________ ;
(2)XZ2与YZ2分子的立体结构分别是___________ 和___________ ,在水中溶解度较大的是________ (填化学式);
(3)Q元素的价电子排布图为___________ ,在形成化合物时它的最高化合价为_____ ;
(4)Z与E形成的化合物中,各原子最外层都达到8电子结构,该化合物中心原子采用的轨道杂化方式是____________ 。
(1)X、Y的元素符号依次为
(2)XZ2与YZ2分子的立体结构分别是
(3)Q元素的价电子排布图为
(4)Z与E形成的化合物中,各原子最外层都达到8电子结构,该化合物中心原子采用的轨道杂化方式是
您最近一年使用:0次
【推荐2】合成氨是人类科学技术发展史上的一项重大成就: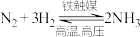 。目前合成氨工业中使用的催化剂铁触媒中主要成分为
。目前合成氨工业中使用的催化剂铁触媒中主要成分为 (
( 和
和 ),还含有少量的
),还含有少量的 、
、 、
、 、
、 、
、 等。回答问题:
等。回答问题:
(1)基态N原子中,电子占据最高能级的符号是_______ ,占据该能级电子的电子云轮廓图为_______ 形,核外存在_______ 对自旋相反的电子。
(2)26号元素 基态原子的价层电子轨道表示式是
基态原子的价层电子轨道表示式是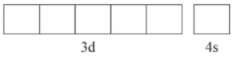
_______ 。
(3) 的价层电子排布式为
的价层电子排布式为_______ ,在元素周期表中位于_______ 区(填“s”“p”“d”或“ ”)。
”)。
(4) 分子中,与N原子相连的H显正电性。分析电负性大小关系为N
分子中,与N原子相连的H显正电性。分析电负性大小关系为N_______ H(填“>”“<”或“=”)。
(5) 的第一电离能
的第一电离能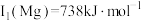 ,
, 的第一电离能
的第一电离能 ,结合基态原子价层电子排布式解释第一电离能镁元素高于铝元素的原因:
,结合基态原子价层电子排布式解释第一电离能镁元素高于铝元素的原因:_______ 。
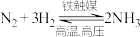 。目前合成氨工业中使用的催化剂铁触媒中主要成分为
。目前合成氨工业中使用的催化剂铁触媒中主要成分为 (
( 和
和 ),还含有少量的
),还含有少量的 、
、 、
、 、
、 、
、 等。回答问题:
等。回答问题:(1)基态N原子中,电子占据最高能级的符号是
(2)26号元素
 基态原子的价层电子轨道表示式是
基态原子的价层电子轨道表示式是
(3)
 的价层电子排布式为
的价层电子排布式为 ”)。
”)。(4)
 分子中,与N原子相连的H显正电性。分析电负性大小关系为N
分子中,与N原子相连的H显正电性。分析电负性大小关系为N(5)
 的第一电离能
的第一电离能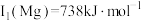 ,
, 的第一电离能
的第一电离能 ,结合基态原子价层电子排布式解释第一电离能镁元素高于铝元素的原因:
,结合基态原子价层电子排布式解释第一电离能镁元素高于铝元素的原因:
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】C和Si元素在化学中占有极其重要的地位。
(1)写出Si的基态原子核外最外层电子排布式_______ ,C、O、Si三种元素的电负性由大到小的顺序为_______ 。C、N、O三种元素的第一电离能由大到小的顺序为_______ 。
(2)基态铬原子和基态锰原子中第一电离能较大的是_______ (填元素符号),原因为_______ 。
(3)SiC晶体的结构与晶体硅的相似,其中C原子的杂化方式为_______ 。
(4)氧化物XO的电子总数与SiC的相等,则X为_______ (填元素符号),XO是优良的耐高温材料,其熔点比CaO高的原因是_______ 。
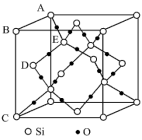
(5)下图表示的是SiO2的晶胞结构(白圈代表硅原子,黑点代表氧原子),判断在30g二氧化硅晶体中含_______ 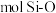 键。
键。
(1)写出Si的基态原子核外最外层电子排布式
(2)基态铬原子和基态锰原子中第一电离能较大的是
(3)SiC晶体的结构与晶体硅的相似,其中C原子的杂化方式为
(4)氧化物XO的电子总数与SiC的相等,则X为

(5)下图表示的是SiO2的晶胞结构(白圈代表硅原子,黑点代表氧原子),判断在30g二氧化硅晶体中含
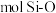 键。
键。
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐1】氟是特种塑料、橡胶和冷冻剂(氟氯烷)中的关键元素。回答下列问题:
(1)基态F原子核外电子的空间运动状态有___________ 种。
(2)同周期元素N、O、F的第一电离能由大到小的顺序为___________ ,N、O、F常见的氢化物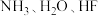 的稳定性由强到弱的顺序为
的稳定性由强到弱的顺序为___________ 。
(3)氟气与水的反应复杂,主要生成 和
和 ,副反应生成少量的
,副反应生成少量的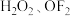 等。
等。 分子的空间构型为
分子的空间构型为___________ ; 与水能以任意比例互溶,原因是
与水能以任意比例互溶,原因是___________ 。在一定浓度的氢氟酸溶液中,部分溶质以二分子缔合 形式存在,使
形式存在,使 分子缔合的作用力是
分子缔合的作用力是___________ 。
(4)同主族元素 的单质均可与水反应生成次卤酸,则
的单质均可与水反应生成次卤酸,则 中氯原子的杂化方式为
中氯原子的杂化方式为___________ 。
(1)基态F原子核外电子的空间运动状态有
(2)同周期元素N、O、F的第一电离能由大到小的顺序为
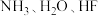 的稳定性由强到弱的顺序为
的稳定性由强到弱的顺序为(3)氟气与水的反应复杂,主要生成
 和
和 ,副反应生成少量的
,副反应生成少量的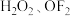 等。
等。 分子的空间构型为
分子的空间构型为 与水能以任意比例互溶,原因是
与水能以任意比例互溶,原因是 形式存在,使
形式存在,使 分子缔合的作用力是
分子缔合的作用力是(4)同主族元素
 的单质均可与水反应生成次卤酸,则
的单质均可与水反应生成次卤酸,则 中氯原子的杂化方式为
中氯原子的杂化方式为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐2】回答下列问题
(1)在较低温度下CuFeS2与浓硫酸作用时,有少量臭鸡蛋气味的气体X产生。
①X分子的立体构型是___________ ,中心原子杂化类型为___________ ,属于___________ (填“极性”或“非极性”)分子。
②X的沸点比水低的主要原因是___________ 。
(2)CuFeS2与氧气反应生成SO2,SO2中心原子的价层电子对数为___________ ,共价键的类型有___________ 。
(1)在较低温度下CuFeS2与浓硫酸作用时,有少量臭鸡蛋气味的气体X产生。
①X分子的立体构型是
②X的沸点比水低的主要原因是
(2)CuFeS2与氧气反应生成SO2,SO2中心原子的价层电子对数为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】按要求回答下列问题
(1)写出下列物质的电子式:N2___________ 、氮化镁___________ 。
(2)比较F、Cl简单氢化物水溶液的酸性强弱___________ >___________ (用化学式表示),NH3和PH3在水中溶解度较大的是___________ ,原因是___________ 。
(3)已知一些物质的熔点数据如下表:
 与
与 均为第三周期元素,
均为第三周期元素, 熔点明显高于
熔点明显高于 ,原因是
,原因是___________ ,分析同族元素的氯化物 、
、 、
、 熔点变化趋势及其原因
熔点变化趋势及其原因___________ 。
(1)写出下列物质的电子式:N2
(2)比较F、Cl简单氢化物水溶液的酸性强弱
(3)已知一些物质的熔点数据如下表:
| 物质 | 熔点/℃ |
 | 800.7 |
 |  |
 | 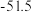 |
 |  |
 与
与 均为第三周期元素,
均为第三周期元素, 熔点明显高于
熔点明显高于 ,原因是
,原因是 、
、 、
、 熔点变化趋势及其原因
熔点变化趋势及其原因
您最近一年使用:0次



