2022年10月18日《自然化学》发表我国科学家研究成果,发现AgCrS2(AMX2家族成员之一,A为一价金属,M为三价金属,X为氧族元素)在室温下具有超离子行为。回答下列问题:
(1)基态硫原子核外电子排布式为___________ 。
(2)氧族元素有氧、硫、硒、碲等元素,其中电负性最大的元素是___________ ,科学家用亚硒酸盐和硫酸盐跟踪固氨酶,研究反应机理。 中硫的杂化轨道类型是
中硫的杂化轨道类型是___________ , 的空间结构模型为
的空间结构模型为___________ 。
(3)配合物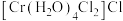 中铬的化合价为
中铬的化合价为___________ ,配离子为___________ ,中心离子配位数为___________ 。
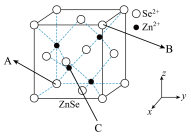
(4)ZnSe晶胞与ZnS晶胞相似(如图),ZnSe晶胞中部分原子的分数坐标为:A点 (0,0,0),B点
(0,0,0),B点 的坐标为
的坐标为___________ ,从该晶胞中找出距离B点Se2-最远的 的位置
的位置___________ (用分数坐标表示),该晶胞中晶胞中 的个数为
的个数为___________ 个,若晶胞中的边长为acm,阿伏加德罗常数的值为 ,请计算ZnSe晶胞的密度
,请计算ZnSe晶胞的密度___________ 
(1)基态硫原子核外电子排布式为
(2)氧族元素有氧、硫、硒、碲等元素,其中电负性最大的元素是
 中硫的杂化轨道类型是
中硫的杂化轨道类型是 的空间结构模型为
的空间结构模型为(3)配合物
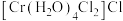 中铬的化合价为
中铬的化合价为(4)ZnSe晶胞与ZnS晶胞相似(如图),ZnSe晶胞中部分原子的分数坐标为:A点
 (0,0,0),B点
(0,0,0),B点 的坐标为
的坐标为 的位置
的位置 的个数为
的个数为 ,请计算ZnSe晶胞的密度
,请计算ZnSe晶胞的密度

更新时间:2023-07-06 01:27:02
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】原子序数依次增大的A、B、C、D、E、F六种元素均为前四周期元素,A是形成化合物种类最多的元素,B与A同周期,其原子核外s能级上的电子总数与p能级上的电子总数相等,C为第3周期元素,其离子半径在该周期中最小,D原子核外p能级上的电子总数比s能级上的电子总数多2,E元素位于元素周期表中的第8列,F的单质为紫红色金属。回答下列问题:
(1)D在元素周期表中的位置为___________ 。
(2)A元素的原子核外共有___________ 种不同运动状态的电子;B元素基态原子中能量最高的电子所占据的原子轨道呈___________ 形。
(3)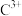 与过量氨水反应的离子方程式为
与过量氨水反应的离子方程式为___________ 。
(4)E元素位于元素周期表中___________ 区(按电子排布分区),其基态原子价电子轨道表示式为___________ 。
(5)基态F原子的核外电子排布式为___________ ,其基态原子核外填充有电子的能量最高的电子层的符号为___________ ,该电子层上具有的原子轨道数是___________ 。
(1)D在元素周期表中的位置为
(2)A元素的原子核外共有
(3)
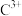 与过量氨水反应的离子方程式为
与过量氨水反应的离子方程式为(4)E元素位于元素周期表中
(5)基态F原子的核外电子排布式为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】翡翠的主要成分为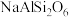 ,还含有其他多种金属阳离子。
,还含有其他多种金属阳离子。
(1)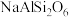 所含元素中,第一电离能最小的元素和电负性最大的元素组成的含有两种化学键的化合物的名称为:
所含元素中,第一电离能最小的元素和电负性最大的元素组成的含有两种化学键的化合物的名称为:___________ 。
(2)Al的电子排布式为___________ 。
(3)配合物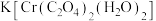 中的配体是:
中的配体是:___________ ,Cr的价层电子的电子排布图:___________ 。
(4)Ca、O、Cr可以形成一种具有特殊导电性的复合氧化物,晶胞结构如图所示,其中 ,
, 采用面心立方最密堆积方式。
采用面心立方最密堆积方式。

①该晶体的化学式为:___________ 。
②已知钙离子、氧离子半径分别为apm、bpm,该晶胞的参数(边长)为___________ pm。
(5)Ga可以形成 等一系列配位数为6的配合物,向上述某物质的溶液中加入足量
等一系列配位数为6的配合物,向上述某物质的溶液中加入足量 溶液,有沉淀生成;过滤后,充分加热滤液有氨气逸出,且又有沉淀生成,两次沉淀的物质的量之比为1:2.则该溶液中溶质的化学式为
溶液,有沉淀生成;过滤后,充分加热滤液有氨气逸出,且又有沉淀生成,两次沉淀的物质的量之比为1:2.则该溶液中溶质的化学式为___________ 。
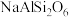 ,还含有其他多种金属阳离子。
,还含有其他多种金属阳离子。(1)
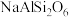 所含元素中,第一电离能最小的元素和电负性最大的元素组成的含有两种化学键的化合物的名称为:
所含元素中,第一电离能最小的元素和电负性最大的元素组成的含有两种化学键的化合物的名称为:(2)Al的电子排布式为
(3)配合物
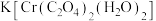 中的配体是:
中的配体是:(4)Ca、O、Cr可以形成一种具有特殊导电性的复合氧化物,晶胞结构如图所示,其中
 ,
, 采用面心立方最密堆积方式。
采用面心立方最密堆积方式。
①该晶体的化学式为:
②已知钙离子、氧离子半径分别为apm、bpm,该晶胞的参数(边长)为
(5)Ga可以形成
 等一系列配位数为6的配合物,向上述某物质的溶液中加入足量
等一系列配位数为6的配合物,向上述某物质的溶液中加入足量 溶液,有沉淀生成;过滤后,充分加热滤液有氨气逸出,且又有沉淀生成,两次沉淀的物质的量之比为1:2.则该溶液中溶质的化学式为
溶液,有沉淀生成;过滤后,充分加热滤液有氨气逸出,且又有沉淀生成,两次沉淀的物质的量之比为1:2.则该溶液中溶质的化学式为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
【推荐3】回答下列问题:
(1) 、
、 、
、 是三种重要的金属元素。三种元素二价氧化物的晶胞类型相同,其熔点由高到低的顺序为
是三种重要的金属元素。三种元素二价氧化物的晶胞类型相同,其熔点由高到低的顺序为_______ 。
(2) 的四卤化物熔点如下表所示,
的四卤化物熔点如下表所示, 熔点高于其他二种卤化物,原因是
熔点高于其他二种卤化物,原因是_______ 。
(3)一些氧化物的熔点如下表所示:
解释表中氧化物之间熔点差异的原因:_______ 。
氮化镓是一种半导体材料。晶胞结构可看作金刚石晶胞内部的碳原子被 原子代替(如
原子代替(如 ),顶点和面心的碳原子被
),顶点和面心的碳原子被 原子代替(如
原子代替(如 )。
)。

(4)写出 的价电子排布式
的价电子排布式_______ 。
(5)基态 原子核外电子能量最高的电子所占的能级是
原子核外电子能量最高的电子所占的能级是_______ 。
(6)与同一个 原子相连的
原子相连的 原子构成的空间构型为
原子构成的空间构型为_______ 。
(7) 晶体中
晶体中 和
和 的原子核间距为
的原子核间距为 ,
, 摩尔质量为
摩尔质量为 ,阿伏伽德罗常数的值为
,阿伏伽德罗常数的值为 ,则
,则 晶体的密度为
晶体的密度为_______ 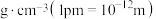 。
。
(1)
 、
、 、
、 是三种重要的金属元素。三种元素二价氧化物的晶胞类型相同,其熔点由高到低的顺序为
是三种重要的金属元素。三种元素二价氧化物的晶胞类型相同,其熔点由高到低的顺序为(2)
 的四卤化物熔点如下表所示,
的四卤化物熔点如下表所示, 熔点高于其他二种卤化物,原因是
熔点高于其他二种卤化物,原因是| 化合物 |  |  |  |
| 熔点/℃ | 377 | -24.12 | 155 |
| 氧化物 | 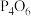 |  |
| 熔点/℃ | 23.8 | -75.5 |
氮化镓是一种半导体材料。晶胞结构可看作金刚石晶胞内部的碳原子被
 原子代替(如
原子代替(如 ),顶点和面心的碳原子被
),顶点和面心的碳原子被 原子代替(如
原子代替(如 )。
)。
(4)写出
 的价电子排布式
的价电子排布式(5)基态
 原子核外电子能量最高的电子所占的能级是
原子核外电子能量最高的电子所占的能级是(6)与同一个
 原子相连的
原子相连的 原子构成的空间构型为
原子构成的空间构型为(7)
 晶体中
晶体中 和
和 的原子核间距为
的原子核间距为 ,
, 摩尔质量为
摩尔质量为 ,阿伏伽德罗常数的值为
,阿伏伽德罗常数的值为 ,则
,则 晶体的密度为
晶体的密度为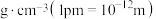 。
。
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐1】治疗疟疾的有效药物青蒿素是白色针状晶体,受热不稳定,易溶于乙醇和乙醚;乙醚( )的沸点小于乙醇的。按要求回答下列问题。
)的沸点小于乙醇的。按要求回答下列问题。
(1)青蒿素的提取:
①萃取剂选用乙醚( )而不用乙醇。这使蒸馏分离提纯青蒿素时效果更好的原因是
)而不用乙醇。这使蒸馏分离提纯青蒿素时效果更好的原因是_____ 。
②将粗品蒸馏所用装置如图所示,虚线框内应选用右侧的仪器_____ (填“x”或“y”)。
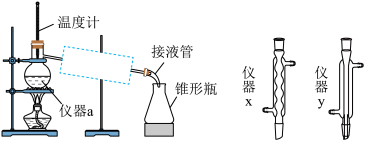
(2)青蒿素的分子式的确定
①经元素分析,得知其分子中含有C、H、O三种元素,其中电负性最最大的是_________ 。
②经测定得知其相对分子质量为282,所用物理方法名称是_________ 。
(3)青蒿素的分子结构的确定
①用红外光线照射青蒿素分子,是为获得其__________________ 信息。
②通过晶体X射线衍射实验,获得其晶胞的类型和大小、原子的种类和数目等信息,可计算出原子间的距离,判断出晶体中哪些原子间存在化学键,进而确定键参数如_________ 、_________ ,得出该分子的空间结构及其晶胞(长方体,棱长分别为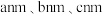 ,含4个青蒿素分子),如图甲所示。
,含4个青蒿素分子),如图甲所示。
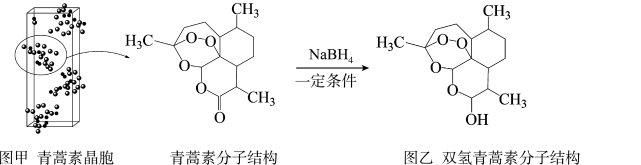
③晶体的密度为_________  (阿伏伽德罗常数的值设为
(阿伏伽德罗常数的值设为 ;列出表达式)。
;列出表达式)。
(4)青蒿素结构的修饰:一定条件下,用 将青蒿素选择性反应,结构修饰为双氢青蒿素(如图乙)。
将青蒿素选择性反应,结构修饰为双氢青蒿素(如图乙)。
①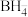 的中心原子的VSEPR模型名称为
的中心原子的VSEPR模型名称为_________ 。
②青蒿素结构修饰过程中,杂化轨道发生变化的碳原子的杂化方式变为_________ ,对应的官能团转变为_________ 。
 )的沸点小于乙醇的。按要求回答下列问题。
)的沸点小于乙醇的。按要求回答下列问题。(1)青蒿素的提取:
①萃取剂选用乙醚(
 )而不用乙醇。这使蒸馏分离提纯青蒿素时效果更好的原因是
)而不用乙醇。这使蒸馏分离提纯青蒿素时效果更好的原因是②将粗品蒸馏所用装置如图所示,虚线框内应选用右侧的仪器

(2)青蒿素的分子式的确定
①经元素分析,得知其分子中含有C、H、O三种元素,其中电负性最最大的是
②经测定得知其相对分子质量为282,所用物理方法名称是
(3)青蒿素的分子结构的确定
①用红外光线照射青蒿素分子,是为获得其
②通过晶体X射线衍射实验,获得其晶胞的类型和大小、原子的种类和数目等信息,可计算出原子间的距离,判断出晶体中哪些原子间存在化学键,进而确定键参数如
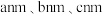 ,含4个青蒿素分子),如图甲所示。
,含4个青蒿素分子),如图甲所示。
③晶体的密度为
 (阿伏伽德罗常数的值设为
(阿伏伽德罗常数的值设为 ;列出表达式)。
;列出表达式)。(4)青蒿素结构的修饰:一定条件下,用
 将青蒿素选择性反应,结构修饰为双氢青蒿素(如图乙)。
将青蒿素选择性反应,结构修饰为双氢青蒿素(如图乙)。①
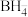 的中心原子的VSEPR模型名称为
的中心原子的VSEPR模型名称为②青蒿素结构修饰过程中,杂化轨道发生变化的碳原子的杂化方式变为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐2】硒( )是人体必需微量元素之一,含硒化合物在材料和药物领域具有重要应用。自我国科学家发现聚集诱导发光(
)是人体必需微量元素之一,含硒化合物在材料和药物领域具有重要应用。自我国科学家发现聚集诱导发光( )效应以来,
)效应以来, 在发光材料、生物医学等领域引起广泛关注。一种含
在发光材料、生物医学等领域引起广泛关注。一种含 的新型
的新型 分子
分子 的合成路线如下:
的合成路线如下: 与S同族,基态硒原子价电子排布式为
与S同族,基态硒原子价电子排布式为_______ 。
(2) 的沸点低于
的沸点低于 ,其原因是
,其原因是_______ 。
(3)关于I~III三种反应物,下列说法正确的有_______ 。
A.I中仅有 键
键
B.I中的 键为非极性共价键
键为非极性共价键
C.II易溶于水
D.II中原子的杂化轨道类型只有 与
与
E.I~III含有的元素中,O电负性最大
(4)IV中具有孤对电子的原子有_______ 。
(5)硒的两种含氧酸的酸性强弱为
_______  (填“>”或“<”)。研究发现,给小鼠喂食适量硒酸钠(
(填“>”或“<”)。研究发现,给小鼠喂食适量硒酸钠( )可减轻重金属铊引起的中毒。
)可减轻重金属铊引起的中毒。 的立体构型为
的立体构型为_______ 。
(6)我国科学家发展了一种理论计算方法,可利用材料的晶体结构数据预测其热电性能,该方法有助于加速新型热电材料的研发进程。化合物X是通过该方法筛选出的潜在热电材料之一,其晶胞结构如图1,沿x、y、z轴方向的投影均为图2。_______ 。
②设X的最简式的式量为 ,晶体密度为
,晶体密度为 ,则X中相邻K之间的最短距离为
,则X中相邻K之间的最短距离为_______  (列出计算式,
(列出计算式, 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
 )是人体必需微量元素之一,含硒化合物在材料和药物领域具有重要应用。自我国科学家发现聚集诱导发光(
)是人体必需微量元素之一,含硒化合物在材料和药物领域具有重要应用。自我国科学家发现聚集诱导发光( )效应以来,
)效应以来, 在发光材料、生物医学等领域引起广泛关注。一种含
在发光材料、生物医学等领域引起广泛关注。一种含 的新型
的新型 分子
分子 的合成路线如下:
的合成路线如下: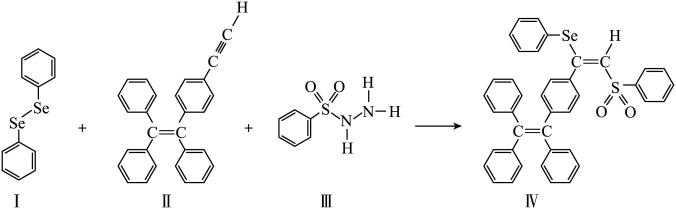
 与S同族,基态硒原子价电子排布式为
与S同族,基态硒原子价电子排布式为(2)
 的沸点低于
的沸点低于 ,其原因是
,其原因是(3)关于I~III三种反应物,下列说法正确的有
A.I中仅有
 键
键B.I中的
 键为非极性共价键
键为非极性共价键C.II易溶于水
D.II中原子的杂化轨道类型只有
 与
与
E.I~III含有的元素中,O电负性最大
(4)IV中具有孤对电子的原子有
(5)硒的两种含氧酸的酸性强弱为

 (填“>”或“<”)。研究发现,给小鼠喂食适量硒酸钠(
(填“>”或“<”)。研究发现,给小鼠喂食适量硒酸钠( )可减轻重金属铊引起的中毒。
)可减轻重金属铊引起的中毒。 的立体构型为
的立体构型为(6)我国科学家发展了一种理论计算方法,可利用材料的晶体结构数据预测其热电性能,该方法有助于加速新型热电材料的研发进程。化合物X是通过该方法筛选出的潜在热电材料之一,其晶胞结构如图1,沿x、y、z轴方向的投影均为图2。
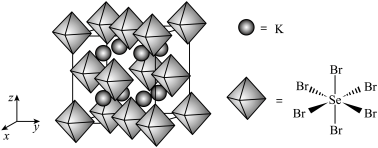
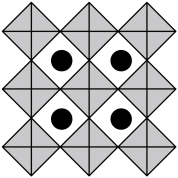
②设X的最简式的式量为
 ,晶体密度为
,晶体密度为 ,则X中相邻K之间的最短距离为
,则X中相邻K之间的最短距离为 (列出计算式,
(列出计算式, 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】铜是应用最广泛的金属之一,其抗氧化防腐技术一直是化学研究的热点课题。
(1)基态铜原子的价电子排布图为_____ ,铜元素位于元素周期表中_____ 区。
(2)我国科学家发现经甲酸钠(HCOONa)溶液热处理后的金属铜具有良好的抗氧化能力。
①组成甲酸钠的四种元素的电负性由大到小的顺序为_____ 。
②HCOO-中碳原子的杂化方式为_____ ,其空间构型为____ 。
③HCOOH能与水任意比互溶的原因为_____ 。
(3)在金属铜表面覆盖WBN型氮化硼(熔点为2967℃)也可以达到金属铜的防腐目的,WBN型氮化硼属于_____ 晶体。
(1)基态铜原子的价电子排布图为
(2)我国科学家发现经甲酸钠(HCOONa)溶液热处理后的金属铜具有良好的抗氧化能力。
①组成甲酸钠的四种元素的电负性由大到小的顺序为
②HCOO-中碳原子的杂化方式为
③HCOOH能与水任意比互溶的原因为
(3)在金属铜表面覆盖WBN型氮化硼(熔点为2967℃)也可以达到金属铜的防腐目的,WBN型氮化硼属于
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐1】过渡金属元素及其化合物的应用广泛,是科学家们进行前沿研究的方向之一、
(1)CuCl的盐酸溶液能够与CO发生反应: 。上述化学方程式中的4种物质含有的化学键类型有
。上述化学方程式中的4种物质含有的化学键类型有___________ 。
A.配位键 B.极性键 C.离子键 D.非极性键 E.氢键 F.金属键
(2) 是一种紫色晶体,其中DMSO为二甲基亚矾,化学式为
是一种紫色晶体,其中DMSO为二甲基亚矾,化学式为 。
。 中C—S—O的键角
中C—S—O的键角___________ (填“大于”“小于”或“等于”) 中C—C—O的键角,理由是
中C—C—O的键角,理由是___________ ;元素S、Cl、O的电负性由大到小的顺序为___________ 。
(3) 溶液与乙二胺(
溶液与乙二胺(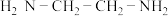 )可形成配离子
)可形成配离子 (En是乙二胺的简写):
(En是乙二胺的简写): 的配位原子为
的配位原子为___________ 。
②乙二胺分子中氮原子轨道的杂化类型为___________ ,乙二胺和三甲胺 均属于胺,但乙二胺比三甲胺的沸点高的多,原因是
均属于胺,但乙二胺比三甲胺的沸点高的多,原因是___________ 。
(1)CuCl的盐酸溶液能够与CO发生反应:
 。上述化学方程式中的4种物质含有的化学键类型有
。上述化学方程式中的4种物质含有的化学键类型有A.配位键 B.极性键 C.离子键 D.非极性键 E.氢键 F.金属键
(2)
 是一种紫色晶体,其中DMSO为二甲基亚矾,化学式为
是一种紫色晶体,其中DMSO为二甲基亚矾,化学式为 。
。 中C—S—O的键角
中C—S—O的键角 中C—C—O的键角,理由是
中C—C—O的键角,理由是(3)
 溶液与乙二胺(
溶液与乙二胺(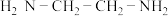 )可形成配离子
)可形成配离子 (En是乙二胺的简写):
(En是乙二胺的简写):
 的配位原子为
的配位原子为②乙二胺分子中氮原子轨道的杂化类型为
 均属于胺,但乙二胺比三甲胺的沸点高的多,原因是
均属于胺,但乙二胺比三甲胺的沸点高的多,原因是
您最近一年使用:0次
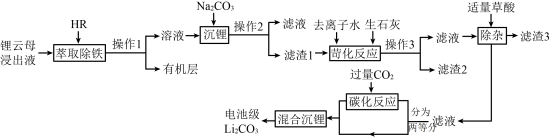
【推荐2】电池级碳酸锂是制造LiCoO2等锂离子电池必不可少的原材料。享誉“亚洲锂都”的宜春拥有亚洲储量最大的锂云母矿,以锂云母浸出液(含Li+、Fe3+、Mg2+、SO 等)为原料制取电池级Li2CO3的工艺流程如图:
等)为原料制取电池级Li2CO3的工艺流程如图:
已知:①HR为有机萃取剂,难溶于水,可萃取Fe3+,萃取时发生的反应可表示为:Fe3++3HR⇌FeR3+3H+;
②常温时,1mol·L-1LiOH溶液的pH=14。
回答下列问题:
(1)“滤渣1”中含有的物质为________ 。
(2)某种HR的结构简式为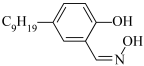 ,该分子中可能与Fe3+形成配位键的原子有
,该分子中可能与Fe3+形成配位键的原子有_____ 。
(3)加适量草酸的目的____________________________________________ 。
(4)“混合沉锂”的离子方程式为_______________________________________ 。
(5)Li2CO3与Co3O4在空气中加热可以制备重要的电极材料钴酸锂(LiCoO2)。写出对应的化学方程式____________________________________________ 。
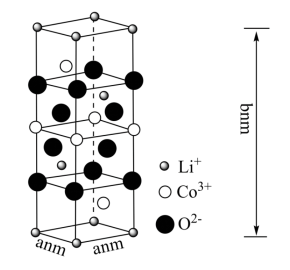
(6)钴酸锂(LiCoO2)是常见的锂离子电池正极材料,其晶胞结构示意图如下图所示,各离子位于晶胞的顶点、棱和体内。
②该晶胞密度为___________ g.cm-3。(写出计算式,阿伏加德罗常数为NA)
 等)为原料制取电池级Li2CO3的工艺流程如图:
等)为原料制取电池级Li2CO3的工艺流程如图:已知:①HR为有机萃取剂,难溶于水,可萃取Fe3+,萃取时发生的反应可表示为:Fe3++3HR⇌FeR3+3H+;
②常温时,1mol·L-1LiOH溶液的pH=14。
回答下列问题:
(1)“滤渣1”中含有的物质为
(2)某种HR的结构简式为
 ,该分子中可能与Fe3+形成配位键的原子有
,该分子中可能与Fe3+形成配位键的原子有(3)加适量草酸的目的
(4)“混合沉锂”的离子方程式为
(5)Li2CO3与Co3O4在空气中加热可以制备重要的电极材料钴酸锂(LiCoO2)。写出对应的化学方程式
(6)钴酸锂(LiCoO2)是常见的锂离子电池正极材料,其晶胞结构示意图如下图所示,各离子位于晶胞的顶点、棱和体内。
①基态Co原子核外电子排布式为
②该晶胞密度为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】秦始皇帝陵博物院首次在兵马俑的彩绘中发现了古人人工合成的“中国蓝”“中国紫”颜料。通过对这些颜料的研究发现,其成分主要是钡和铜的硅酸盐(BaCuSixOy) 。
回答下列问题:
(1)“中国蓝”的发色与硫酸铜溶液呈天蓝色类似,都是由于形成了[Cu(H2O)4]2+,该配离子中Cu2+提供_______ ,配位原子是_______ ,1 mol [Cu(H2O)4]2+中σ键的数目为_________ 。
(2)写出向硫酸铜溶液里逐滴加入氨水过程中沉淀溶解的离子方程式_______________ ,再向溶液中加入乙醇,会析出深蓝色晶体____________ (写出化学式)。
(3)“中国蓝”“中国紫”中存在 四面体结构,其中Si原子采取的杂化方式为
四面体结构,其中Si原子采取的杂化方式为_______ 。
(4)BaO的熔沸点_____ MgO(填“>”“<”“=”),原因是______________ 。
(5)立方CuO晶胞结构如图所示。其中Cu2+的配位数为_______ 。NA代表阿伏加德罗常数的值,晶胞参数为a pm,则其晶体密度为___________ g·cm-3。
回答下列问题:
(1)“中国蓝”的发色与硫酸铜溶液呈天蓝色类似,都是由于形成了[Cu(H2O)4]2+,该配离子中Cu2+提供
(2)写出向硫酸铜溶液里逐滴加入氨水过程中沉淀溶解的离子方程式
(3)“中国蓝”“中国紫”中存在
 四面体结构,其中Si原子采取的杂化方式为
四面体结构,其中Si原子采取的杂化方式为(4)BaO的熔沸点
(5)立方CuO晶胞结构如图所示。其中Cu2+的配位数为

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐1】A、B、C、D 4种短周期元素,原子序数依次增大。其元素相关信息如下表。
(1)元素A、B、C中,电负性最大的是_______ (填元素符号)。
(2)A与B形成共价化合物 ,其分子的空间结构呈
,其分子的空间结构呈_______ 形。
(3) 易溶于
易溶于 中的原因是
中的原因是_______ 。
(4) 中B原子轨道的杂化类型为
中B原子轨道的杂化类型为_______ ; 的空间结构为
的空间结构为_______ 。
(5)B和D两种元素组成的化合物是共价晶体,其晶胞如下图所示,则表示该化合物的化学式为_______ (请用元素符号表示)。
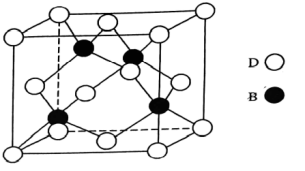
| 元素 | 信息 |
| A | 元素原子的核外电子只有一种运动状态 |
| B | 价电子层中的未成对电子有3个 |
| C | 最外层电子数为其内层电子数的3倍 |
| D | 离子半径在同周期金属元素中最小 |
(1)元素A、B、C中,电负性最大的是
(2)A与B形成共价化合物
 ,其分子的空间结构呈
,其分子的空间结构呈(3)
 易溶于
易溶于 中的原因是
中的原因是(4)
 中B原子轨道的杂化类型为
中B原子轨道的杂化类型为 的空间结构为
的空间结构为(5)B和D两种元素组成的化合物是共价晶体,其晶胞如下图所示,则表示该化合物的化学式为

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】钛酸锌(ZnTiO3)是一种抗菌涂料,应用于人造骨骼等生物移植技术。回答下列问题:
(1)基态Zn原子的电子占据能量最高的能层符号为_____________ ,与Zn同周期的所有副族元素的基态原子中,最外层电子数与Zn相同的元素有___________ 种
(2)钛能与B、C、N、O等非金属元素形成稳定的化合物。则电负性C____ B(选填“>或“<”);第一电离能N>O,原因是__________________________________________ 。
(3)ZnTiO3与80%H2SO4反应可生成TiOSO4。
① 的空间构型为
的空间构型为_____________ ,其中硫原子采用____________ 杂化。
②与 互为等电子体的分子的化学式为
互为等电子体的分子的化学式为_________________ (任写一种即可)
(4)Zn与S所形成化合物晶体的晶胞如图所示。

①与Zn原子距离最近的Zn原子有___________ 个。
②该化合物的化学式为_________________________________ 。
③已知该晶体的晶胞参数为a×10-12m,阿伏加 德罗常数为NA。则该晶体的密度为__________________ g/cm3(列式即可)
(1)基态Zn原子的电子占据能量最高的能层符号为
(2)钛能与B、C、N、O等非金属元素形成稳定的化合物。则电负性C
(3)ZnTiO3与80%H2SO4反应可生成TiOSO4。
①
 的空间构型为
的空间构型为②与
 互为等电子体的分子的化学式为
互为等电子体的分子的化学式为(4)Zn与S所形成化合物晶体的晶胞如图所示。

①与Zn原子距离最近的Zn原子有
②该化合物的化学式为
③已知该晶体的晶胞参数为a×10-12m,阿伏加 德罗常数为NA。则该晶体的密度为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
【推荐3】新冠期间受“谣言”影响蒙脱石散曾一度脱销。蒙脱石散的有效成分可表示(AlMg)2(SixOy)(OH)z•nH2O,常用于成人及儿童急、慢性腹泻。
(1)基态Si原子的电子排布式为_______ 。
(2)比较B、Al第一电离能大小:I1(Al)_______ I1(B)(填“>”或“<”),说明判断理由_______ 。
(3)SiCl4能用于制取纯硅、硅酸乙酯等,也能用于制取烟幕剂。
①将用毛皮摩擦过的橡胶棒靠近SiCl4液流,液流_______ (填“会”或“不会”)发生偏转。
②SiH4、CH4中较稳定的是_______ ;SiCl4、CCl4中沸点较高是_______ 。
(4)硅酸盐与二氧化硅一样,都是以硅氧四面体作为基本结构单元。
①蒙脱石散中的“(SixOy)”是一种大片层状的多硅酸根,其可能结构如图所示:

据此分析,x:y=_______ 。
②SiO2晶胞可理解成将金刚石晶胞(如图)中的C原子置换成Si原子,然后在Si-Si之间插入O原子而形成。若SiO2晶胞的密度为dg•cm-3,NA表示阿伏加德罗常数的值,则晶胞中Si与Si之间的最短距离为_______ nm(用含NA表和d的式子表示)。

(1)基态Si原子的电子排布式为
(2)比较B、Al第一电离能大小:I1(Al)
(3)SiCl4能用于制取纯硅、硅酸乙酯等,也能用于制取烟幕剂。
①将用毛皮摩擦过的橡胶棒靠近SiCl4液流,液流
②SiH4、CH4中较稳定的是
(4)硅酸盐与二氧化硅一样,都是以硅氧四面体作为基本结构单元。
①蒙脱石散中的“(SixOy)”是一种大片层状的多硅酸根,其可能结构如图所示:

据此分析,x:y=
②SiO2晶胞可理解成将金刚石晶胞(如图)中的C原子置换成Si原子,然后在Si-Si之间插入O原子而形成。若SiO2晶胞的密度为dg•cm-3,NA表示阿伏加德罗常数的值,则晶胞中Si与Si之间的最短距离为

您最近一年使用:0次



