过渡金属元素及其化合物的应用广泛,是科学家们进行前沿研究的方向之一、
(1)CuCl的盐酸溶液能够与CO发生反应: 。上述化学方程式中的4种物质含有的化学键类型有
。上述化学方程式中的4种物质含有的化学键类型有___________ 。
A.配位键 B.极性键 C.离子键 D.非极性键 E.氢键 F.金属键
(2) 是一种紫色晶体,其中DMSO为二甲基亚矾,化学式为
是一种紫色晶体,其中DMSO为二甲基亚矾,化学式为 。
。 中C—S—O的键角
中C—S—O的键角___________ (填“大于”“小于”或“等于”) 中C—C—O的键角,理由是
中C—C—O的键角,理由是___________ ;元素S、Cl、O的电负性由大到小的顺序为___________ 。
(3) 溶液与乙二胺(
溶液与乙二胺(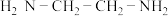 )可形成配离子
)可形成配离子 (En是乙二胺的简写):
(En是乙二胺的简写): 的配位原子为
的配位原子为___________ 。
②乙二胺分子中氮原子轨道的杂化类型为___________ ,乙二胺和三甲胺 均属于胺,但乙二胺比三甲胺的沸点高的多,原因是
均属于胺,但乙二胺比三甲胺的沸点高的多,原因是___________ 。
(1)CuCl的盐酸溶液能够与CO发生反应:
 。上述化学方程式中的4种物质含有的化学键类型有
。上述化学方程式中的4种物质含有的化学键类型有A.配位键 B.极性键 C.离子键 D.非极性键 E.氢键 F.金属键
(2)
 是一种紫色晶体,其中DMSO为二甲基亚矾,化学式为
是一种紫色晶体,其中DMSO为二甲基亚矾,化学式为 。
。 中C—S—O的键角
中C—S—O的键角 中C—C—O的键角,理由是
中C—C—O的键角,理由是(3)
 溶液与乙二胺(
溶液与乙二胺(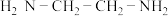 )可形成配离子
)可形成配离子 (En是乙二胺的简写):
(En是乙二胺的简写):
 的配位原子为
的配位原子为②乙二胺分子中氮原子轨道的杂化类型为
 均属于胺,但乙二胺比三甲胺的沸点高的多,原因是
均属于胺,但乙二胺比三甲胺的沸点高的多,原因是
更新时间:2024-04-15 09:08:23
|
相似题推荐
【推荐1】镍的化合物是一组多彩的物质。
(1)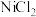 呈黄色,其中
呈黄色,其中 的价电子轨道表示式为
的价电子轨道表示式为______ 。
(2) 呈绿色,晶体结构与氯化钠类似,每个
呈绿色,晶体结构与氯化钠类似,每个 周围有
周围有______ 个最近距离的 。
。
(3) 是一种无色挥发性液体,沸点为
是一种无色挥发性液体,沸点为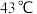 ,熔点为
,熔点为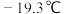 。
。
①它形成的晶体类型为______ 。
②配体 中
中 键和
键和 键的个数比为
键的个数比为______ 。
(4)丁二酮肟镍呈鲜红色,其结构如下图。

①分子中第二周期元素的第一电离能由大到小的顺序为______ 。
②丁二酮肟镍分子中存在的化学键有______ 。
A.共价键 B.氢键 C.离子键 D.金属键 E.配位键
(1)
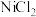 呈黄色,其中
呈黄色,其中 的价电子轨道表示式为
的价电子轨道表示式为(2)
 呈绿色,晶体结构与氯化钠类似,每个
呈绿色,晶体结构与氯化钠类似,每个 周围有
周围有 。
。(3)
 是一种无色挥发性液体,沸点为
是一种无色挥发性液体,沸点为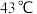 ,熔点为
,熔点为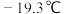 。
。①它形成的晶体类型为
②配体
 中
中 键和
键和 键的个数比为
键的个数比为(4)丁二酮肟镍呈鲜红色,其结构如下图。

①分子中第二周期元素的第一电离能由大到小的顺序为
②丁二酮肟镍分子中存在的化学键有
A.共价键 B.氢键 C.离子键 D.金属键 E.配位键
您最近半年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】下表为元素周期表中的一部分,表中列出了10种元素在周期表中的位置,按要求完成下列各小题。
(1)这10种元素中,化学性质最不活泼的元素是________ (填元素符号),非金属性最强的元素是________ (填元素符号)。
(2)①③⑤三种元素的最高价氧化物对应的水化物中,碱性最强的化合物的电子式是________ 。
(3)①②③三种元素的原子半径由大到小的顺序是________ (填元素符号)。
(4)某元素的最高价氧化物对应的水化物既能与酸又能和碱反应生成盐和水,向该元素和⑨号元素形成的化合物的溶液中,缓慢滴加氢氧化钠溶液至过量,产生的实验现象是________ 。
(5)下列物质中:①N2 ②CO2 ③NH3 ④Na2O ⑤Na2O2 ⑥NaOH ⑦ NH4Cl ⑧ H2O2既含有极性键又含有非极性键的是________ ;(填序号)
(6)晶体中阳离子阴离子个数比为2:1的有________ (填序号)
(7)含有配位键的是________ (填序号)
(8)非极性分子有________ (填序号)
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
2 | ⑥ | ⑦ | ⑧ | |||||
3 | ① | ③ | ⑤ | ⑨ | ⑩ | |||
4 | ② | ④ |
(1)这10种元素中,化学性质最不活泼的元素是
(2)①③⑤三种元素的最高价氧化物对应的水化物中,碱性最强的化合物的电子式是
(3)①②③三种元素的原子半径由大到小的顺序是
(4)某元素的最高价氧化物对应的水化物既能与酸又能和碱反应生成盐和水,向该元素和⑨号元素形成的化合物的溶液中,缓慢滴加氢氧化钠溶液至过量,产生的实验现象是
(5)下列物质中:①N2 ②CO2 ③NH3 ④Na2O ⑤Na2O2 ⑥NaOH ⑦ NH4Cl ⑧ H2O2既含有极性键又含有非极性键的是
(6)晶体中阳离子阴离子个数比为2:1的有
(7)含有配位键的是
(8)非极性分子有
您最近半年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】X、Y、Z、W是关乎宇宙起源、生命形成的最为核心的元素,称之为元素中的“四大天王”,其中Y、Z、W位于同一周期,且原子序数依次增大。下表是6种元素的相关信息:
(1)Y元素在周期表中的位置是_______ 。
(2)Z的气态氢化物可与其最高价氧化物的水化物化合生成M,写出M中存在的化学键的类型_______ 。
(3)请写出U的最高价氧化物的水化物与氢氧化钠溶液反应的离子方程式_______ (U用实际元素符号表示)。
(4)比较沸点:X2W_______ X2V (填“>”、“=”或“<”)。
| X | 该元素的一种核素的中子数为0 |
| Y | 能与X形成正四面体形的分子 |
| Z | 空气中含量最多的元素 |
| W | 其单质通常作助燃剂 |
| U | 地壳中含量最多的金属元素 |
| V | M层电子数是K层的3倍 |
(2)Z的气态氢化物可与其最高价氧化物的水化物化合生成M,写出M中存在的化学键的类型
(3)请写出U的最高价氧化物的水化物与氢氧化钠溶液反应的离子方程式
(4)比较沸点:X2W
您最近半年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐1】N、P、Sb原子的最外层电子数都是5,与卤素原子形成的化合物有广泛用途。 是液晶显示器生产过程中常用的化学清洗剂,
是液晶显示器生产过程中常用的化学清洗剂, 可用于面粉的漂白和杀菌,
可用于面粉的漂白和杀菌, 广泛应用于农药、杀虫剂的制造,
广泛应用于农药、杀虫剂的制造, 常用于有机反应催化剂。
常用于有机反应催化剂。
(1)几种化学键的键能如下表所示:
由两种单质化合形成1mol  ,焓变
,焓变
___________  。
。
(2)已知: 常温常压下为无色气体,熔点-129℃,沸点-207℃;
常温常压下为无色气体,熔点-129℃,沸点-207℃; 为黄色油状液体,熔点-40℃,沸点70℃,95℃以上易爆炸。根据物质结构知识和题中信息解释以下问题:
为黄色油状液体,熔点-40℃,沸点70℃,95℃以上易爆炸。根据物质结构知识和题中信息解释以下问题:
① 热稳定性高于
热稳定性高于 :
:___________ 。
② 熔、沸点高于
熔、沸点高于 :
:___________ 。
(3) 在水中溶解度不大,而
在水中溶解度不大,而 在水中溶解度较大,由此判断是
在水中溶解度较大,由此判断是
___________ 分子, 是
是___________ 分子。(填“极性”或“非极性”)
 是液晶显示器生产过程中常用的化学清洗剂,
是液晶显示器生产过程中常用的化学清洗剂, 可用于面粉的漂白和杀菌,
可用于面粉的漂白和杀菌, 广泛应用于农药、杀虫剂的制造,
广泛应用于农药、杀虫剂的制造, 常用于有机反应催化剂。
常用于有机反应催化剂。(1)几种化学键的键能如下表所示:
| 化学键 |  |  |  |
键能/ | 941.6 | 154.8 | 283.0 |
 ,焓变
,焓变
 。
。(2)已知:
 常温常压下为无色气体,熔点-129℃,沸点-207℃;
常温常压下为无色气体,熔点-129℃,沸点-207℃; 为黄色油状液体,熔点-40℃,沸点70℃,95℃以上易爆炸。根据物质结构知识和题中信息解释以下问题:
为黄色油状液体,熔点-40℃,沸点70℃,95℃以上易爆炸。根据物质结构知识和题中信息解释以下问题:①
 热稳定性高于
热稳定性高于 :
:②
 熔、沸点高于
熔、沸点高于 :
:(3)
 在水中溶解度不大,而
在水中溶解度不大,而 在水中溶解度较大,由此判断是
在水中溶解度较大,由此判断是
 是
是
您最近半年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】已知  和
和 可以形成
可以形成  和
和  两种化合物,试根据有关信息完成下列问题:
两种化合物,试根据有关信息完成下列问题:
① 内的
内的 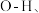 水分子间的范德华力和氢键,从强到弱依次为
水分子间的范德华力和氢键,从强到弱依次为___________ ;
②用球棍模型表示的水分子结构是 ; 可与
可与  形成
形成 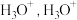 中的
中的 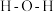 键角比
键角比  的键角
的键角___________ 。(填“大”或“小”)
(2)已知 分子的结构如图所示:
分子的结构如图所示: 分子不是直线形的,两个氢原子犹如在半展开的书的两面上,两个氧原子在书脊位置上,书页夹角
分子不是直线形的,两个氢原子犹如在半展开的书的两面上,两个氧原子在书脊位置上,书页夹角 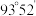 ,而两个
,而两个  键与
键与  键的夹角均为
键的夹角均为 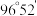 。
。
请回答下列问题:
① 子的电子式是
子的电子式是___________ ,结构式是___________ 。
② 分子是含有
分子是含有___________ 键和___________ 键的___________ (填“极性”或“非极性”)分子。
③ 能与水混溶,却不溶于
能与水混溶,却不溶于  试剂,请予以解释:
试剂,请予以解释:___________ 。
 和
和 可以形成
可以形成  和
和  两种化合物,试根据有关信息完成下列问题:
两种化合物,试根据有关信息完成下列问题: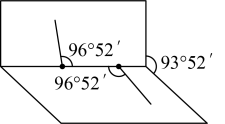
①
 内的
内的 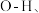 水分子间的范德华力和氢键,从强到弱依次为
水分子间的范德华力和氢键,从强到弱依次为②用球棍模型表示的水分子结构是 ;
A. 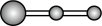 B.
B. 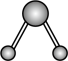 C.
C.  D.
D.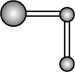
 可与
可与  形成
形成 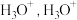 中的
中的 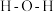 键角比
键角比  的键角
的键角(2)已知
 分子的结构如图所示:
分子的结构如图所示: 分子不是直线形的,两个氢原子犹如在半展开的书的两面上,两个氧原子在书脊位置上,书页夹角
分子不是直线形的,两个氢原子犹如在半展开的书的两面上,两个氧原子在书脊位置上,书页夹角 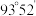 ,而两个
,而两个  键与
键与  键的夹角均为
键的夹角均为 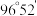 。
。请回答下列问题:
①
 子的电子式是
子的电子式是②
 分子是含有
分子是含有③
 能与水混溶,却不溶于
能与水混溶,却不溶于  试剂,请予以解释:
试剂,请予以解释:
您最近半年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】Ⅰ.金刚砂(SIC)是重要的工业制品,可由一以下反应制得: 。SiC的晶体结构与金刚石的相似,如图所示,其中C原子和Si原子的位置是交替的。回答下列问题。
。SiC的晶体结构与金刚石的相似,如图所示,其中C原子和Si原子的位置是交替的。回答下列问题。
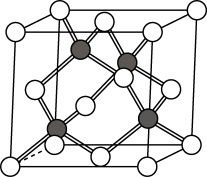
(1)X的化学式为___________
(2)写出基态Si原子的电子排布式___________ ,SiC中Si的化合价为___________
(3)SiC,金刚石,硅单质的熔点由高到低的顺序为___________
(4)X可与氧气反应生成Y,Y分子中中心原子的杂化类型为___________ ,键角为___________
Ⅱ. 晶体是一种性能良好的光学材料,其晶胞为立方体,棱长为0.446nm,晶胞中K、I、O分别位于顶点、体心、面心位置,如图所示。
晶体是一种性能良好的光学材料,其晶胞为立方体,棱长为0.446nm,晶胞中K、I、O分别位于顶点、体心、面心位置,如图所示。
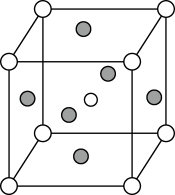
(5)与K原子紧邻的O原子有___________
(6)晶体中K原子与O原子的最短距离为___________ nm(保留三位小数)
 。SiC的晶体结构与金刚石的相似,如图所示,其中C原子和Si原子的位置是交替的。回答下列问题。
。SiC的晶体结构与金刚石的相似,如图所示,其中C原子和Si原子的位置是交替的。回答下列问题。
(1)X的化学式为
(2)写出基态Si原子的电子排布式
(3)SiC,金刚石,硅单质的熔点由高到低的顺序为
(4)X可与氧气反应生成Y,Y分子中中心原子的杂化类型为
Ⅱ.
 晶体是一种性能良好的光学材料,其晶胞为立方体,棱长为0.446nm,晶胞中K、I、O分别位于顶点、体心、面心位置,如图所示。
晶体是一种性能良好的光学材料,其晶胞为立方体,棱长为0.446nm,晶胞中K、I、O分别位于顶点、体心、面心位置,如图所示。
(5)与K原子紧邻的O原子有
(6)晶体中K原子与O原子的最短距离为
您最近半年使用:0次
【推荐1】氢能的存储是氢能应用的主要瓶颈,目前所采用或正在研究的主要储氢材料有:配位氢化物、富氢载体化合物、碳质材料、金属氢化物等。
(1)Ti(BH4)2是一种过渡元素硼氢化物储氢材料。
①Ti2+基态的电子排布式可表示为_______ 。
②BH 的空间构型是
的空间构型是_______ (用文字描述)。
(2)液氨是富氢物质,是氢能的理想载体,利用N2+3H2⇌2NH3实现储氢和输氢。下列说法正确的是_______。
(3)2008年,Yoon等人发现Ca与C60生成的Ca32C60能大量吸附H2分子。C60晶体易溶于苯、CS2,说明C60是_______ 分子(选填“极性”或“非极性”)。
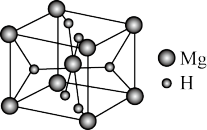
(4)MgH2是金属氢化物储氢材料,其晶胞结构如图所示,已知该晶体的密度为a g·cm-3,则晶胞的体积为_______ cm3[用a、NA表示(NA表示阿伏加德罗常数的数值)]。
(1)Ti(BH4)2是一种过渡元素硼氢化物储氢材料。
①Ti2+基态的电子排布式可表示为
②BH
 的空间构型是
的空间构型是(2)液氨是富氢物质,是氢能的理想载体,利用N2+3H2⇌2NH3实现储氢和输氢。下列说法正确的是_______。
| A.NH3分子中N原子采用sp3杂化 |
| B.相同压强时,NH3沸点比PH3高 |
| C.[Cu(NH3)4]2+中,N原子是配位原子 |
D.CN-的电子式为[∶C︙︙N∶]-,C60分子结构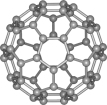 |
(4)MgH2是金属氢化物储氢材料,其晶胞结构如图所示,已知该晶体的密度为a g·cm-3,则晶胞的体积为

您最近半年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】氮的化合物应用广泛。
(1)Reineckesalt的结构如图所示:
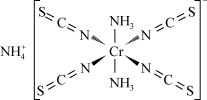
其中配位原子为_______ (填元素符号),阳离子的空间结构为_______ , 中碳原子杂化方式为
中碳原子杂化方式为_______ 。
(2)重铬酸铵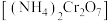 为桔黄色单斜结晶,常用作有机合成催化剂,
为桔黄色单斜结晶,常用作有机合成催化剂, 的结构如图。
的结构如图。
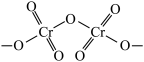
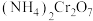 中N、O、
中N、O、 三种元素第一电离能由大到小的顺序是
三种元素第一电离能由大到小的顺序是_______ (填元素符号), 该物质中含σ键的数目为
该物质中含σ键的数目为_______  。
。
(3) 是
是 的一种配合物,
的一种配合物, 的结构为
的结构为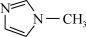 。
。 的某种衍生物与甘氨酸形成的离子化合物
的某种衍生物与甘氨酸形成的离子化合物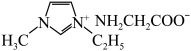 常温下为液态而非固态,原因是
常温下为液态而非固态,原因是_______ 。
(4)已知:多原子分子中,若原子都在同一平面上且这些原子有相互平行的p轨道,则p电子可在多个原子间运动,形成“离域 键”(或大
键”(或大 键)。大
键)。大 键可用
键可用 表示,其中m、n分别代表参与形成大
表示,其中m、n分别代表参与形成大 键的原子个数和电子数,如苯分子中大
键的原子个数和电子数,如苯分子中大 键表示为
键表示为 。
。
①下列微粒中存在“离域 键”的是
键”的是_______ 。
A. B.
B.
C. D.
D.
② 中阴离子
中阴离子 与
与 互为等电子体,均为直线型结构,
互为等电子体,均为直线型结构, 中的2个大
中的2个大 键可表示为
键可表示为_______ 。
(5)符号“ ”没有给出的信息是_______。
”没有给出的信息是_______。
(6)下列实验事实不能用氢键来解释的是_______。
(7)下列图像是 、
、 、
、 等离子晶体结构图或者是从其中分割出来的部分结构图。其中属于
等离子晶体结构图或者是从其中分割出来的部分结构图。其中属于 的晶体结构的图是
的晶体结构的图是
(8)键能的大小可以衡量化学键的强弱。下列说法中错误的是
(1)Reineckesalt的结构如图所示:

其中配位原子为
 中碳原子杂化方式为
中碳原子杂化方式为(2)重铬酸铵
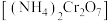 为桔黄色单斜结晶,常用作有机合成催化剂,
为桔黄色单斜结晶,常用作有机合成催化剂, 的结构如图。
的结构如图。
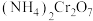 中N、O、
中N、O、 三种元素第一电离能由大到小的顺序是
三种元素第一电离能由大到小的顺序是 该物质中含σ键的数目为
该物质中含σ键的数目为 。
。(3)
 是
是 的一种配合物,
的一种配合物, 的结构为
的结构为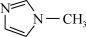 。
。 的某种衍生物与甘氨酸形成的离子化合物
的某种衍生物与甘氨酸形成的离子化合物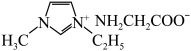 常温下为液态而非固态,原因是
常温下为液态而非固态,原因是(4)已知:多原子分子中,若原子都在同一平面上且这些原子有相互平行的p轨道,则p电子可在多个原子间运动,形成“离域
 键”(或大
键”(或大 键)。大
键)。大 键可用
键可用 表示,其中m、n分别代表参与形成大
表示,其中m、n分别代表参与形成大 键的原子个数和电子数,如苯分子中大
键的原子个数和电子数,如苯分子中大 键表示为
键表示为 。
。①下列微粒中存在“离域
 键”的是
键”的是A.
 B.
B.
C.
 D.
D.
②
 中阴离子
中阴离子 与
与 互为等电子体,均为直线型结构,
互为等电子体,均为直线型结构, 中的2个大
中的2个大 键可表示为
键可表示为(5)符号“
 ”没有给出的信息是_______。
”没有给出的信息是_______。| A.能层 | B.能级 |
| C.电子云在空间的伸展方向 | D.电子的自旋方向 |
A. 比 比 稳定 稳定 |
| B.乙醇能与水以任意比互溶 |
| C.邻羟基苯甲醛的沸点低于对羟基苯甲醛 |
| D.接近沸点的水蒸气的相对分子质量测量值大于18 |
 、
、 、
、 等离子晶体结构图或者是从其中分割出来的部分结构图。其中属于
等离子晶体结构图或者是从其中分割出来的部分结构图。其中属于 的晶体结构的图是
的晶体结构的图是A.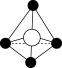 | B.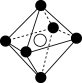 | C. | D.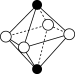 |
| 化学键 |  |  |  |  |  |  |
键能 | 460 | 360 | 436 | 431 | 176 | 347 |
A. 的熔点比 的熔点比 熔点低 熔点低 |
B. 的稳定性比 的稳定性比 稳定性高 稳定性高 |
C. 的键能大于 的键能大于 |
D.拆开 晶体硅中的化学键所吸收的能量为 晶体硅中的化学键所吸收的能量为 |
您最近半年使用:0次
【推荐3】黄铜矿(主要成分为CuFeS2)是一种天然矿石。中国在商代或更早就掌握了由它冶炼铜的技术。医药上,黄铜矿有促进骨折愈合的作用。请回答下列问题:
(1)基态Cu+比Cu2+稳定的原因是___ 。
(2)SO 的空间构型为
的空间构型为___ ,与SO 互为等电子体的离子是
互为等电子体的离子是___ (写出一种化学式即可)。
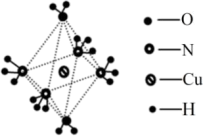
(3)图为某阳离子的结构,加热时该离子先失去的配位体是___ (填化学式),原因是___ 。
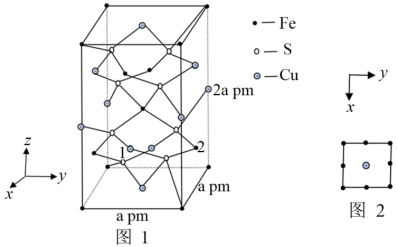
(4)四方晶系的CuFeS2晶胞结构如图1所示。
①CuFeS2中各元素电负性数值从小到大的顺序为___ ,晶胞中S原子的杂化方式为___ 。
②晶胞中Cu和Fe的投影位置如图2所示。设阿伏加德罗常数的值为NA,则该晶体的密度为___ g·cm-3。
③以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标,例如图1中原子1的坐标为( ,
, ,
, ),则原子2的坐标为
),则原子2的坐标为___ 。晶体中距离Fe最近的S有___ 个。
(1)基态Cu+比Cu2+稳定的原因是
(2)SO
 的空间构型为
的空间构型为 互为等电子体的离子是
互为等电子体的离子是(3)图为某阳离子的结构,加热时该离子先失去的配位体是

(4)四方晶系的CuFeS2晶胞结构如图1所示。
①CuFeS2中各元素电负性数值从小到大的顺序为
②晶胞中Cu和Fe的投影位置如图2所示。设阿伏加德罗常数的值为NA,则该晶体的密度为
③以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标,例如图1中原子1的坐标为(
 ,
, ,
, ),则原子2的坐标为
),则原子2的坐标为
您最近半年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐1】A.[物质结构与性质]
Cu2O广泛应用于太阳能电池领域。以CuSO4、NaOH和抗坏血酸为原料,可制备Cu₂O。
(1)Cu2+基态核外电子排布式为____ 。
(2) 的空间构型为
的空间构型为____ (用文字描述);Cu2+与OH−反应能生成[Cu(OH)4]2−,[Cu(OH)4]2−中的配位原子为____ (填元素符号)。
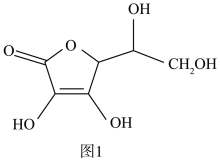
(3)抗坏血酸的分子结构如图1所示,分子中碳原子的轨道杂化类型为____ ;推测抗坏血酸在水中的溶解性:____ (填“难溶于水”或“易溶于水”)。
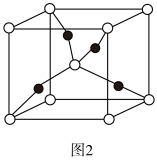
(4)一个Cu2O晶胞(见图2)中,Cu原子的数目为____ 。
Cu2O广泛应用于太阳能电池领域。以CuSO4、NaOH和抗坏血酸为原料,可制备Cu₂O。
(1)Cu2+基态核外电子排布式为
(2)
 的空间构型为
的空间构型为(3)抗坏血酸的分子结构如图1所示,分子中碳原子的轨道杂化类型为


(4)一个Cu2O晶胞(见图2)中,Cu原子的数目为
您最近半年使用:0次
【推荐2】我国科学家利用碲化锆(ZrTe2)和砷化镉(Cd3As2)为材料成功地验证了三维两字霍尔效应,并发现了金属—绝缘体的转换。回答下列问题:
(1)基态砷原子的价电子排布式为____ 。
(2)As与Ge、Se同周期且相邻,它们的第一电离能由大到小的顺序为____ (用元素符号表示)。
(3)与砷(As)同主族的N、P两种元素的氢化物水溶液的碱性:NH3>PH3原因是____ 。
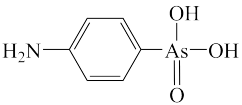
(4)含砷有机物“对氨基苯砷酸”的结构简式如图,砷原子轨道杂化类型为____ 。
(5)Cd2+与NH3形成的配离子[Cd(NH3)4]2+中,2个NH3被2个Cl-替代只得到1种结构,[Cd(NH3)4]2+的立体构型是____ ,1mol[Cd(NH3)4]2+含____ molσ键。
(1)基态砷原子的价电子排布式为
(2)As与Ge、Se同周期且相邻,它们的第一电离能由大到小的顺序为
(3)与砷(As)同主族的N、P两种元素的氢化物水溶液的碱性:NH3>PH3原因是
(4)含砷有机物“对氨基苯砷酸”的结构简式如图,砷原子轨道杂化类型为

(5)Cd2+与NH3形成的配离子[Cd(NH3)4]2+中,2个NH3被2个Cl-替代只得到1种结构,[Cd(NH3)4]2+的立体构型是
您最近半年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】Fe、Co、Ni是几种重要的金属元素。请回答下列问题。
(1)基态Co原子的价电子轨道表示式为___________ 。
(2) 常温下为无色液体,沸点为42.1℃,熔点为-19.3℃,难溶于水,易溶于有机溶剂。推测
常温下为无色液体,沸点为42.1℃,熔点为-19.3℃,难溶于水,易溶于有机溶剂。推测 是
是___________ 分子(填“极性”或“非极性”)。
(3)实验室常用KSCN溶液或苯酚(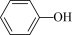 )检验
)检验 。第一电离能:N
。第一电离能:N___________ O(填“>”或“<”),KSCN的配位原子有___________ 。苯酚中碳原子和氧原子的杂化类型分别为___________ ;___________ 。
(4)配位化合物 中心原子Co的配位数为
中心原子Co的配位数为___________ ,配体为___________ 。
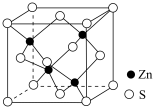
(5)ZnS在荧光体、光导体材料、涂料、颜料等行业中应用广泛。立方ZnS晶体结构如下图所示,S原子的配位数是___________ ,其晶胞边长为540.0pm,密度为___________ (列式并计算)。Zn:65 S:32
(1)基态Co原子的价电子轨道表示式为
(2)
 常温下为无色液体,沸点为42.1℃,熔点为-19.3℃,难溶于水,易溶于有机溶剂。推测
常温下为无色液体,沸点为42.1℃,熔点为-19.3℃,难溶于水,易溶于有机溶剂。推测 是
是(3)实验室常用KSCN溶液或苯酚(
 )检验
)检验 。第一电离能:N
。第一电离能:N(4)配位化合物
 中心原子Co的配位数为
中心原子Co的配位数为(5)ZnS在荧光体、光导体材料、涂料、颜料等行业中应用广泛。立方ZnS晶体结构如下图所示,S原子的配位数是

您最近半年使用:0次



