多硫化物Na2Sx与Na2O2在结构上有相似之处,在碱性条件下,Na2Sx与NaClO反应生成Na2SO4和NaCl。若反应物之间的物质的量比为1:13,则X应为
| A.5 | B.4 | C.3 | D.2 |
更新时间:2021-08-12 21:53:09
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】已知反应:Fe3++ClO-+X→FeO +Cl-+Y,下列说法错误的是
+Cl-+Y,下列说法错误的是
 +Cl-+Y,下列说法错误的是
+Cl-+Y,下列说法错误的是A.FeO 是氧化产物 是氧化产物 |
| B.Fe3+、ClO-的化学计量数之比(系数比)是3∶2 |
| C.配平后X是“10OH-” |
D.每生成1个FeO 就会有3个电子发生转移 就会有3个电子发生转移 |
您最近一年使用:0次
【推荐2】高铁酸钾(K2FeO4)是一种暗紫色固体,低温碱性条件下比较稳定。高铁酸钾微溶于浓KOH溶液,能溶于水,且能与水反应放出氧气,并生成Fe(OH)3胶体,常用作水处理剂。高铁酸钾有强氧化性,酸性条件下,其氧化性强于Cl2、KMnO4等。工业上湿法制备K2FeO4的流程如下:
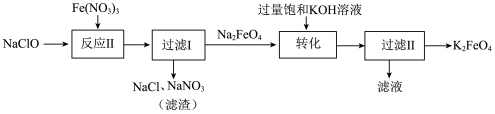
下列说法错误的是

下列说法错误的是
| A.过滤操作需要用到的玻璃仪器有普通漏斗、玻璃棒和烧杯 |
| B.K2FeO4与水反应,每生成1个O2转移4个电子 |
| C.将K2FeO4与盐酸混合使用,会降低其杀菌消毒的效果 |
| D.“反应Ⅰ”中,氧化剂和还原剂的个数之比为2:3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】某温度下,将 通入KOH溶液中,反应后得到KCl、KClO、
通入KOH溶液中,反应后得到KCl、KClO、 的混合液,经测定,
的混合液,经测定, 和
和 的物质的量之比为1∶3,则
的物质的量之比为1∶3,则 与KOH溶液反应时,被还原的氯原子与被氧化的氯原子的物质的量之比为( )
与KOH溶液反应时,被还原的氯原子与被氧化的氯原子的物质的量之比为( )
 通入KOH溶液中,反应后得到KCl、KClO、
通入KOH溶液中,反应后得到KCl、KClO、 的混合液,经测定,
的混合液,经测定, 和
和 的物质的量之比为1∶3,则
的物质的量之比为1∶3,则 与KOH溶液反应时,被还原的氯原子与被氧化的氯原子的物质的量之比为( )
与KOH溶液反应时,被还原的氯原子与被氧化的氯原子的物质的量之比为( )| A.2∶5 | B.11∶3 | C.3∶1 | D.4∶1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】将一定量的铁和铜组成的混合物加入稀硝酸中,金属完全溶解(假设反应中还原产物只有 )。向反应后的溶液中加入
)。向反应后的溶液中加入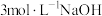 溶液至沉淀完全,测得生成沉淀的质量比原合金的质量增加
溶液至沉淀完全,测得生成沉淀的质量比原合金的质量增加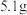 。下列叙述不正确的是
。下列叙述不正确的是
 )。向反应后的溶液中加入
)。向反应后的溶液中加入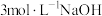 溶液至沉淀完全,测得生成沉淀的质量比原合金的质量增加
溶液至沉淀完全,测得生成沉淀的质量比原合金的质量增加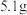 。下列叙述不正确的是
。下列叙述不正确的是A.当生成的沉淀量达到最大时,消耗 溶液的体积V≥100mL 溶液的体积V≥100mL |
B.当金属全部溶解时收集到 气体的体积折算成标准状况为 气体的体积折算成标准状况为 |
C.参加反应的金属的总质量 |
D.当金属全部溶解时,参加反应的硝酸的物质的量可能是 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】向lmol炽热的Cu2S中通入足量的水蒸气,充分反应后生成2molH2,则Cu2S应转化为
| A.Cu和SO2 | B.Cu和S | C.CuO和SO2 | D.Cu2O和S |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】水溶液中φ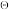 (MnO
(MnO /Mn2+)的代数值大于 φ
/Mn2+)的代数值大于 φ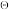 (H2S/S),下 列化学方程式配平正确的是
(H2S/S),下 列化学方程式配平正确的是
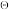 (MnO
(MnO /Mn2+)的代数值大于 φ
/Mn2+)的代数值大于 φ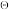 (H2S/S),下 列化学方程式配平正确的是
(H2S/S),下 列化学方程式配平正确的是| A.2KMnO4+ 11H2S + 5H2SO4= K2SO4+ 2MnSO4+ 13S↓+ 16H2O |
| B.2KMnO4+ 8H2S + 4H2SO4=K2SO4+ 2MnSO4+9S↓+ 12H2O |
| C.2KMnO4+ 5H2S +3H2SO4= K2SO4+2MnSO4+ S↓+4H2O |
| D.2KMnO4+ 5H2S + 3H2SO4= K2SO4+ 2MnSO4+ 5S↓+ 8H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】某同学进行如下实验:
已知: i.H2O2 H+ + HO
H+ + HO HO
HO
 H++O
H++O
ii.BaO2是一种白色难溶于水的固体
下列说法不合理的是
| 序号 | 实验① | 实验② | 实验③ | 实验④ | 实验⑤ |
| 方案 | BaCl2溶液
| BaCl2溶液
| BaCl2溶液
| 先加MnO2粉末,后加酸性 KMnO4溶液 | 稀H2SO4
|
| 现象 | 出现白色沉淀 | 无明显现象 | 出现白色沉淀 | 产生大量气泡,高锰酸钾溶液不褪色 | 出现白色沉淀 |
 H+ + HO
H+ + HO HO
HO
 H++O
H++O
ii.BaO2是一种白色难溶于水的固体
下列说法不合理的是
| A.实验①和②说明BaO2可溶于酸 |
| B.实验①和③得到的沉淀组成一样 |
| C.实验⑤的白色沉淀经检验为BaSO4,说明溶解度BaO2> BaSO4 |
| D.可用BaCl2、MnO2、H2O检验长期放置的Na2O2中是否含有Na2CO3 |
您最近一年使用:0次

 获得钼(
获得钼( )的反应原理为:
)的反应原理为: 。在恒容密闭容器中进行该反应,平衡时正、逆反应平衡常数与温度的关系如图所示。下列说法正确的是
。在恒容密闭容器中进行该反应,平衡时正、逆反应平衡常数与温度的关系如图所示。下列说法正确的是
 下达平衡时,
下达平衡时,
 ,转移电子的数目约为
,转移电子的数目约为
 ,且这三种离子的数目之比为10:3:1,则原混合气体中Cl2和HCl数目之比为
,且这三种离子的数目之比为10:3:1,则原混合气体中Cl2和HCl数目之比为






