Cl2是一种有毒气体,如果泄漏会造成严重的危害。
(1)已知:3Cl2+8NH3=6NH4Cl+N2,化工厂可用浓氨水来检验Cl2是否泄漏。当有少量Cl2泄漏,可以观察到的现象是___________ ;NH4Cl的电离方程式为___________ 。
(2)喷射石灰乳等碱性物质可以减轻少量Cl2泄漏造成的危害。Cl2和石灰乳反应的化学方程式是___________ 。
(3)实验室制备氯气的化学方程式为___________ 。
(4)实验室常用烧碱溶液吸收Cl2。若将Cl2通入热的烧碱溶液中,可以得到NaCl、NaClO和NaClO3的混合液。当NaCl和NaClO3的物质的量之比为8︰1时,混合液中NaClO和NaClO3的物质的量之比为___________ 。
(1)已知:3Cl2+8NH3=6NH4Cl+N2,化工厂可用浓氨水来检验Cl2是否泄漏。当有少量Cl2泄漏,可以观察到的现象是
(2)喷射石灰乳等碱性物质可以减轻少量Cl2泄漏造成的危害。Cl2和石灰乳反应的化学方程式是
(3)实验室制备氯气的化学方程式为
(4)实验室常用烧碱溶液吸收Cl2。若将Cl2通入热的烧碱溶液中,可以得到NaCl、NaClO和NaClO3的混合液。当NaCl和NaClO3的物质的量之比为8︰1时,混合液中NaClO和NaClO3的物质的量之比为
更新时间:2021-08-22 11:52:13
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】按要求填空。
(1)已知甲、乙、丙三种物质分别由H、C、Na、O、Cl、Fe、Al元素中的一种或几种组成。
①若甲物质为碱性氧化物,则甲的化学式为_______ (写2种)。
②若乙物质可作为呼吸面具中氧气的来源,则乙物质的电子式_______ ,其供氧原理是_______ (用化学方程式表示)。
③丙物质是两性氢氧化物,它能与强碱溶液反应,则反应的离子方程式为_______ 。
(2)在横线上填入合适的化学式:_______ +2H+=CO2↑+H2O+Ba2+;并判断其所属化合物类型_______ (填写“离子化合物”或“共价化合物”)。
(3)写出氯气与水反应的化学方程式,并用双线桥法标出电于转移的方向和数目:_______ 。
(4)酸性高锰酸钾溶液具有强氧化性。某反应中参加反应的离子为MnO 、H+和一种未知离子,产物为Fe3+、Mn2+和H2O,该反应的离子方程式为
、H+和一种未知离子,产物为Fe3+、Mn2+和H2O,该反应的离子方程式为_______ 。
(1)已知甲、乙、丙三种物质分别由H、C、Na、O、Cl、Fe、Al元素中的一种或几种组成。
①若甲物质为碱性氧化物,则甲的化学式为
②若乙物质可作为呼吸面具中氧气的来源,则乙物质的电子式
③丙物质是两性氢氧化物,它能与强碱溶液反应,则反应的离子方程式为
(2)在横线上填入合适的化学式:
(3)写出氯气与水反应的化学方程式,并用双线桥法标出电于转移的方向和数目:
(4)酸性高锰酸钾溶液具有强氧化性。某反应中参加反应的离子为MnO
 、H+和一种未知离子,产物为Fe3+、Mn2+和H2O,该反应的离子方程式为
、H+和一种未知离子,产物为Fe3+、Mn2+和H2O,该反应的离子方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】甲、乙、丙均为化合物,其中甲为淡黄色固体,乙在常温下为无色无味液体,丙为常见的无色无味气体,可使澄清石灰水变浑浊。它们有如图所示的转化关系,反应的量均为充足。(生成物中有水生成的,框图中没有表示出来),已知D为黄绿色气体,按要求回答下列问题:
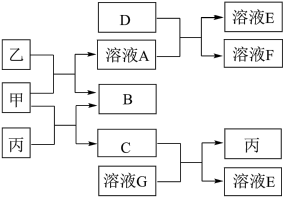
(1)F为______ (填化学式),G的溶质为_______ (填化学式)。
(2)若有3.9g甲与4.4g丙完全反应,则固体质量增加_____ g。
(3)C与溶液G反应生成丙的离子方程式为:________ 。
(4)甲与乙反应的化学方程式为:_______ 。
(5)D能使湿润的有色布条褪色,其褪色原因是_______ (结合离子方程式描述)。

(1)F为
(2)若有3.9g甲与4.4g丙完全反应,则固体质量增加
(3)C与溶液G反应生成丙的离子方程式为:
(4)甲与乙反应的化学方程式为:
(5)D能使湿润的有色布条褪色,其褪色原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】Ⅰ.A~D是四种烃分子的球棍模型(如图)。
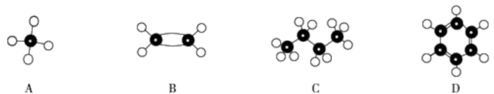
(1)D和液溴反应的化学方程式是:___ 。
(2)A、B、C、D四种烃中属于同系物的是___ (填序号)。
(3)“84”消毒液在抗击新冠肺炎中经常用到,在常温下,将氯气通入氢氧化钠溶液中制备消毒液,请写出该反应的离子方程式:___ 。
(4)实验室通常用浓盐酸与二氧化锰加热制备氯气,请写出反应的化学方程式:___ 。

(1)D和液溴反应的化学方程式是:
(2)A、B、C、D四种烃中属于同系物的是
(3)“84”消毒液在抗击新冠肺炎中经常用到,在常温下,将氯气通入氢氧化钠溶液中制备消毒液,请写出该反应的离子方程式:
(4)实验室通常用浓盐酸与二氧化锰加热制备氯气,请写出反应的化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】完成下列问题
(1)完成下列反应的离子方程式,注意难溶、气体、难电离微粒的书写形式。
①氧化镁溶于稀硫酸:___________ 。
②向AlCl3溶液中滴加过量的氨水:___________ 。
③小苏打溶液与乙酸溶液混合:___________ 。
④向NaHSO3溶液中加入过量NaHSO4溶液:___________ 。
(2)按要求完成下列反应的离子方程式,注意微溶物质、NH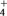 与碱反应的条件。
与碱反应的条件。
①向澄清石灰水中加入稀盐酸:___________ 。
②石灰乳与Na2CO3溶液反应:___________ 。
③Na2SO4溶液与AgNO3溶液混合:___________ 。
④NH4Cl与NaOH两种稀溶液混合:___________ 。
(3)完成下列反应的离子方程式,注意单质、氧化物、浓盐酸、浓硝酸、浓硫酸的书写形式。
①过氧化钠溶于水:___________ 。
②FeCl3溶液腐蚀铜箔:___________ 。
③用MnO2与浓盐酸共热制Cl2:___________ 。
④铜与浓硝酸反应:___________ 。
⑤硫化钠溶液与浓硫酸反应:___________ 。
(4)多重反应。完成下列反应的离子方程式。
①Ba(OH)2+H2SO4:___________ 。
②CuSO4+Ba(OH)2:___________ 。
③向HI溶液中加入少量Fe(OH)3:___________ 。
④FeO溶于稀硝酸中:___________ 。
(1)完成下列反应的离子方程式,注意难溶、气体、难电离微粒的书写形式。
①氧化镁溶于稀硫酸:
②向AlCl3溶液中滴加过量的氨水:
③小苏打溶液与乙酸溶液混合:
④向NaHSO3溶液中加入过量NaHSO4溶液:
(2)按要求完成下列反应的离子方程式,注意微溶物质、NH
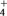 与碱反应的条件。
与碱反应的条件。①向澄清石灰水中加入稀盐酸:
②石灰乳与Na2CO3溶液反应:
③Na2SO4溶液与AgNO3溶液混合:
④NH4Cl与NaOH两种稀溶液混合:
(3)完成下列反应的离子方程式,注意单质、氧化物、浓盐酸、浓硝酸、浓硫酸的书写形式。
①过氧化钠溶于水:
②FeCl3溶液腐蚀铜箔:
③用MnO2与浓盐酸共热制Cl2:
④铜与浓硝酸反应:
⑤硫化钠溶液与浓硫酸反应:
(4)多重反应。完成下列反应的离子方程式。
①Ba(OH)2+H2SO4:
②CuSO4+Ba(OH)2:
③向HI溶液中加入少量Fe(OH)3:
④FeO溶于稀硝酸中:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】按要求回答下列问题:
(1)实验室制取氯气反应的离子方程式为_______
(2)写出铁与水蒸气反应方程式:_______
(3)某反应为: ,用单线桥表示出该反应中电子转移的方向和数目
,用单线桥表示出该反应中电子转移的方向和数目_______ 。
(4) 中各原子均满足8电子稳定结构。写出
中各原子均满足8电子稳定结构。写出 的电子式
的电子式_______
(5)请解释 的熔沸点高于
的熔沸点高于 的原因
的原因_______
(1)实验室制取氯气反应的离子方程式为
(2)写出铁与水蒸气反应方程式:
(3)某反应为:
 ,用单线桥表示出该反应中电子转移的方向和数目
,用单线桥表示出该反应中电子转移的方向和数目(4)
 中各原子均满足8电子稳定结构。写出
中各原子均满足8电子稳定结构。写出 的电子式
的电子式(5)请解释
 的熔沸点高于
的熔沸点高于 的原因
的原因
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】按要求填空:
(1)实验室用加热二氧化锰和浓盐酸制氯气,离子方程式为____________________ 。若生成标准状况下2.24 L Cl2,则被氧化的HCl的物质的量为 _______________ 。
(2)向淀粉碘化钾溶液中通入少量氯气,立即会看到溶液变蓝色,反应的离子方程式为_______________________________________ 。
(3)①乙醇 ②MgCl2晶体 ③蔗糖 ④铜 ⑤食盐水 ⑥BaSO4 ⑦次氯酸
以上物质中属于电解质的是(填序号)_____________________________________ 。
(4)在甲、乙两个烧杯中,分别含有下列离子中的三种:Cu2+、Na+、H+、SO42-、CO32-、OH-。已知甲烧杯中的溶液呈蓝色,则乙烧杯中的溶液中大量存在的离子是_____________________ 。
(1)实验室用加热二氧化锰和浓盐酸制氯气,离子方程式为
(2)向淀粉碘化钾溶液中通入少量氯气,立即会看到溶液变蓝色,反应的离子方程式为
(3)①乙醇 ②MgCl2晶体 ③蔗糖 ④铜 ⑤食盐水 ⑥BaSO4 ⑦次氯酸
以上物质中属于电解质的是(填序号)
(4)在甲、乙两个烧杯中,分别含有下列离子中的三种:Cu2+、Na+、H+、SO42-、CO32-、OH-。已知甲烧杯中的溶液呈蓝色,则乙烧杯中的溶液中大量存在的离子是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】(1)写出制取硝基苯的化学反应方程式_________________________________ ;
(2)写出镁铝氢氧化钠原电池的负极电极反应式___________________________ ;
(3)氯气是重要的化工原料,可以用来制备很多化工产品,比如可以制备净水剂高铁酸钾(K2FeO4),写出碱性条件下,由氯化铁制备高铁酸钾的离子方程式___________ ;
写出工业制漂白粉的化学反应方程式__________________________ 。
(2)写出镁铝氢氧化钠原电池的负极电极反应式
(3)氯气是重要的化工原料,可以用来制备很多化工产品,比如可以制备净水剂高铁酸钾(K2FeO4),写出碱性条件下,由氯化铁制备高铁酸钾的离子方程式
写出工业制漂白粉的化学反应方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】氯水及氯的许多化合物是高效广谱的消毒剂,同时又是生产中重要的化工原料,根据所学知识,回答下列问题:
(1)新制的氯水呈淡黄色,向氯水中滴入几滴 溶液,现象是
溶液,现象是_______ ,说明新制氯水中有_______ 存在。
(2)某品牌的“84”消毒液含NaClO的质量分数约为6%,NaClO溶液能够杀灭新冠病毒的原因是具有_______ (填“强氧化性”或“强还原性”);为了较长时间保持NaClO溶液的杀菌能力,NaClO溶液应密闭避光保存,原因是_______ 。生活中,若不小心将“84”消毒液与洁厕剂(含有盐酸)混合,易生成_______ 气体(填化学式),能使人中毒。
(3)近些年来,科学家提出使用 对自来水进行消毒。以
对自来水进行消毒。以 和稀盐酸为原料可制备
和稀盐酸为原料可制备 ,写出该反应的化学方程式:
,写出该反应的化学方程式:_______ ,在上述过程中被氧化和被还原的物质的物质的量之比为_______ 。
(1)新制的氯水呈淡黄色,向氯水中滴入几滴
 溶液,现象是
溶液,现象是(2)某品牌的“84”消毒液含NaClO的质量分数约为6%,NaClO溶液能够杀灭新冠病毒的原因是具有
(3)近些年来,科学家提出使用
 对自来水进行消毒。以
对自来水进行消毒。以 和稀盐酸为原料可制备
和稀盐酸为原料可制备 ,写出该反应的化学方程式:
,写出该反应的化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】某同学在复习元素化合物的性质时,做了如下学习笔记,请你一起完成。
(1)常温下将______ 通入到NaOH溶液中,可获得______ 为有效成分的漂白液(填化学式);
(2)NaHCO3俗名是______ ,常温时,NaHCO3的溶解度______ Na2CO3(填“大于”或“小于”);氯气的颜色为__________ ;由氯的原子结构示意图推测,氯气具有很强的______ 性。为了证明推测是否正确,进行如下实验:
I:将红热的铁丝伸入盛满氯气的集气瓶,观察铁丝在氯气中燃烧,有大量棕褐色烟。该反应的化学方程式是_________________ 。
II:在空气中点燃H2,然后将导管缓缓伸入盛满氯气的集气瓶,可观察到H2在氯气中安静燃烧,产生______ 色的火焰,瓶口有白雾的现象。
(1)常温下将
(2)NaHCO3俗名是
I:将红热的铁丝伸入盛满氯气的集气瓶,观察铁丝在氯气中燃烧,有大量棕褐色烟。该反应的化学方程式是
II:在空气中点燃H2,然后将导管缓缓伸入盛满氯气的集气瓶,可观察到H2在氯气中安静燃烧,产生
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病暴发的有效方法之一。漂白粉是常用的消毒剂。
(1)工业上将氯气通入石灰乳 中制取漂白粉,化学方程式为
中制取漂白粉,化学方程式为____________________________ 。
(2)漂白粉溶于水后,受空气中的 作用,即产生有漂白、杀菌作用的次氯酸,化学方程式为
作用,即产生有漂白、杀菌作用的次氯酸,化学方程式为____________________________________ 。
(3)已知浓盐酸和次氯酸钙能发生如下反应: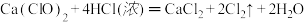 。用贮存很久的漂白粉与浓盐酸制得的氯气中,可能含有的杂质气体是
。用贮存很久的漂白粉与浓盐酸制得的氯气中,可能含有的杂质气体是___________ (填序号)。
① ②
② ③
③ ④
④
A.①②③ B.②③④ C.②③ D.①④
(1)工业上将氯气通入石灰乳
 中制取漂白粉,化学方程式为
中制取漂白粉,化学方程式为(2)漂白粉溶于水后,受空气中的
 作用,即产生有漂白、杀菌作用的次氯酸,化学方程式为
作用,即产生有漂白、杀菌作用的次氯酸,化学方程式为(3)已知浓盐酸和次氯酸钙能发生如下反应:
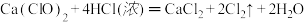 。用贮存很久的漂白粉与浓盐酸制得的氯气中,可能含有的杂质气体是
。用贮存很久的漂白粉与浓盐酸制得的氯气中,可能含有的杂质气体是①
 ②
② ③
③ ④
④
A.①②③ B.②③④ C.②③ D.①④
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】按要求写出下列方程式。
(1)实验室(舍勒法)制氯气的离子方程式:___________ 。
(2)碳酸钙溶于醋酸的离子方程式:___________ 。
(3) 胶体制备的离子方程式:
胶体制备的离子方程式:___________ 。
(4)工业制漂白粉的化学方程式:___________ 。
(5)向 溶液滴加
溶液滴加 溶液至
溶液至 时的离子方程式:
时的离子方程式:___________ 。
(1)实验室(舍勒法)制氯气的离子方程式:
(2)碳酸钙溶于醋酸的离子方程式:
(3)
 胶体制备的离子方程式:
胶体制备的离子方程式:(4)工业制漂白粉的化学方程式:
(5)向
 溶液滴加
溶液滴加 溶液至
溶液至 时的离子方程式:
时的离子方程式:
您最近一年使用:0次



