ZnSe是一种光电性能优异的II~VI族半导体材料,人们开发出了多种制备ZnSe纳米粒子的方法。某研究小组用如下方法制备了ZnSe纳米粒子。
①将1mmol的Zn(NO3)2·6H2O溶于去离子水中形成无色澄清溶液,往该溶液中加入1mmolSeO2,超声完全溶解后形成无色澄清溶液;
②再加入过量的水合肼(N2H4·H2O),超声几分钟后将溶液转移到内衬聚四氟乙烯套的不锈钢高压反应釜中,将高压反应釜拧紧密封后放在160°C的恒温干燥箱中保温12小时(已知肼有强还原性,Se在碱性条件下可发生岐化反应);
③反应结束后自然冷却至室温,得到淡黄色沉淀,将产物用蒸馏水和无水乙醇洗涤数次,干燥后得到产物。将产物用X-射线粉末衍射仪(XRD)和X射线能谱仪进行物相和成分分析,发现其Zn和Se的原子个数比接近1:1。
(1)写出过程①中的化学方程式:_______
(2)写出过程②中的离子方程式:_______
(3)产物样品的红外光谱分析结果如图1所示,该谱图反映出产物有明显的N-H、N-N吸收峰。这是因为产物中可能含有:_______ 。
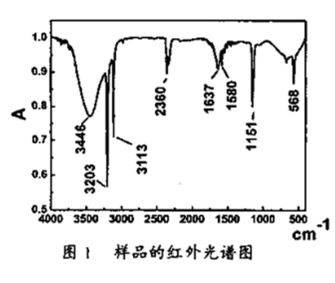
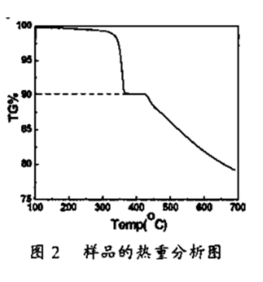
(4)产物样品的热重(重量-温度关系图)分析结果如图2所示,根据图1和图2提供的信息,推测产物的化学式可能为:_______ 。
①将1mmol的Zn(NO3)2·6H2O溶于去离子水中形成无色澄清溶液,往该溶液中加入1mmolSeO2,超声完全溶解后形成无色澄清溶液;
②再加入过量的水合肼(N2H4·H2O),超声几分钟后将溶液转移到内衬聚四氟乙烯套的不锈钢高压反应釜中,将高压反应釜拧紧密封后放在160°C的恒温干燥箱中保温12小时(已知肼有强还原性,Se在碱性条件下可发生岐化反应);
③反应结束后自然冷却至室温,得到淡黄色沉淀,将产物用蒸馏水和无水乙醇洗涤数次,干燥后得到产物。将产物用X-射线粉末衍射仪(XRD)和X射线能谱仪进行物相和成分分析,发现其Zn和Se的原子个数比接近1:1。
(1)写出过程①中的化学方程式:
(2)写出过程②中的离子方程式:
(3)产物样品的红外光谱分析结果如图1所示,该谱图反映出产物有明显的N-H、N-N吸收峰。这是因为产物中可能含有:

(4)产物样品的热重(重量-温度关系图)分析结果如图2所示,根据图1和图2提供的信息,推测产物的化学式可能为:

更新时间:2021-08-24 10:17:19
|
相似题推荐
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】黄铜矿主要成分为 ,某研究团队利用氧化亚铁硫杆菌溶浸,通过系列操作可获得铜和硫酸铁铵晶体。工艺流程如下:
,某研究团队利用氧化亚铁硫杆菌溶浸,通过系列操作可获得铜和硫酸铁铵晶体。工艺流程如下:
(1)“溶浸”时,需要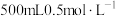 硫酸溶液,在配制硫酸溶液时:所需质量分数为98%、密度为
硫酸溶液,在配制硫酸溶液时:所需质量分数为98%、密度为 的浓硫酸的体积为
的浓硫酸的体积为______ mL(计算结果保留一位小数),“溶浸”时被氧化的元素为_______ (填元素符号)。
(2)“分离Cu”时,Fe与 反应的离子方程式为
反应的离子方程式为________ ,该过程中分离出Fe、Cu的操作名称为_______ 。
(3)“氧化”时,温度不能太高,原因是________ ,反应过程中,参加反应的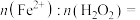
______ 。
(4)硫酸铁铵晶体[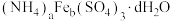 ]组成的测定
]组成的测定
步骤1:准确称取质量为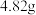 固体在酸性条件下溶于水配成
固体在酸性条件下溶于水配成 溶液A;
溶液A;
步骤2:取 溶液A,加入足量的
溶液A,加入足量的 溶液,过滤得
溶液,过滤得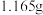 沉淀;
沉淀;
步骤3:取 溶液A,加入足量氢氧化钠溶液,过滤,洗涤并灼烧得
溶液A,加入足量氢氧化钠溶液,过滤,洗涤并灼烧得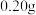 固体。
固体。
通过上述步骤,计算确定该晶体的化学式为___________ 。
 ,某研究团队利用氧化亚铁硫杆菌溶浸,通过系列操作可获得铜和硫酸铁铵晶体。工艺流程如下:
,某研究团队利用氧化亚铁硫杆菌溶浸,通过系列操作可获得铜和硫酸铁铵晶体。工艺流程如下: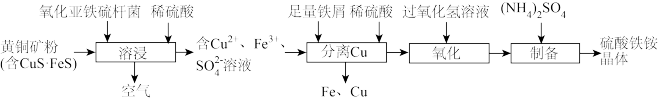
(1)“溶浸”时,需要
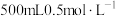 硫酸溶液,在配制硫酸溶液时:所需质量分数为98%、密度为
硫酸溶液,在配制硫酸溶液时:所需质量分数为98%、密度为 的浓硫酸的体积为
的浓硫酸的体积为(2)“分离Cu”时,Fe与
 反应的离子方程式为
反应的离子方程式为(3)“氧化”时,温度不能太高,原因是
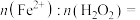
(4)硫酸铁铵晶体[
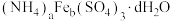 ]组成的测定
]组成的测定步骤1:准确称取质量为
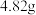 固体在酸性条件下溶于水配成
固体在酸性条件下溶于水配成 溶液A;
溶液A;步骤2:取
 溶液A,加入足量的
溶液A,加入足量的 溶液,过滤得
溶液,过滤得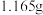 沉淀;
沉淀;步骤3:取
 溶液A,加入足量氢氧化钠溶液,过滤,洗涤并灼烧得
溶液A,加入足量氢氧化钠溶液,过滤,洗涤并灼烧得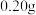 固体。
固体。通过上述步骤,计算确定该晶体的化学式为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐2】现有A、B、C、D、E、F六种物质的溶液,分别为NH3·H2O、NaHSO4、AlCl3、AgNO3、NaAlO2、NaOH中的一种,已知:
①将A溶液逐滴滴加到B溶液中至过量,先出现沉淀,后沉淀溶解;
②将C溶液逐滴滴加到D溶液中至过量,先出现沉淀,后沉淀溶解;
③将E溶液逐滴滴加到F溶液中至过量,先出现沉淀,后沉淀溶解;
④在①和③的反应中出现的沉淀是同一种物质;
⑤A、D、F三种溶液呈酸性。
请回答:
(1)写出下列化学式:A_____ ;D_____ ;E_____ 。
(2)过量A溶液与B溶液反应的离子方程式为________________ ;
将C溶液逐滴滴加到F溶液中至过量,此过程中反应的离子方程式为______________ 。
(3)若A、C的混合溶液呈中性,则该溶液中所有离子的浓度的大小关系为_________________ 。
①将A溶液逐滴滴加到B溶液中至过量,先出现沉淀,后沉淀溶解;
②将C溶液逐滴滴加到D溶液中至过量,先出现沉淀,后沉淀溶解;
③将E溶液逐滴滴加到F溶液中至过量,先出现沉淀,后沉淀溶解;
④在①和③的反应中出现的沉淀是同一种物质;
⑤A、D、F三种溶液呈酸性。
请回答:
(1)写出下列化学式:A
(2)过量A溶液与B溶液反应的离子方程式为
将C溶液逐滴滴加到F溶液中至过量,此过程中反应的离子方程式为
(3)若A、C的混合溶液呈中性,则该溶液中所有离子的浓度的大小关系为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
【推荐3】A、B、C、D为四种可溶性的盐,它们的阳离子分别可能是Ba2+、Ag+、Na+、Cu2+中的某一种,阴离子分别可能是 、
、 、Cl−、
、Cl−、 中的一种。(离子在物质中不重复出现)
中的一种。(离子在物质中不重复出现)
①若把四种盐分别溶于盛有蒸馏水的四支试管中,只有C盐的溶液呈蓝色;
②若向①的四支试管中分别加入盐酸,B盐的溶液有沉淀生成,D盐的溶液有无色无味的气体逸出。
根据①②实验事实可推断:
(1)A的化学式为____________ ,B的化学式为____________ 。
(2)写出少量盐酸与D反应的离子方程式:____________ 。
(3)写出C与Ba(OH)2溶液反应的离子方程式:________________________ 。
(4)C溶液中阴离子的检验方法是_____________________________ 。
 、
、 、Cl−、
、Cl−、 中的一种。(离子在物质中不重复出现)
中的一种。(离子在物质中不重复出现)①若把四种盐分别溶于盛有蒸馏水的四支试管中,只有C盐的溶液呈蓝色;
②若向①的四支试管中分别加入盐酸,B盐的溶液有沉淀生成,D盐的溶液有无色无味的气体逸出。
根据①②实验事实可推断:
(1)A的化学式为
(2)写出少量盐酸与D反应的离子方程式:
(3)写出C与Ba(OH)2溶液反应的离子方程式:
(4)C溶液中阴离子的检验方法是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐1】水杨酸异戊酯( ,摩尔质量为208g/mol)是一种具有较高应用价值的化工产品,在香精、医药等领域有广泛的应用。制备水杨酸异戊酯实验步骤如下:
,摩尔质量为208g/mol)是一种具有较高应用价值的化工产品,在香精、医药等领域有广泛的应用。制备水杨酸异戊酯实验步骤如下:
②按照下图搭建反应装置,在145~155℃油浴下加热回流至不再有水生成。
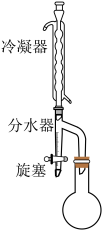
④干燥、减压蒸馏有机层,收集到31.2g产物。
⑤用红外光谱仪和核磁共振仪对产物进行表征。
已知:
①环己烯(沸点83℃)可与水形成沸点为70℃的共沸物。
②沸点:水杨酸211℃、异戊醇131℃、环己烯83℃、水杨酸异戊酯282℃。
回答以下问题:
(1)反应中浓硫酸的作用是吸水剂和
(2)写出制备水杨酸异戊酯的化学方程式
(3)步骤②中表明反应中不再有水生成的现象是
(4)洗涤反应液时需要使用的主要仪器是
(5)步骤③中NaHCO3溶液的作用是
(6)本次实验的产率为
(7)红外光谱图中可获得产物信息包括
a.产物中碳氧双键键长 b.产物相对分子质量
c.产物中含有酯基结构 d.产物中氧元素质量分数
您最近一年使用:0次
解答题-有机推断题
|
较难
(0.4)
解题方法
【推荐2】某有机化合物A经李比希法测得其中含碳元素为70.6%、含氢元素为5.9%,其余为氧元素。现用下列方法测定该有机化合物的相对分子质量和确定分子结构。
方法一:用质谱法分析得知A的质谱图如图所示。
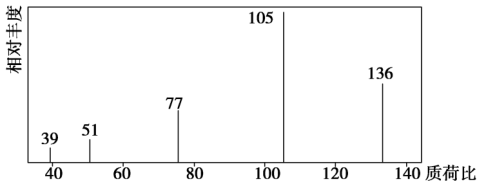
方法二:核磁共振仪测出A的核磁共振氢谱如图所示
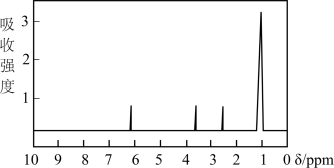
方法三:利用红外光谱仪测得A分子的红外光谱,如图所示。
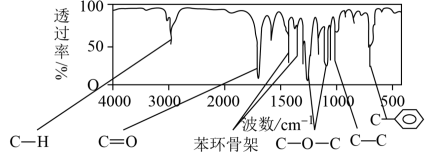
已知:A分子中苯环上只有一个取代基,试回答下列问题。
(1)A的相对分子质量是___________ 。其有___________ 种化学环境不同的氢原子。
(2)A的分子式为___________ 。
(3)该有机物中含有的官能团是___________ 。
(4)A的分子中只含一个甲基的直接依据是___________ (填字母)。
a.A的相对分子质量 b.A的分子式
c.A的核磁共振氢谱图 d.A分子的红外光谱图
(5)A的结构简式为___________ 。
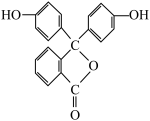
(6)酚酞是一种常见指示剂,结构如下图所示,该分子的分子式为___________ ,分子中最多有___________ 个原子共平面。
方法一:用质谱法分析得知A的质谱图如图所示。

方法二:核磁共振仪测出A的核磁共振氢谱如图所示

方法三:利用红外光谱仪测得A分子的红外光谱,如图所示。

已知:A分子中苯环上只有一个取代基,试回答下列问题。
(1)A的相对分子质量是
(2)A的分子式为
(3)该有机物中含有的官能团是
(4)A的分子中只含一个甲基的直接依据是
a.A的相对分子质量 b.A的分子式
c.A的核磁共振氢谱图 d.A分子的红外光谱图
(5)A的结构简式为
(6)酚酞是一种常见指示剂,结构如下图所示,该分子的分子式为

您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐3】纳米TiO2在涂料、光催化、化妆品等领域有着极其广泛的应用。
制备纳米TiO2的方法之一是TiCl4水解生成TiO2·xH2O,经过滤、水洗除去其中的Cl-,再烘干、焙烧除去水分得到粉体TiO2。
用现代分析仪器测定TiO2粒子的大小;用氧化还原滴定法测定TiO2的质量分数:一定条件下,将TiO2溶解并还原为Ti3+,再以KSCN溶液作指示剂,用NH4Fe(SO4)2标准溶液滴定Ti3+至全部生成Ti4+。
请回答下列问题:
(1)TiCl4水解生成TiO2·xH2O的化学方程式为:____________________________ 。
(2)检验TiO2·xH2O中Cl-是否被除净的方法是:____________________________ 。
(3)可用于测定TiO2粒子大小的方法是____________________ (填字母代号)。
a.核磁共振法 b.红外光谱法 c.质谱法 d.透射电子显微镜法
(4)配制NH4Fe(SO4)2标准溶液时,使用的仪器除天平、药匙、玻璃棒、烧杯、量筒外,还需要下图中的_________ (填字母代号)。

(5)滴定时,称取TiO2(摩尔质量为Mg·mol-1)试样wg,消耗cmol·L-1NH4Fe(SO4)2标准溶液VmL,则TiO2质量分数表达式为____________ 。
(6)判断下列操作对配制NH4Fe(SO4)2标准溶液的影响(填“偏高”、“偏低”或“无影响”)
①若在配制标准溶液过程中,烧杯中的NH4Fe(SO4)2溶液有少量溅出,将导致结果______ 。
②若定容时俯视容量瓶刻线,将导致结果_____________ 。
制备纳米TiO2的方法之一是TiCl4水解生成TiO2·xH2O,经过滤、水洗除去其中的Cl-,再烘干、焙烧除去水分得到粉体TiO2。
用现代分析仪器测定TiO2粒子的大小;用氧化还原滴定法测定TiO2的质量分数:一定条件下,将TiO2溶解并还原为Ti3+,再以KSCN溶液作指示剂,用NH4Fe(SO4)2标准溶液滴定Ti3+至全部生成Ti4+。
请回答下列问题:
(1)TiCl4水解生成TiO2·xH2O的化学方程式为:
(2)检验TiO2·xH2O中Cl-是否被除净的方法是:
(3)可用于测定TiO2粒子大小的方法是
a.核磁共振法 b.红外光谱法 c.质谱法 d.透射电子显微镜法
(4)配制NH4Fe(SO4)2标准溶液时,使用的仪器除天平、药匙、玻璃棒、烧杯、量筒外,还需要下图中的

(5)滴定时,称取TiO2(摩尔质量为Mg·mol-1)试样wg,消耗cmol·L-1NH4Fe(SO4)2标准溶液VmL,则TiO2质量分数表达式为
(6)判断下列操作对配制NH4Fe(SO4)2标准溶液的影响(填“偏高”、“偏低”或“无影响”)
①若在配制标准溶液过程中,烧杯中的NH4Fe(SO4)2溶液有少量溅出,将导致结果
②若定容时俯视容量瓶刻线,将导致结果
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐1】探究无机盐 X(仅含三种短周期元素)的组成和性质,设计并完成如下实验:

请回答:
(1)X 的化学式是__________ 。
(2)白色粉末溶于氢氧化钠溶液的离子方程式是__________ 。
(3)白色沉淀用途广泛,请列举一例:__________ 。

请回答:
(1)X 的化学式是
(2)白色粉末溶于氢氧化钠溶液的离子方程式是
(3)白色沉淀用途广泛,请列举一例:
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐2】某研究小组为了探究一种抗酸药X(仅含五种短周期元素)的组成和性质,设计并完成了如下实验:
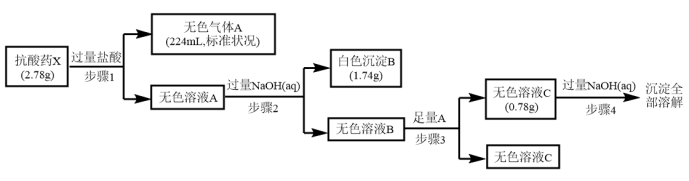
请回答下列问题:
(1)白色沉淀B中金属元素的离子结构示意图为_________ ,A的电子式为________ 。
(2)步骤3中生成沉淀C的离子方程式为_____________ 。
(3)X的化学式为_________ ,该抗酸药不适合胃溃疡重症患者使用,原因是________ 。
(4)设计实验方案验证步骤3后得到的无色溶液中的含有碳酸氢根离子_____________ 。

请回答下列问题:
(1)白色沉淀B中金属元素的离子结构示意图为
(2)步骤3中生成沉淀C的离子方程式为
(3)X的化学式为
(4)设计实验方案验证步骤3后得到的无色溶液中的含有碳酸氢根离子
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐3】某研究小组为了探究一种有机盐 X(仅含四种元素)的组成与性质,设计并完成如下实验:
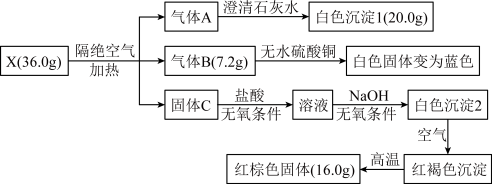
已知: A为两种常见气体的混合物, B、 C 均为常见物质。
(1)X中除含有氢、氧元素外,还含有的元素为:________________ (写元素名称)。
(2)写出 X 受热分解的化学方程式:____________________________________________ 。
(3)设计实验验证“红棕色固体”中金属阳离子______________________________________ 。

已知: A为两种常见气体的混合物, B、 C 均为常见物质。
(1)X中除含有氢、氧元素外,还含有的元素为:
(2)写出 X 受热分解的化学方程式:
(3)设计实验验证“红棕色固体”中金属阳离子
您最近一年使用:0次
解答题-有机推断题
|
较难
(0.4)
解题方法
【推荐1】某α-氨基酸,相对分子质量不超过100,经分析可知,该氨基酸含C、H、O、N四种元素,其中N元素的质量分数为15.7%,O元素的质量分数为36.0%。
(1)该氨基酸的分子中有_______ 个氨基,_______ 个羧基;
(2)该氨基酸相对分子质量(取整数值)为_______ ;
(3)该氨基酸的结构简式为_______ ;
(4)两分子该氨基酸在适当条件下加热去水生成一个具有六元环结构的化合物A,写出A的结构式_______ 。
(1)该氨基酸的分子中有
(2)该氨基酸相对分子质量(取整数值)为
(3)该氨基酸的结构简式为
(4)两分子该氨基酸在适当条件下加热去水生成一个具有六元环结构的化合物A,写出A的结构式
您最近一年使用:0次
解答题-有机推断题
|
较难
(0.4)
解题方法
【推荐2】Diels-Alder反应是一种合成氮杂环化合物的重要方法。水是代替有机溶剂最绿色、最便宜的溶剂,在很多Diels-Alder反应里具有优异的效果,不仅能提高产率而且提高立体选择性。据报道,有人据此原理合成了化合物(G),合成路线如下:

(1)写出化合物A的系统命名:_______ ;
(2)写出化合物B及C的结构简式:B:_______ ;C:_______ 。
(3)化合物E制备G可能经过生成F一步,则F的结构式为:_______ 。
(4)写出化合物D的立体异构体:_______ 。

(1)写出化合物A的系统命名:
(2)写出化合物B及C的结构简式:B:
(3)化合物E制备G可能经过生成F一步,则F的结构式为:
(4)写出化合物D的立体异构体:
您最近一年使用:0次
解答题-有机推断题
|
较难
(0.4)
解题方法
【推荐3】丙三醇,又称甘油。在印刷、食品、化妆品及烟草等工业中常用作润湿剂,也可以用来制造医药和炸药,工业用途极广。早前它以制肥皂的副产品而得;现在大多以合成方法制得。
CH3CH=CH2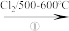 A(C3H5Cl)
A(C3H5Cl)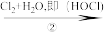
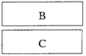 (B和C互为同分异构体)
(B和C互为同分异构体)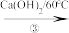
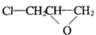
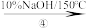 丙三醇
丙三醇
丙三醇和硝酸反应可以制炸药,其反应方程式如下: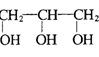
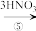 D(C3H5N3O9)
D(C3H5N3O9)
(1). 写出化合物A、B、C、D的结构简式:A_______ 、B_______ 、C_______ 、D_______ 。
(2). 写出下列反应的反应类型:③_______ 、⑤_______ 。
(3). 化合物D发生爆炸完全分解可生成CO2、N2、O2等,写出其反应方程式_______ 。
CH3CH=CH2
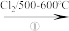 A(C3H5Cl)
A(C3H5Cl)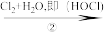
 (B和C互为同分异构体)
(B和C互为同分异构体)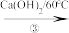
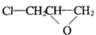
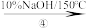 丙三醇
丙三醇丙三醇和硝酸反应可以制炸药,其反应方程式如下:
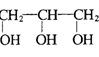
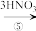 D(C3H5N3O9)
D(C3H5N3O9)(1). 写出化合物A、B、C、D的结构简式:A
(2). 写出下列反应的反应类型:③
(3). 化合物D发生爆炸完全分解可生成CO2、N2、O2等,写出其反应方程式
您最近一年使用:0次



