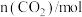设计原电池装置证明Fe3+的氧化性比Cu2+强。
(1)写出能说明氧化性Fe3+大于Cu2+的离子方程式:___________ 。
(2)若要将上述反应设计成原电池,电极反应式分别是:
①负极:___________
②正极:___________ 。
(3)画出装置图,指出电极材料和电解质溶液:
(1)写出能说明氧化性Fe3+大于Cu2+的离子方程式:
(2)若要将上述反应设计成原电池,电极反应式分别是:
①负极:
②正极:
(3)画出装置图,指出电极材料和电解质溶液:
| ①不含盐桥 | ②含盐桥 |
2021高二·全国·专题练习 查看更多[7]
(已下线)1.2.2 化学电源(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)(已下线)高中化学《新教材变化解读与考法剖析》第四章 化学反应与电能(人教版2019选择性必修1)(已下线)4.1 原电池-2021-2022学年高二化学课后培优练(人教版选修4)(已下线)第11讲 原电池的工作原理(word讲义)-【帮课堂】2021-2022学年高一化学同步精品讲义(人教版2019必修第二册)(已下线)第24讲 原电池的工作原理(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)(已下线)第六章 化学反应与能量 第35讲 原电池 化学电源(已下线)第3讲 原电池 化学电源
更新时间:2021-08-27 07:51:17
|
相似题推荐
【推荐1】完成下列问题
(1)氧化气化法可提纯电弧法合成的碳纳米管中的碳纳米颗粒杂质,反应的化学方程式为:3C + 2K2Cr2O7 + 8H2SO4 = 3CO2↑+ 2K2SO4 + 2Cr2(SO4)3 + 8H2O用双线桥标出电子转移的方向和数目_______ 。该反应中氧化剂是_______ ,每生成1个氧化产物,转移的电子数目为_______ 。
(2)高铁酸钾(K2FeO4)是一种新型的自来水处理剂,用于杀菌消毒。其制备可通过在强碱性条件下,由NaClO和FeCl3共热而得。则氧化性比较:NaClO_______ (填“>”或“<”)K2FeO4。
(3)ClO2是一种新型的水处理剂,可通过多种方法制取:如
①2KClO3 + 4HCl(浓) = 2KCl + 2ClO2↑ + Cl2↑+ 2H2O;
②Cl2 + 2KClO2 = 2KCl + 2ClO2。
则反应①中还原剂是_______ ,反应②的氧化产物与还原产物的质量比是_______ 。
(4)某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2.已知该反应中H2O2只发生如下过程:H2O2→O2,写出该反应的化学方程式,并用单线桥标出电子转移的方向和数目_______ 。
(5)一个完整的氧化还原反应方程式可以拆开写成两个“半反应式”,一个是“氧化反应”式,一个是“还原反应”式。如2Fe3++Cu=2Fe2++Cu2+的拆写结果是:氧化反应为:Cu﹣2e﹣=Cu2+;还原反应为:2Fe3++2e﹣=2Fe2+。请据此将反应:Fe+2H+=Fe2++H2↑拆写成两个“半反应式”:氧化反应为_______ 。
(1)氧化气化法可提纯电弧法合成的碳纳米管中的碳纳米颗粒杂质,反应的化学方程式为:3C + 2K2Cr2O7 + 8H2SO4 = 3CO2↑+ 2K2SO4 + 2Cr2(SO4)3 + 8H2O用双线桥标出电子转移的方向和数目
(2)高铁酸钾(K2FeO4)是一种新型的自来水处理剂,用于杀菌消毒。其制备可通过在强碱性条件下,由NaClO和FeCl3共热而得。则氧化性比较:NaClO
(3)ClO2是一种新型的水处理剂,可通过多种方法制取:如
①2KClO3 + 4HCl(浓) = 2KCl + 2ClO2↑ + Cl2↑+ 2H2O;
②Cl2 + 2KClO2 = 2KCl + 2ClO2。
则反应①中还原剂是
(4)某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2.已知该反应中H2O2只发生如下过程:H2O2→O2,写出该反应的化学方程式,并用单线桥标出电子转移的方向和数目
(5)一个完整的氧化还原反应方程式可以拆开写成两个“半反应式”,一个是“氧化反应”式,一个是“还原反应”式。如2Fe3++Cu=2Fe2++Cu2+的拆写结果是:氧化反应为:Cu﹣2e﹣=Cu2+;还原反应为:2Fe3++2e﹣=2Fe2+。请据此将反应:Fe+2H+=Fe2++H2↑拆写成两个“半反应式”:氧化反应为
您最近一年使用:0次
填空题
|
适中
(0.64)
【推荐2】(并非只有得氧、失氧的反应才是氧化还原反应,凡是有元素化合价升降的化学反应都是氧化还原反应。现在如下氧化还原反应,回答下列问题:
MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
(1)氧化剂是_________ ,氧化产物是________
(2)未变价元素是_______ ,将反应成离子方程式________
(3)用单线桥表示转移的电子数:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O_______________
(4)氧化产物和还原产物的质量之比为___________________
(5)反应中生成3.6gH2O,转移电子数为_______ 个。
(6)已知铵盐受热易分解,硝酸铵在一定条件下发生的分解反应为:5NH4NO3=2HNO3+4N2↑+9H2O,当生成还原产物0.6mol时,转移的电子的物质的量是_________ mol。
MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O(1)氧化剂是
(2)未变价元素是
(3)用单线桥表示转移的电子数:MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O(4)氧化产物和还原产物的质量之比为
(5)反应中生成3.6gH2O,转移电子数为
(6)已知铵盐受热易分解,硝酸铵在一定条件下发生的分解反应为:5NH4NO3=2HNO3+4N2↑+9H2O,当生成还原产物0.6mol时,转移的电子的物质的量是
您最近一年使用:0次
【推荐3】含氯物质在日常生活中具有许多重要用途,回答下列问题:
(1)工业上常利用反应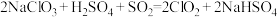 制备ClO2,其中还原剂是
制备ClO2,其中还原剂是___________ 。
(2)亚氯酸钠(NaClO2)较稳定,但加热或敲击亚氯酸钠固体时立即爆炸,爆炸后的产物可能为___________(填标号)。
(3)工业上可利用ClO2制备亚氯酸钠(NaClO2),反应体系中涉及下列物质(有一种物质未列出):NaClO2、ClO2、H2O2、NaOH、O2,写出反应的化学方程式___________ 。
(4)某温度下将Cl2通入KOH溶液里,反应后得到KCl、KClO、KClO3,的混合溶液,其中ClO—与 的个数之比为11∶1,则Cl2与KOH反应时,被还原的氯原子和被氧化的氯原子的个数之比为
的个数之比为11∶1,则Cl2与KOH反应时,被还原的氯原子和被氧化的氯原子的个数之比为___________ 。
(5)已知还原性:I—>Fe2+>Cl—,写出少量氯气通入到FeI2溶液中的离子方程式___________ 。
(6)实验室用下列方法均可制取氯气
①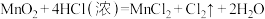
②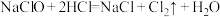
③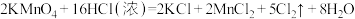
④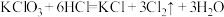
若各反应转移的电子数相同,①②③④生成的氯气质量比为___________ 。
(1)工业上常利用反应
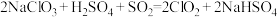 制备ClO2,其中还原剂是
制备ClO2,其中还原剂是(2)亚氯酸钠(NaClO2)较稳定,但加热或敲击亚氯酸钠固体时立即爆炸,爆炸后的产物可能为___________(填标号)。
| A.NaCl、Cl2 | B.NaCl、NaClO |
| C.NaClO3、NaClO4 | D.NaCl、NaClO3 |
(4)某温度下将Cl2通入KOH溶液里,反应后得到KCl、KClO、KClO3,的混合溶液,其中ClO—与
 的个数之比为11∶1,则Cl2与KOH反应时,被还原的氯原子和被氧化的氯原子的个数之比为
的个数之比为11∶1,则Cl2与KOH反应时,被还原的氯原子和被氧化的氯原子的个数之比为(5)已知还原性:I—>Fe2+>Cl—,写出少量氯气通入到FeI2溶液中的离子方程式
(6)实验室用下列方法均可制取氯气
①
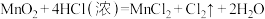
②
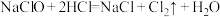
③
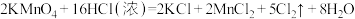
④
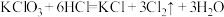
若各反应转移的电子数相同,①②③④生成的氯气质量比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献。
(1)现有如下两个反应:A. ;B.
;B. 。上述反应中能设计成原电池的是
。上述反应中能设计成原电池的是___________ (填字母)。
(2)将纯锌片和纯铜片按如图甲、乙所示方式插入100mL相同浓度的稀硫酸中一段时间,回答下列问题:___________ (填字母)。
A.甲、乙均为化学能转变为电能的装置 B.乙中铜片上没有明显变化
C.甲中铜片质量减少、乙中锌片质量减少 D.两烧杯中溶液的pH均增大
②在相同时间内,两烧杯中产生气泡的速度:甲___________ (填“>”、“<”或“=”)乙。
③请写出图中构成原电池的装置负极的电极反应式___________ 。
④当乙中产生11.2L(标准状况)气体时,转移电子为___________ mol。
(1)现有如下两个反应:A.
 ;B.
;B. 。上述反应中能设计成原电池的是
。上述反应中能设计成原电池的是(2)将纯锌片和纯铜片按如图甲、乙所示方式插入100mL相同浓度的稀硫酸中一段时间,回答下列问题:

A.甲、乙均为化学能转变为电能的装置 B.乙中铜片上没有明显变化
C.甲中铜片质量减少、乙中锌片质量减少 D.两烧杯中溶液的pH均增大
②在相同时间内,两烧杯中产生气泡的速度:甲
③请写出图中构成原电池的装置负极的电极反应式
④当乙中产生11.2L(标准状况)气体时,转移电子为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】从能量的变化和反应的快慢等角度研究反应:CH4+2O2=2H2O+CO2。
(1)下图能正确表示该反应中能量变化的是________ 。

(2)酸性甲烷燃料电池的总反应方程式为CH4+2O2 = 2H2O+CO2。其中,负极的电极反应式为________ ;正极发生________ 反应(填“氧化”或“还原”)。电路中每转移0.2 mol电子,标准状况下消耗O2的体积是________ L。
(3)理论上讲,任何自发的氧化还原反应都可以设计成原电池,请你利用下列反应Cu+2Ag+=Cu2++2Ag设计一个化学电池,并回答下列问题:
①该电池的正极材料是________ ,负极材料是 ________ ,电解质溶液是 ________ 。
②正极的电极反应式为________ 。
(1)下图能正确表示该反应中能量变化的是

(2)酸性甲烷燃料电池的总反应方程式为CH4+2O2 = 2H2O+CO2。其中,负极的电极反应式为
(3)理论上讲,任何自发的氧化还原反应都可以设计成原电池,请你利用下列反应Cu+2Ag+=Cu2++2Ag设计一个化学电池,并回答下列问题:
①该电池的正极材料是
②正极的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献。将锌片和铜片插入相同浓度的稀硫酸中,如图所示:
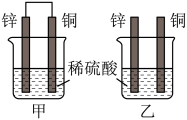
回答下列问题:
(1)下列说法正确的是________ 。
a.甲、乙均为化学能转变为电能的装置
b.甲中锌片是负极,乙中铜片是正极
c.甲、乙溶液中的pH均增大
d.若将稀硫酸换为硫酸铜溶液,则甲、乙中铜片的质量均增加
(2)甲、乙中构成原电池的正极电极反应式为_________ ,原电池工作过程中,电流由_________ (填“铜片”或“锌片”)经导线流向___________ (填“铜片”或“锌片”);溶液中的 向
向________ (填“正极”或“负极”)移动。
(3)当甲中溶液质量增重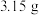 时,电极上转移电子数目为
时,电极上转移电子数目为_________ ,生成的氢气在标准状况下的体积为________ 。
(4)对甲、乙装置做如下变化后,可形成原电池的是__________ 。
a.甲中铜片换成锌片
b.乙中锌片和铜片相互倾斜至上端接触
c.甲中稀硫酸用乙醇代替

回答下列问题:
(1)下列说法正确的是
a.甲、乙均为化学能转变为电能的装置
b.甲中锌片是负极,乙中铜片是正极
c.甲、乙溶液中的pH均增大
d.若将稀硫酸换为硫酸铜溶液,则甲、乙中铜片的质量均增加
(2)甲、乙中构成原电池的正极电极反应式为
 向
向(3)当甲中溶液质量增重
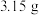 时,电极上转移电子数目为
时,电极上转移电子数目为(4)对甲、乙装置做如下变化后,可形成原电池的是
a.甲中铜片换成锌片
b.乙中锌片和铜片相互倾斜至上端接触
c.甲中稀硫酸用乙醇代替
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】下图是一个电化学过程的示意图,请回答下列问题:

(1)图中甲池是_________ (填“原电池” “电解池”或“电镀池”)。
(2)A(石墨)电极的名称是_________ (填“正极” “负极” “阴极”或“阳极”)。
(3)写出通入CH3OH的电极的电极反应式________________ 。
(4)乙池中反应的化学方程式为__________________ 。当乙池中B(Ag)极质量增加54g,甲池中理论上消耗O2的体积为____ L(标准状况)。

(1)图中甲池是
(2)A(石墨)电极的名称是
(3)写出通入CH3OH的电极的电极反应式
(4)乙池中反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】I. 作为化石燃料燃烧产生的废气,是主要的温室气体之一,使用电化学方法能够对
作为化石燃料燃烧产生的废气,是主要的温室气体之一,使用电化学方法能够对 进行吸收。利用活泼金属与二氧化碳的反应,能够构建金属-
进行吸收。利用活泼金属与二氧化碳的反应,能够构建金属- 电池,其中一种
电池,其中一种 电池的模型如下图所示:(图中
电池的模型如下图所示:(图中 是固体)
是固体)
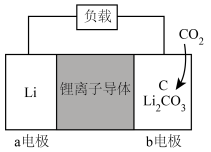
(1)下列有关该原电池的说法中,正确的是___________。
(2)写出该原电池的正极反应以及总反应,正极:___________ ;总反应:___________ 。
(3)原电池中每转移 电子,能够吸收
电子,能够吸收___________ 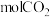 。
。
II.利用电解池,通过电化学还原, 能够被还原为低价碳化合物。一种电化学还原二氧化碳的装置能够将二氧化碳还原为甲酸
能够被还原为低价碳化合物。一种电化学还原二氧化碳的装置能够将二氧化碳还原为甲酸 ,该装置中,石墨作为阳极,单质银作为阴极,电解质溶液是硫酸溶液。
,该装置中,石墨作为阳极,单质银作为阴极,电解质溶液是硫酸溶液。
(4)在该装置中,应该向___________ 极(填“阴”或“阳”)附近通入 气体。
气体。
(5)写出 在该电极上反应的电极反应式:
在该电极上反应的电极反应式:___________ 。
(6)当电极上生成5.6L(标准状况)的氧气时,生成甲酸的质量为___________ g。
 作为化石燃料燃烧产生的废气,是主要的温室气体之一,使用电化学方法能够对
作为化石燃料燃烧产生的废气,是主要的温室气体之一,使用电化学方法能够对 进行吸收。利用活泼金属与二氧化碳的反应,能够构建金属-
进行吸收。利用活泼金属与二氧化碳的反应,能够构建金属- 电池,其中一种
电池,其中一种 电池的模型如下图所示:(图中
电池的模型如下图所示:(图中 是固体)
是固体)
(1)下列有关该原电池的说法中,正确的是___________。
| A.该原电池工作时,电子由正极向负极移动 |
| B.在该原电池中,石墨作为负极 |
| C.原电池工作时,阳离子一定向正极方向移动 |
| D.原电池工作时,b电极发生氧化反应 |
(2)写出该原电池的正极反应以及总反应,正极:
(3)原电池中每转移
 电子,能够吸收
电子,能够吸收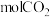 。
。II.利用电解池,通过电化学还原,
 能够被还原为低价碳化合物。一种电化学还原二氧化碳的装置能够将二氧化碳还原为甲酸
能够被还原为低价碳化合物。一种电化学还原二氧化碳的装置能够将二氧化碳还原为甲酸 ,该装置中,石墨作为阳极,单质银作为阴极,电解质溶液是硫酸溶液。
,该装置中,石墨作为阳极,单质银作为阴极,电解质溶液是硫酸溶液。(4)在该装置中,应该向
 气体。
气体。(5)写出
 在该电极上反应的电极反应式:
在该电极上反应的电极反应式:(6)当电极上生成5.6L(标准状况)的氧气时,生成甲酸的质量为
您最近一年使用:0次
【推荐3】在容积为2L的恒温容器中,充入 和
和 ,一定条件下发生反应
,一定条件下发生反应 ,测得
,测得 和
和 的物质的量随时间的变化情况如下表。
的物质的量随时间的变化情况如下表。
(1)下列说法正确的是______ (填标号)。
a.反应达到平衡后,反应不再进行
b.使用催化剂可以增大反应速率,提高生产效率
c.当容器内混合气体的平均相对分子质量不变时,说明反应达到了化学平衡状态
d.通过调控反应条件,可以提高该反应进行的程度,使 可以100%地转化为
可以100%地转化为
(2)3~6min内,
______  .
.
(3)12min末时,混合气体中 的体积分数为
的体积分数为______ 。
(4)第3min时
______ (填“>”“<”或“=”)第9min时 。
。
(5)一定温度条件下,能够说明该反应到达平衡的标志是____________ 。
①若恒压容器中,混合气体的密度保持不变;②单位时间内生成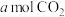 ,同时消耗
,同时消耗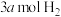 ;③
;③ 与
与 的总浓度等于
的总浓度等于 与
与 的总浓度;④
的总浓度;④ 的物质的量不再变化;⑤恒容容器中,混合气体的总压强不再变化;
的物质的量不再变化;⑤恒容容器中,混合气体的总压强不再变化;
(6) 还可以直接由CO和
还可以直接由CO和 制得,根据如图一所示的转化关系判断,生成
制得,根据如图一所示的转化关系判断,生成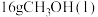 放出
放出______ kJ能量。
(7) 和
和 可以形成碱性燃料电池,结构如图二所示。
可以形成碱性燃料电池,结构如图二所示。
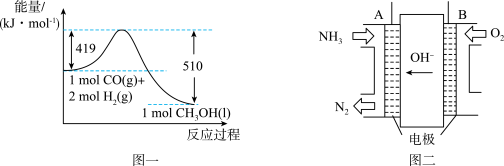
①电极A反应式为__________ 。
②若反应生成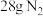 ,则该燃料电池理论上消耗的
,则该燃料电池理论上消耗的 的体积(在标准状况下)为
的体积(在标准状况下)为______ L。
 和
和 ,一定条件下发生反应
,一定条件下发生反应 ,测得
,测得 和
和 的物质的量随时间的变化情况如下表。
的物质的量随时间的变化情况如下表。时间 | 0min | 3min | 6min | 9min | 12min |
| 0 | 0.50 | 0.65 | 0.75 | 0.75 |
| 1 | 0.50 | 0.35 | x | 0.25 |
(1)下列说法正确的是
a.反应达到平衡后,反应不再进行
b.使用催化剂可以增大反应速率,提高生产效率
c.当容器内混合气体的平均相对分子质量不变时,说明反应达到了化学平衡状态
d.通过调控反应条件,可以提高该反应进行的程度,使
 可以100%地转化为
可以100%地转化为
(2)3~6min内,

 .
.(3)12min末时,混合气体中
 的体积分数为
的体积分数为(4)第3min时

 。
。(5)一定温度条件下,能够说明该反应到达平衡的标志是
①若恒压容器中,混合气体的密度保持不变;②单位时间内生成
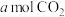 ,同时消耗
,同时消耗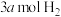 ;③
;③ 与
与 的总浓度等于
的总浓度等于 与
与 的总浓度;④
的总浓度;④ 的物质的量不再变化;⑤恒容容器中,混合气体的总压强不再变化;
的物质的量不再变化;⑤恒容容器中,混合气体的总压强不再变化;(6)
 还可以直接由CO和
还可以直接由CO和 制得,根据如图一所示的转化关系判断,生成
制得,根据如图一所示的转化关系判断,生成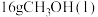 放出
放出(7)
 和
和 可以形成碱性燃料电池,结构如图二所示。
可以形成碱性燃料电池,结构如图二所示。
①电极A反应式为
②若反应生成
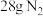 ,则该燃料电池理论上消耗的
,则该燃料电池理论上消耗的 的体积(在标准状况下)为
的体积(在标准状况下)为
您最近一年使用:0次