某工厂以废料(主要含 ,还含少量的
,还含少量的 、
、 、
、 )为原料制备碳酸铈、氯化铈等铈产品的流程如下:
)为原料制备碳酸铈、氯化铈等铈产品的流程如下:
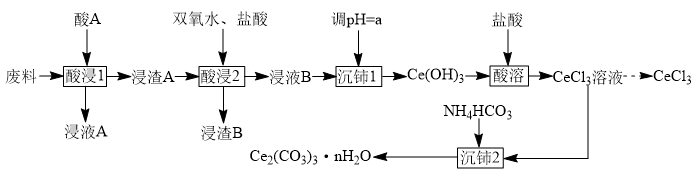
已知: 具有强氧化性,通常情况下不和无机酸反应。
具有强氧化性,通常情况下不和无机酸反应。
回答下列问题:
(1)为加快“酸浸1”的速率,可采取的措施是___________ (写一条即可)。
(2)检验“浸液 ”中含有
”中含有 的试剂是
的试剂是___________ (填化学式,下同)溶液,“浸渣 ”的主要成分为
”的主要成分为___________ 。
(3)“酸浸2”中双氧水的作用是___________ (用离子方程式回答)。
(4)获得 的方法:将
的方法:将 和
和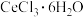 混合灼烧,得到
混合灼烧,得到 并放出能使品红溶液褪色的气体。加入
并放出能使品红溶液褪色的气体。加入 的原因是
的原因是___________ 。
(5)已知醋酸铵溶液呈中性,则 溶液中:
溶液中:
___________ (填“ ”、“
”、“ ”或“
”或“ ”)
”)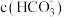 。
。
(6)测定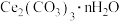 的纯度:
的纯度:
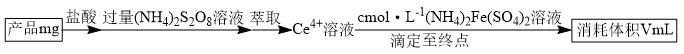
①已知 与
与 反应后的产物为
反应后的产物为 ,则该反应中氧化产物(
,则该反应中氧化产物( )与还原产物(
)与还原产物( )的物质的量之比为
)的物质的量之比为___________ 。
② 的纯度为
的纯度为___________  。[已知:
。[已知: 的摩尔质量为
的摩尔质量为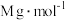 ]
]
③若其他操作均正确,滴定后俯视读数,则测得 的纯度
的纯度___________ (填“偏高”“偏低”或“无影响”)。
 ,还含少量的
,还含少量的 、
、 、
、 )为原料制备碳酸铈、氯化铈等铈产品的流程如下:
)为原料制备碳酸铈、氯化铈等铈产品的流程如下:
已知:
 具有强氧化性,通常情况下不和无机酸反应。
具有强氧化性,通常情况下不和无机酸反应。回答下列问题:
(1)为加快“酸浸1”的速率,可采取的措施是
(2)检验“浸液
 ”中含有
”中含有 的试剂是
的试剂是 ”的主要成分为
”的主要成分为(3)“酸浸2”中双氧水的作用是
(4)获得
 的方法:将
的方法:将 和
和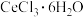 混合灼烧,得到
混合灼烧,得到 并放出能使品红溶液褪色的气体。加入
并放出能使品红溶液褪色的气体。加入 的原因是
的原因是(5)已知醋酸铵溶液呈中性,则
 溶液中:
溶液中:
 ”、“
”、“ ”或“
”或“ ”)
”)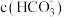 。
。(6)测定
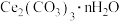 的纯度:
的纯度: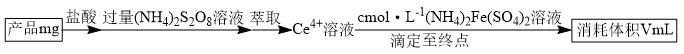
①已知
 与
与 反应后的产物为
反应后的产物为 ,则该反应中氧化产物(
,则该反应中氧化产物( )与还原产物(
)与还原产物( )的物质的量之比为
)的物质的量之比为②
 的纯度为
的纯度为 。[已知:
。[已知: 的摩尔质量为
的摩尔质量为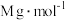 ]
]③若其他操作均正确,滴定后俯视读数,则测得
 的纯度
的纯度
更新时间:2021-08-30 17:33:00
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
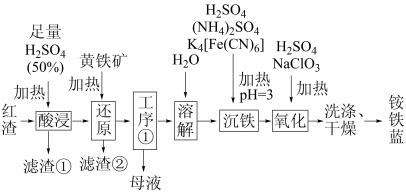
【推荐1】以焙烧黄铁矿FeS2(杂质为石英等)产生的红渣为原料制备铵铁蓝Fe(NH4)Fe(CN)6颜料。工艺流程如图:
(1)红渣的主要成分为________ (填化学式),滤渣①的主要成分为________ (填化学式)。
(2)黄铁矿研细的目的是________ 。
(3)还原工序中,不生成S单质的反应的离子方程式为:________ 。
(4)工序①的名称为________ 、________ 、过滤、洗涤,所得母液循环使用。
(5)沉铁工序产生的白色沉淀Fe(NH4)2Fe(CN)6中Fe的化合价为________ ,氧化工序发生反应的离子方程式为:________ 。
(6)若用还原工序得到的滤液制备Fe2O3•xH2O和(NH4)2SO4,所加试剂为________ 和________ 。(填化学式,不引入杂质)
(1)红渣的主要成分为
(2)黄铁矿研细的目的是
(3)还原工序中,不生成S单质的反应的离子方程式为:
(4)工序①的名称为
(5)沉铁工序产生的白色沉淀Fe(NH4)2Fe(CN)6中Fe的化合价为
(6)若用还原工序得到的滤液制备Fe2O3•xH2O和(NH4)2SO4,所加试剂为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某补铁剂的主要成分是硫酸亚铁( ),说明书中建议“本品与维生素C同服”。小组同学为探究其原理,用放置7天的
),说明书中建议“本品与维生素C同服”。小组同学为探究其原理,用放置7天的 溶液(
溶液(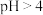 )进行下列实验。
)进行下列实验。
资料:维生素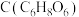 又称抗坏血酸,易溶于水,其溶液呈酸性。
又称抗坏血酸,易溶于水,其溶液呈酸性。
I.检验铁元素的价态
(1)i中观察到_______ ,说明溶液中存在 。将
。将 氧化的物质是
氧化的物质是_______ 。
(2)①小组同学推测,ii中溶液仍为无色是因为维生素 与
与 发生了反应。补全该反应的离子方程式。
发生了反应。补全该反应的离子方程式。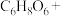 □
□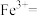 □___
□___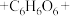 □
□
___
②甲同学认为,可以取ii中溶液加入酸性 溶液验证反应产物。乙同学认为该方法不可行,理由是
溶液验证反应产物。乙同学认为该方法不可行,理由是_______ 。
(3)丙同学认为ii中检验方案不严谨,应考虑pH对反应的影响,依据是_______ 。
II.探究pH对ii中反应的影响
小组同学补充了如下实验,继续探究pH对ii中反应的影响。
(4)判断下列关于实验结论的说法是否正确 (填“对”或“错”)。
①pH对 与
与 的显色反应有影响。
的显色反应有影响。_______
②加维生素 后
后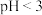 ,导致ii中未末检测出
,导致ii中未末检测出 。
。_______
(5)反思实验i~iii,下列说法合理的是_____ (填序号)。
a.维生素C具有氧化性和酸性
b.同服维生素C可减缓补铁剂中 被氧化
被氧化
c.使用KSCN检验 时,宜先将溶液酸化
时,宜先将溶液酸化
 ),说明书中建议“本品与维生素C同服”。小组同学为探究其原理,用放置7天的
),说明书中建议“本品与维生素C同服”。小组同学为探究其原理,用放置7天的 溶液(
溶液(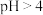 )进行下列实验。
)进行下列实验。资料:维生素
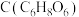 又称抗坏血酸,易溶于水,其溶液呈酸性。
又称抗坏血酸,易溶于水,其溶液呈酸性。I.检验铁元素的价态
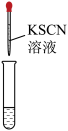 | 实验序号 | 试管中的试剂 | 实验操作及现象 |
| i | 2 mL放置后的 溶液 溶液 | 滴加5滴KSCN溶液后,溶液变为浅红色 | |
| ii | 2 mL放置后的 溶液,0.1 g维生素C 溶液,0.1 g维生素C | 维生素C溶解,溶液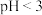 ,滴加5滴KSCN溶液后,溶液 仍呈无色 ,滴加5滴KSCN溶液后,溶液 仍呈无色 |
 。将
。将 氧化的物质是
氧化的物质是(2)①小组同学推测,ii中溶液仍为无色是因为维生素
 与
与 发生了反应。补全该反应的离子方程式。
发生了反应。补全该反应的离子方程式。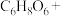 □
□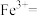 □___
□___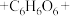 □
□
②甲同学认为,可以取ii中溶液加入酸性
 溶液验证反应产物。乙同学认为该方法不可行,理由是
溶液验证反应产物。乙同学认为该方法不可行,理由是(3)丙同学认为ii中检验方案不严谨,应考虑pH对反应的影响,依据是
II.探究pH对ii中反应的影响
小组同学补充了如下实验,继续探究pH对ii中反应的影响。
| 实验序号 | 试剂 | 实验操作及现象 |
| iii |  | 滴加5滴KSCN溶液后,溶液变为浅红色,浅红色比i中加深 |
①pH对
 与
与 的显色反应有影响。
的显色反应有影响。②加维生素
 后
后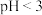 ,导致ii中未末检测出
,导致ii中未末检测出 。
。(5)反思实验i~iii,下列说法合理的是
a.维生素C具有氧化性和酸性
b.同服维生素C可减缓补铁剂中
 被氧化
被氧化c.使用KSCN检验
 时,宜先将溶液酸化
时,宜先将溶液酸化
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】回答下列问题
(1)已知:还原性HSO >I-,氧化性IO
>I-,氧化性IO >I2,在NaIO3溶液中滴加少量NaHSO3溶液,发生下列反应:NaIO3+NaHSO3→I2+Na2SO4+H2SO4+H2O
>I2,在NaIO3溶液中滴加少量NaHSO3溶液,发生下列反应:NaIO3+NaHSO3→I2+Na2SO4+H2SO4+H2O
①配平上述反应的化学方程式_______ ;并写出其氧化产物_______ 。
②在NaIO3溶液中滴加过量NaHSO3溶液,反应完全后,推测反应后溶液中的还原产物为_______ (填化学式);
(2)向某密闭容器中加入0.15 mol/LA、0.05 mol/L C和一定量的B三种气体。一定条件下发生反应,各物质浓度随时间变化如下图中甲图所示[t0时c(B)未画出,t1时增大到0.05 mol/L]。乙图为t2时刻后改变反应条件,平衡体系中正、逆反应速率随时间变化的情况。
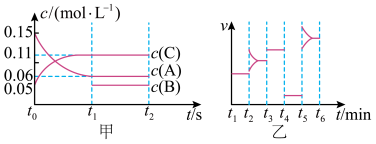
①若t4时改变的条件为减小压强,则B的起始物质的量浓度为_______ mol/L;
②若t1=15 s,则t0~t1阶段以C浓度变化表示的平均反应速率为v(C)=_______ mol/(L·s)。
③t3时改变的某一反应条件可能是_______ (选填序号)。
a.用催化剂 b.增大大压强 c.增大反应物浓度
④有甲、乙两个容积均为2L的密闭容器,在控制两容器温度相同且恒定情况下,向甲中通入3mol A,达到平衡时,B的体积分数为20%,则向乙容器中充入1 mol C和0.5mol B,达到平衡时,C的浓度c(C)=_______
(1)已知:还原性HSO
 >I-,氧化性IO
>I-,氧化性IO >I2,在NaIO3溶液中滴加少量NaHSO3溶液,发生下列反应:NaIO3+NaHSO3→I2+Na2SO4+H2SO4+H2O
>I2,在NaIO3溶液中滴加少量NaHSO3溶液,发生下列反应:NaIO3+NaHSO3→I2+Na2SO4+H2SO4+H2O①配平上述反应的化学方程式
②在NaIO3溶液中滴加过量NaHSO3溶液,反应完全后,推测反应后溶液中的还原产物为
(2)向某密闭容器中加入0.15 mol/LA、0.05 mol/L C和一定量的B三种气体。一定条件下发生反应,各物质浓度随时间变化如下图中甲图所示[t0时c(B)未画出,t1时增大到0.05 mol/L]。乙图为t2时刻后改变反应条件,平衡体系中正、逆反应速率随时间变化的情况。

①若t4时改变的条件为减小压强,则B的起始物质的量浓度为
②若t1=15 s,则t0~t1阶段以C浓度变化表示的平均反应速率为v(C)=
③t3时改变的某一反应条件可能是
a.用催化剂 b.增大大压强 c.增大反应物浓度
④有甲、乙两个容积均为2L的密闭容器,在控制两容器温度相同且恒定情况下,向甲中通入3mol A,达到平衡时,B的体积分数为20%,则向乙容器中充入1 mol C和0.5mol B,达到平衡时,C的浓度c(C)=
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】K2Cr2O7是一种重要的化工原料。以铬铁矿(主要成分为FeO·Cr2O3,还含有Al2O3、Fe2O3等杂质)为原料制备K2Cr2O7的一种工艺流程如下:
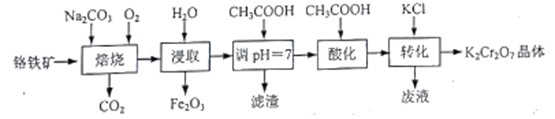
已知:
①4FeO·Cr2O3+8Na2CO3+7O2 8Na2CrO4+2Fe2O3+8CO2
8Na2CrO4+2Fe2O3+8CO2
②Cr2O72-+H2O 2CrO42-+2H+
2CrO42-+2H+
(1)“焙烧”时,Al2O3与Na2CO3发生反应的化学方程式为___________ 。
(2)“滤渣”的主要成分是________ (填化学式).
(3)“酸化”步骤调节溶液pH<5,其目的是_________
(4)“转化”一步发生反应的化学方程式为____________
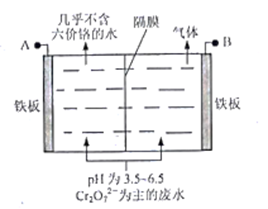
(5)采用电解法处理含铬废水原理如下图所示。阳极区溶液中发生反应:Cr2O72-+6Fe2++14H+ == 2Cr3+ +6Fe3+ + 7H2O,阳极的电极反应式为_______ ,阴极产生的气体为_______ (填化学式)。

已知:
①4FeO·Cr2O3+8Na2CO3+7O2
 8Na2CrO4+2Fe2O3+8CO2
8Na2CrO4+2Fe2O3+8CO2②Cr2O72-+H2O
 2CrO42-+2H+
2CrO42-+2H+(1)“焙烧”时,Al2O3与Na2CO3发生反应的化学方程式为
(2)“滤渣”的主要成分是
(3)“酸化”步骤调节溶液pH<5,其目的是
(4)“转化”一步发生反应的化学方程式为
(5)采用电解法处理含铬废水原理如下图所示。阳极区溶液中发生反应:Cr2O72-+6Fe2++14H+ == 2Cr3+ +6Fe3+ + 7H2O,阳极的电极反应式为

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】重铬酸钾(K2Cr2O7)主要用于制革、印染、电镀等。其水溶液中存在平衡: +H2O
+H2O 2
2 +2H+
+2H+
(1)已知有关物质溶解度如图1。用复分解法制备K2Cr2O7的操作过程是:向Na2Cr2O7溶液中加入_________ (填化学式),搅拌溶解,调节溶液pH约为5,加热溶液至表面有少量晶体析出时,_____________ ,抽滤得到粗产品,再用重结晶法提纯粗产品。

(2)以铬酸钾(K2CrO4)为原料,用电化学法制备重铬酸钾的实验装置如图2。
①不锈钢作________ 极,写出该电极的电极反应式________________________ 。
②分析阳极区能得到重铬酸钾溶液的原因________________________ 。
③当铬酸钾的转化率达到x时,阳极液中K与Cr的物质的量之比为____________ 。
(3)铬对环境能造成污染。某酸性废水中含有 ,处理时可用焦亚硫酸钠(Na2S2O5)将
,处理时可用焦亚硫酸钠(Na2S2O5)将 转化为毒性较低的Cr3+,再调节pH约为8,使铬元素沉降,分离出污泥后检测废水中Cr3+浓度,低于0.5mg·L-1则达到排放标准。
转化为毒性较低的Cr3+,再调节pH约为8,使铬元素沉降,分离出污泥后检测废水中Cr3+浓度,低于0.5mg·L-1则达到排放标准。
①Na2S2O5参加反应的离子方程式为____________________ 。
②经上述工艺处理后的废水,理论上Cr3+浓度约为__________ mg·L-1。(已知室温下Ksp≈6×10-31)
 +H2O
+H2O 2
2 +2H+
+2H+(1)已知有关物质溶解度如图1。用复分解法制备K2Cr2O7的操作过程是:向Na2Cr2O7溶液中加入

(2)以铬酸钾(K2CrO4)为原料,用电化学法制备重铬酸钾的实验装置如图2。
①不锈钢作
②分析阳极区能得到重铬酸钾溶液的原因
③当铬酸钾的转化率达到x时,阳极液中K与Cr的物质的量之比为
(3)铬对环境能造成污染。某酸性废水中含有
 ,处理时可用焦亚硫酸钠(Na2S2O5)将
,处理时可用焦亚硫酸钠(Na2S2O5)将 转化为毒性较低的Cr3+,再调节pH约为8,使铬元素沉降,分离出污泥后检测废水中Cr3+浓度,低于0.5mg·L-1则达到排放标准。
转化为毒性较低的Cr3+,再调节pH约为8,使铬元素沉降,分离出污泥后检测废水中Cr3+浓度,低于0.5mg·L-1则达到排放标准。①Na2S2O5参加反应的离子方程式为
②经上述工艺处理后的废水,理论上Cr3+浓度约为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】为探究由3种短周期元素构成的化合物X的性质。完成以下实验:

(1)X的化学式为_______ 。
(2)气体A与足量CuO反应的化学方程式为_______ 。
(3)溶液II通入过量CO2时,发生反应的离子方程式为_______ 、_______ 。
(4)将F溶液通过一系列操作获得结晶水合物(含有结晶水的盐),加热该结晶水合物。将生成的红棕色混合气体(>100°C)全部收集并冷却。气体全部反应无剩余,得到一元强酸E的水溶液(其中E与水的物质的量之比2∶5)写出该结晶水合物的化学式_______ 。
(5)设计实验证明F溶液的阴离子(OH-除外)_______ 。

(1)X的化学式为
(2)气体A与足量CuO反应的化学方程式为
(3)溶液II通入过量CO2时,发生反应的离子方程式为
(4)将F溶液通过一系列操作获得结晶水合物(含有结晶水的盐),加热该结晶水合物。将生成的红棕色混合气体(>100°C)全部收集并冷却。气体全部反应无剩余,得到一元强酸E的水溶液(其中E与水的物质的量之比2∶5)写出该结晶水合物的化学式
(5)设计实验证明F溶液的阴离子(OH-除外)
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】我国是最早发现并使用锌的国家,《天工开物》记载了炉甘石(ZnCO3)和木炭冶炼锌。现代工业上用氧化锌烟灰(主要成分为ZnO 、少量Pb、CuO和As2O3)制取高纯锌的工艺流程如图所示。

请回答下列问题:
(1)《天工开物》中炼锌的方法中利用了木炭的____ 性。
(2)滤渣1和滤渣3的主要成分分别是______ 、______ (填化学式)。
(3)“溶浸”时,氧化锌参与反应的相关离子方程式是______ ;“溶浸”时温度不宜过高,其原因是______ 。
(4)“氧化除杂”的目的是将AsCl52-转化为As2O5胶体,再经吸附聚沉除去,该反应的离子方程式是______ 。
(5)“电解”含 [Zn(NH3)4]2+的溶液,阴极放电的电极反应式是______ 。阳极区产生一种无色无味的气体,将其通入滴有KSCN的FeCl2溶液中,无明显现象,该气体是_____ (写化学式)。该流程中可以循环使用的物质是_____ (写化学式)。

请回答下列问题:
(1)《天工开物》中炼锌的方法中利用了木炭的
(2)滤渣1和滤渣3的主要成分分别是
(3)“溶浸”时,氧化锌参与反应的相关离子方程式是
(4)“氧化除杂”的目的是将AsCl52-转化为As2O5胶体,再经吸附聚沉除去,该反应的离子方程式是
(5)“电解”含 [Zn(NH3)4]2+的溶液,阴极放电的电极反应式是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】一种以黄铜矿和硫磺为原料制取铜和其他产物的新工艺,原料的综合利用率较高。其主要流程如下:
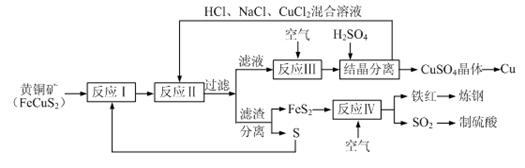
注:反应Ⅱ的离子方程式为Cu2++CuS+4Cl—=2CuCl2-+S
请回答下列问题:
⑴反应Ⅰ的产物为(填化学式) ▲ 。
⑵反应Ⅲ的离子方程式为 ▲ 。
⑶一定温度下,在反应Ⅲ所得的溶液中加入稀硫酸,可以析出硫酸铜晶体,其原因是
▲ 。
⑷炼钢时,可将铁红投入熔融的生铁中,该过程中主要反应的化学方程式是 ▲ 。
⑸某硫酸厂为测定反应Ⅳ所得气体中SO2的体积分数,取280mL(已折算成标准状况)气体样品与足量Fe2(SO4)3溶液完全反应后,用浓度为0.02000 mol/L的K2Cr2O7标准溶液滴定至终点,消耗K2Cr2O7溶液25.00 mL 。
已知:Cr2O72-+ Fe2++ H+→Cr3++ Fe3++ H2O(未配平)
①SO2通入Fe2(SO4)3溶液,发生反应的离子方程式为 ▲ 。
②反应Ⅳ所得气体中SO2的体积分数为 ▲ 。

注:反应Ⅱ的离子方程式为Cu2++CuS+4Cl—=2CuCl2-+S
请回答下列问题:
⑴反应Ⅰ的产物为(填化学式) ▲ 。
⑵反应Ⅲ的离子方程式为 ▲ 。
⑶一定温度下,在反应Ⅲ所得的溶液中加入稀硫酸,可以析出硫酸铜晶体,其原因是
▲ 。
⑷炼钢时,可将铁红投入熔融的生铁中,该过程中主要反应的化学方程式是 ▲ 。
⑸某硫酸厂为测定反应Ⅳ所得气体中SO2的体积分数,取280mL(已折算成标准状况)气体样品与足量Fe2(SO4)3溶液完全反应后,用浓度为0.02000 mol/L的K2Cr2O7标准溶液滴定至终点,消耗K2Cr2O7溶液25.00 mL 。
已知:Cr2O72-+ Fe2++ H+→Cr3++ Fe3++ H2O(未配平)
①SO2通入Fe2(SO4)3溶液,发生反应的离子方程式为 ▲ 。
②反应Ⅳ所得气体中SO2的体积分数为 ▲ 。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】稀土是一种重要的战略资源。氟碳铈矿主要化学成分为CeFCO3,它是提取铈等稀土元素的重要矿物原料。氟碳铈矿的冶炼工艺流程如下:

已知:i.铈的常见化合价为+3、+4。焙烧后铈元素转化成CeO2和CeF4。四价铈不易进入溶液,而三价稀土元素易进入溶液。
ii.酸浸II中发生反应:9CeO2+3CeF4+45HCl+3H3BO3=Ce(BF4)3↓+11CeCl3+6Cl2↑+27H2O
请回答下列问题:
(1)①焙烧氟碳铈矿的目的是_______ 。
②焙烧后产生的CeO2是汽车尾气净化催化剂的关键成分,它能在还原气氛中供氧,在氧化气氛中耗氧。在尾气消除过程中发生着CeO2 CeO2(1-x)+xO2↑的循环。写出CeO2消除CO尾气的化学方程式:
CeO2(1-x)+xO2↑的循环。写出CeO2消除CO尾气的化学方程式:________ 。
(2)在酸浸I中用盐酸浸出时,有少量铈进入滤液,且产生黄绿色气体。少量铈进入稀土溶液发生反应的离子方程式是________ 。
(3)向Ce(BF4)3中加入KCl溶液的目的是______ 。
(4)操作I的名称为_______ ,在实验室中进行操作II时所需要的硅酸盐仪器有_______ 。
(5)“操作I”后,向溶液中加入NaOH溶液来调节溶液的pH,以获得Ce(OH)3沉淀,常温下加入NaOH调节溶液的pH应大于________ 即可认为Ce3+已完全沉淀。(已知:Ksp[Ce(OH)3]=1.0×10-20)
(6)取上述流程中得到的Ce(OH)4产品5.000g,加酸溶解后,向其中加入含0.03300mol FeSO4的FeSO4溶液使Ce4+全部被还原成Ce3+,再用0.1000mol·L-1的酸性KMnO4标准溶液滴定至终点时,消耗20.00mL标准溶液。则该产品中Ce(OH)4的质量分数为______ (已知氧化性:Ce4+>KMnO4;Ce(OH)4的相对分子质量为208,保留3位有效数字)。
(7)在酸性条件下电解Ce2O3制备Ce(SO4)2(如下图),阳极电极反应式_______ 。


已知:i.铈的常见化合价为+3、+4。焙烧后铈元素转化成CeO2和CeF4。四价铈不易进入溶液,而三价稀土元素易进入溶液。
ii.酸浸II中发生反应:9CeO2+3CeF4+45HCl+3H3BO3=Ce(BF4)3↓+11CeCl3+6Cl2↑+27H2O
请回答下列问题:
(1)①焙烧氟碳铈矿的目的是
②焙烧后产生的CeO2是汽车尾气净化催化剂的关键成分,它能在还原气氛中供氧,在氧化气氛中耗氧。在尾气消除过程中发生着CeO2
 CeO2(1-x)+xO2↑的循环。写出CeO2消除CO尾气的化学方程式:
CeO2(1-x)+xO2↑的循环。写出CeO2消除CO尾气的化学方程式:(2)在酸浸I中用盐酸浸出时,有少量铈进入滤液,且产生黄绿色气体。少量铈进入稀土溶液发生反应的离子方程式是
(3)向Ce(BF4)3中加入KCl溶液的目的是
(4)操作I的名称为
(5)“操作I”后,向溶液中加入NaOH溶液来调节溶液的pH,以获得Ce(OH)3沉淀,常温下加入NaOH调节溶液的pH应大于
(6)取上述流程中得到的Ce(OH)4产品5.000g,加酸溶解后,向其中加入含0.03300mol FeSO4的FeSO4溶液使Ce4+全部被还原成Ce3+,再用0.1000mol·L-1的酸性KMnO4标准溶液滴定至终点时,消耗20.00mL标准溶液。则该产品中Ce(OH)4的质量分数为
(7)在酸性条件下电解Ce2O3制备Ce(SO4)2(如下图),阳极电极反应式

您最近一年使用:0次



