下列说法正确的是
| A.SO2与CO2的分子立体构型均为直线形 |
| B.H2O和NH3中的中心原子杂化方式相同 |
| C.SiO2中的键长大于CO2中的键长,所以SiO2的熔点比CO2高 |
| D.凡是具有规则外形的固体都是晶体 |
更新时间:2021-09-09 22:22:10
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】亚铁氯化钾{K4[Fe(CN)4]}的制备方法为Fe+ 6HCN+2K2CO3= K4[Fe(CN)6]+H2↑+2CO2↑+2H2O。设NA为阿伏伽德罗常数,下列说法正确的是
| A.HCN分子中σ键与π键数之比为1:2 |
| B.1 mol K4[Fe(CN)6]中含有12 molσ键 |
| C.反应过程中每生成1 mol CO2转移电子数目为4 NA |
| D.反应所列物质中,碳原子的杂化方式只有1种 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法错误的是
| A.羊毛织品洗后易变形,与氢键有关 |
B.基态 原子中,两种自旋状态的电子数之比为 原子中,两种自旋状态的电子数之比为 |
C.键角: |
D. 二甲醚 二甲醚 中 中 杂化的原子数为2NA 杂化的原子数为2NA |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列说法不正确的是
| A.自然界固氮与工业固氮都是将N2转化为氮的化合物 |
B.NH3中的H-N-H键角小于 |
C. 与 与 中,中心原子的杂化方式相同 中,中心原子的杂化方式相同 |
D. 晶体属于共价晶体 晶体属于共价晶体 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法错误 的是
| A.从CH4、NH4+、SO42-为正四面体结构,可推测PH4+、PO43-也为正四面体结构 |
| B.1mol碳化硅晶体中,平均含有4mol C—Si共价键 |
| C.水的沸点比硫化氢的高,是因为H2O分子间存在氢键,H2S分子间不能形成氢键 |
D.某气态团簇分子结构如图所示,该气态团簇分子的分子式为EF或FE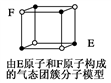 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列各组固体物质熔化或升华所克服的粒子间作用属于同种类型的是
| A.Na2O和晶体硅 | B.碘和干冰 | C.Mg和S | D.氯化钠和蔗糖 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】短周期主族元素X、Y、Z、W、M的原子序数依次增大,且位于三个不同周期,已知基态原子的最高能级上的电子数W是X的4倍,Y与W同主族,Z是地壳中含量最高的金属元素,下列说法正确的是
| A.非金属性:X>Y | B.Z与Y、M形成的常见化合物熔点:Y<M |
| C.简单离子半径:Z>W | D.X与W、M形成的常见化合物还原性:W>M |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列关于晶体的说法正确的组合是
①分子晶体中都存在范德华力和共价键
②在晶体中有阳离子不一定有阴离子
③金刚石、SiC、Si、干冰、冰晶体的熔点依次降低
④离子化合物中只有离子键,分子晶体中肯定没有离子键
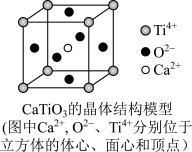
⑤CaTiO3晶体中(晶胞结构如图所示)每个Ti4+和12个O2-相紧邻
⑥1molSiO2晶体中含有2NA个Si-O共价键
⑦晶格能指破坏1mol离子键所吸收的能量
⑧原子晶体融化时只需要破坏共价键

①分子晶体中都存在范德华力和共价键
②在晶体中有阳离子不一定有阴离子
③金刚石、SiC、Si、干冰、冰晶体的熔点依次降低
④离子化合物中只有离子键,分子晶体中肯定没有离子键
⑤CaTiO3晶体中(晶胞结构如图所示)每个Ti4+和12个O2-相紧邻
⑥1molSiO2晶体中含有2NA个Si-O共价键
⑦晶格能指破坏1mol离子键所吸收的能量
⑧原子晶体融化时只需要破坏共价键
| A.①②③⑥⑧ | B.①②④⑥ | C.②⑤⑧ | D.②③⑤⑦⑧ |
您最近半年使用:0次

 的空间结构模型:
的空间结构模型:
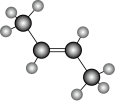
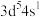

 和CH4
和CH4

