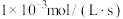反应2NO(g)+2H2(g)=N2(g)+2H2O(g)中,每生成7gN2放出166kJ的热量,该反应的速率表达式为v=k·cm(NO)·cn(H2)(k、m、n待测),其反应包含下列两步:①2NO+H2=N2+H2O2(慢)②H2O2+H2=2H2O(快)
T℃时测得有关实验数据如下:
下列说法错误的是
T℃时测得有关实验数据如下:
| 序号 | c(NO)/(mol·L-1) | c(H2)/(mol·L-1) | 速率/(mol·L-1·min-1) |
| Ⅰ | 0.0060 | 0.0010 | 1.8×10-4 |
| Ⅱ | 0.0060 | 0.0020 | 3.6×10-4 |
| Ⅲ | 0.0010 | 0.0060 | 3.0×10-5 |
| Ⅳ | 0.0020 | 0.0060 | 1.2×10-4 |
| A.整个反应速率由第①步反应决定 |
| B.正反应的活化能一定是①<② |
| C.该反应速率表达式:v=5000c2(NO)·c(H2) |
| D.该反应的热化学方程式为2NO(g)+2H2(g)=N2(g)+2H2O(g)ΔH=-664kJ·mol-1 |
21-22高二上·重庆北碚·阶段练习 查看更多[11]
重庆市西南大学附属中学校2021-2022学年高二上学期第一次定时检测化学试题四川省眉山市仁寿第一中学北校区2021-2022学年高二上学期10月月考化学试题三峡名校联盟2021-2022学年高二上学期联考化学试题山东省东营市广饶县第一中学三校区2022-2023学年高二9月月考化学试题(已下线)第20讲 化学平衡常数及转化率的计算(练)-2023年高考化学一轮复习讲练测(新教材新高考)四川省邻水实验学校2021-2022学年高二上学期期中考试化学试题山东省潍坊第一中学2022-2023学年高二上学期期末考试化学试题(已下线)第1讲 化学反应速率及其影响因素贵州省贵阳市三新改革联盟校2023-2024学年高二上学期10月月考化学试题山东省青岛第六十八中学2023-2024学年高二上学期期中考试化学试卷广东省深圳市蛇口育才教育集团育才中学2023-2024学年高二上学期阶段检测(一)化学试题
更新时间:2021-10-09 16:41:50
|
相似题推荐
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】X(g)+3Y(g) 2Z(g) ΔH=-akJ·mol-1 (a>0),一定条件下,将1molX和3molY通入2L的恒容密闭容器中,反应10min,测得Y的物质的量为2.4mol。下列说法正确的是( )
2Z(g) ΔH=-akJ·mol-1 (a>0),一定条件下,将1molX和3molY通入2L的恒容密闭容器中,反应10min,测得Y的物质的量为2.4mol。下列说法正确的是( )
 2Z(g) ΔH=-akJ·mol-1 (a>0),一定条件下,将1molX和3molY通入2L的恒容密闭容器中,反应10min,测得Y的物质的量为2.4mol。下列说法正确的是( )
2Z(g) ΔH=-akJ·mol-1 (a>0),一定条件下,将1molX和3molY通入2L的恒容密闭容器中,反应10min,测得Y的物质的量为2.4mol。下列说法正确的是( )| A.10min内,Y的平均反应速率为0.03mol·L-1·s-1 |
| B.第10min时,X的反应速率为0.01mol·L-1·min-1 |
| C.10min内,消耗0.2mol X,生成0.4mol Z |
| D.随着反应物量的减少,正反应速率一定逐渐下降。 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】800℃时,在2 L密闭容器中发生反应:2NO(g)+O2(g) 2NO2(g),该反应体系中n(NO)随时间的变化如下表:
2NO2(g),该反应体系中n(NO)随时间的变化如下表:
下列有关说法不正确的是
 2NO2(g),该反应体系中n(NO)随时间的变化如下表:
2NO2(g),该反应体系中n(NO)随时间的变化如下表:| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.022 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
| A.用氧气表示0~3 s内该反应的平均速率ν(O2)=0.0025 mol·L-1·s-1 |
| B.容器内颜色保持不变时,说明该反应达到平衡状态 |
| C.增大氧气的浓度,既加快反应速率,又使平衡正向移动 |
| D.该反应达到平衡时,转移电子总数为0.03NA |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】某课外小组为探究金属铜的还原性,进行如下实验:①将金属铜投入用 酸化的
酸化的 的
的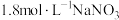 溶液中,现象不明显②将金属铜投入用盐酸酸化的
溶液中,现象不明显②将金属铜投入用盐酸酸化的 的
的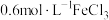 溶液中,铜粉溶解,溶液变为蓝绿色③将金属铜投入用
溶液中,铜粉溶解,溶液变为蓝绿色③将金属铜投入用 酸化的
酸化的 的
的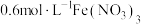 溶液中,铜粉溶解,溶液变为深棕色[经检验含
溶液中,铜粉溶解,溶液变为深棕色[经检验含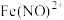 ],无气泡生成。下列分析正确的是
],无气泡生成。下列分析正确的是
 酸化的
酸化的 的
的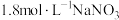 溶液中,现象不明显②将金属铜投入用盐酸酸化的
溶液中,现象不明显②将金属铜投入用盐酸酸化的 的
的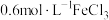 溶液中,铜粉溶解,溶液变为蓝绿色③将金属铜投入用
溶液中,铜粉溶解,溶液变为蓝绿色③将金属铜投入用 酸化的
酸化的 的
的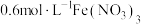 溶液中,铜粉溶解,溶液变为深棕色[经检验含
溶液中,铜粉溶解,溶液变为深棕色[经检验含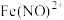 ],无气泡生成。下列分析正确的是
],无气泡生成。下列分析正确的是A.①说明 的 的 溶液不与铜粉反应 溶液不与铜粉反应 |
B.②证明氧化性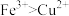 还原性 还原性 |
C.③中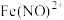 的生成速率一定小于 的生成速率一定小于 被还原的速率 被还原的速率 |
| D.在①中加入少量绿矾,铜粉可溶解,溶液变为深棕色 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】生产环氧乙烷( )的反应为: 2CH2=CH2(g) + O2(g)
)的反应为: 2CH2=CH2(g) + O2(g)  2
2  (g) △H=-106 kJ/mol
(g) △H=-106 kJ/mol
其反应机理如下:
①Ag + O2→AgO2 慢 ②CH2=CH2 + AgO2→ +AgO 快
+AgO 快
③CH2=CH2 + 6AgO→2CO2+2H2O+6Ag 快
下列有关该反应的说法正确的是( )
 )的反应为: 2CH2=CH2(g) + O2(g)
)的反应为: 2CH2=CH2(g) + O2(g)  2
2  (g) △H=-106 kJ/mol
(g) △H=-106 kJ/mol其反应机理如下:
①Ag + O2→AgO2 慢 ②CH2=CH2 + AgO2→
 +AgO 快
+AgO 快③CH2=CH2 + 6AgO→2CO2+2H2O+6Ag 快
下列有关该反应的说法正确的是( )
| A.反应的活化能等于 106 kJ/mol | B.AgO2也是该反应的催化剂 |
| C.增大乙烯的浓度能显著提高环氧乙烷的生成速率 | D.该反应的原子利用率为100% |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
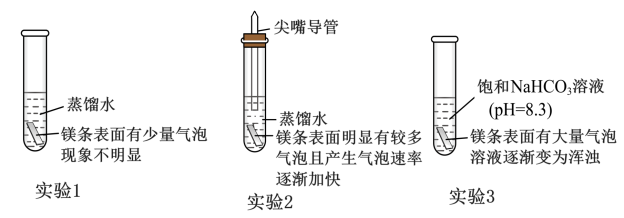
【推荐3】如图表示室温下用砂纸打磨过的镁条与水反应的探究实验,实验2的镁条放在尖嘴玻璃导管内并浸于蒸馏水中,实验3产生的浑浊物主要为碱式碳酸镁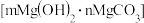 。下列说法错误的是
。下列说法错误的是
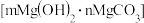 。下列说法错误的是
。下列说法错误的是
A.实验1现象不明显,可能与 Mg 表面生成了难溶的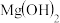 有关 有关 |
| B.实验2比实验1现象更明显,可能是由于玻璃管空间狭小热量不易散失 |
| C.由实验1和实验3可得出“碱性增强有利于加快镁与水反应速率”的结论 |
D.实验3中 破坏了 破坏了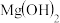 在镁条表面的沉积,增大了镁与水的接触面积 在镁条表面的沉积,增大了镁与水的接触面积 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】恒容密闭容器中充入X,在催化剂作用下发生反应: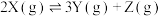 ,起始压强为p kPa,反应时间为t s,测得X的转化率随温度变化如图中实线所示,虚线表示X平衡转化率。下列说法正确的是
,起始压强为p kPa,反应时间为t s,测得X的转化率随温度变化如图中实线所示,虚线表示X平衡转化率。下列说法正确的是
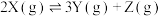 ,起始压强为p kPa,反应时间为t s,测得X的转化率随温度变化如图中实线所示,虚线表示X平衡转化率。下列说法正确的是
,起始压强为p kPa,反应时间为t s,测得X的转化率随温度变化如图中实线所示,虚线表示X平衡转化率。下列说法正确的是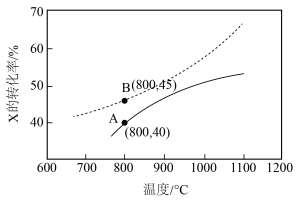
| A.该反应的ΔH<0 |
| B.催化剂可降低该反应的焓变,但不能提高平衡转化率 |
| C.通过延长反应时间,X的转化率能从A点交到B点 |
D.800℃时,A点物质X在0~t s内化学反应速率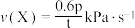 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】将4 mol A气体和2 mol B气体置于2L的密闭容器中,混合后发生如下反应:2A(g)+ B(g) = 2C(g)。若经2 s后测得C的浓度为1.2 mol/L,下列说法正确的是
| A.用物质A表示的反应速率为1.2 mol / (L • s) |
| B.用物质B表示的反应速率为0.3 mol / (L • s) |
| C.2 s时物质A的转化率为30% |
| D.2 s时物质B的浓度为0.6 mol / L |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】室温下过氧化铬( )在硝酸酸化的戊醇中会溶解并发生反应:
)在硝酸酸化的戊醇中会溶解并发生反应: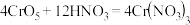
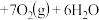 。在5m1
。在5m1 的过氧化铬戊醇溶液中滴入一定量的稀硝酸,在不同时刻测得过氧化铬浓度如下表:
的过氧化铬戊醇溶液中滴入一定量的稀硝酸,在不同时刻测得过氧化铬浓度如下表:
下列叙述正确的是
 )在硝酸酸化的戊醇中会溶解并发生反应:
)在硝酸酸化的戊醇中会溶解并发生反应: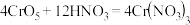
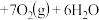 。在5m1
。在5m1 的过氧化铬戊醇溶液中滴入一定量的稀硝酸,在不同时刻测得过氧化铬浓度如下表:
的过氧化铬戊醇溶液中滴入一定量的稀硝酸,在不同时刻测得过氧化铬浓度如下表:| 时间/min | 4 | 6 | 8 | 10 | t | 20 | 25 | 35 |
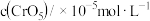 | 4.230 | 2.510 | 1.790 | 1.350 | 1.240 | 1.130 | 1.110 | 1.100 |
A.4~6min内过氧化铬分解的平均速率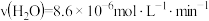 |
B.8~10min内过氧化铬分解释放的 体积为0.86mL(标准状况) 体积为0.86mL(标准状况) |
| C.推测表中t的取值范围为:10<t<15 |
D.若升高温度后重新实验发现20min时过氧化铬浓度为 ,则证明反应的△H>0 ,则证明反应的△H>0 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】在溶液中,反应A+2B C分别在三种不同实验条件下进行,它们的起始状态均为c(A)=0.100 mol·L-1、c(B)=0.200 mol·L-1、c(C)=0 mol·L-1。在三种条件下,反应物A的浓度随时间的变化如图所示。下列说法中正确的是
C分别在三种不同实验条件下进行,它们的起始状态均为c(A)=0.100 mol·L-1、c(B)=0.200 mol·L-1、c(C)=0 mol·L-1。在三种条件下,反应物A的浓度随时间的变化如图所示。下列说法中正确的是

 C分别在三种不同实验条件下进行,它们的起始状态均为c(A)=0.100 mol·L-1、c(B)=0.200 mol·L-1、c(C)=0 mol·L-1。在三种条件下,反应物A的浓度随时间的变化如图所示。下列说法中正确的是
C分别在三种不同实验条件下进行,它们的起始状态均为c(A)=0.100 mol·L-1、c(B)=0.200 mol·L-1、c(C)=0 mol·L-1。在三种条件下,反应物A的浓度随时间的变化如图所示。下列说法中正确的是
| A.反应的平衡常数:①<② |
B.反应A+2B C的ΔH>0 C的ΔH>0 |
| C.实验②平衡时B的转化率为60% |
| D.实验③平衡时c(C)=0.040 mol·L-1 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】在一定条件下,将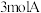 和
和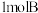 两种气体混合于固定容积为
两种气体混合于固定容积为 的密闭容器中,发生如下反应:
的密闭容器中,发生如下反应: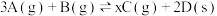 。
。 时该反应达到平衡,生成了
时该反应达到平衡,生成了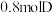 ,并测得
,并测得 的浓度为
的浓度为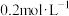 。下列判断错误的是
。下列判断错误的是
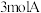 和
和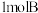 两种气体混合于固定容积为
两种气体混合于固定容积为 的密闭容器中,发生如下反应:
的密闭容器中,发生如下反应: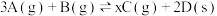 。
。 时该反应达到平衡,生成了
时该反应达到平衡,生成了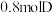 ,并测得
,并测得 的浓度为
的浓度为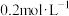 。下列判断错误的是
。下列判断错误的是A. |
B.平衡时 与 与 的浓度之比为 的浓度之比为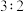 |
C.平衡时 与 与 的转化率相等,均为 的转化率相等,均为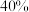 |
| D.充入稀有气体增大体系压强,可提高该反应的反应速率 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐3】某温度下,降冰片烯在钛杂环丁烷催化发生聚合反应:n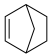

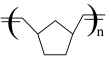 。在不同时刻测得反应物浓度与时间关系如下表:
。在不同时刻测得反应物浓度与时间关系如下表:
下列说法正确的是


 。在不同时刻测得反应物浓度与时间关系如下表:
。在不同时刻测得反应物浓度与时间关系如下表:| t/min | 0 | 25 | 75 | 105 | 125 | 150 | 250 |
| c(降冰片烯)/(mol·L-1) | 3.00 | 2.70 | a | 1.74 | 1.50 | 1.20 | 0 |
| A.推测上表中的a>2.10 |
| B.若将钛杂环丁烷催化剂制成蜂窝形状可提高该反应的平衡转化率 |
| C.105-155min,生成聚降冰片烯的平均速率为0.012mol·L-1·min-1 |
| D.其他条件相同时,若将降冰片烯起始浓度减少为1.5mol/L,则该反应速率不变 |
您最近一年使用:0次

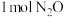 和4molCO,发生反应
和4molCO,发生反应
 。已知:
。已知: 、
、 分别是正、逆反应速率常数,
分别是正、逆反应速率常数, ,
,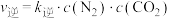 ,A、B容器中
,A、B容器中 的转化率随时间的变化关系如图所示。下列说法中正确的是
的转化率随时间的变化关系如图所示。下列说法中正确的是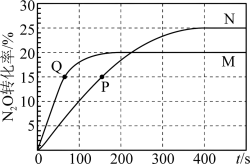
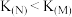
 与
与 浓度比为1∶1时,标志此反应已达平衡
浓度比为1∶1时,标志此反应已达平衡