 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ⑪ | ⑫ |
(1)写出⑧的元素名称
(2)画出②的原子原子结构示意图
(3)在这些元素中,(用元素符号填写,下同)最活泼的非金属元素:
(4)以上元素的最高价氧化物的对应水化物中,碱性最强的是
(5)⑤和⑪形成的化合物的电子式为
相似题推荐

(1)元素④在元素周期表中的位置为
(2)最高价氧化物的水化物中碱性最强的物质的化学式为
(3)写出②和⑦两种元素的最高价氧化物的水化物相互反应的化学方程式:
(4)④、⑤、⑥三种元素按原子半径由大到小的顺序排列为
(5)分别画出③的原子结构示意图和⑦的离子结构示意图
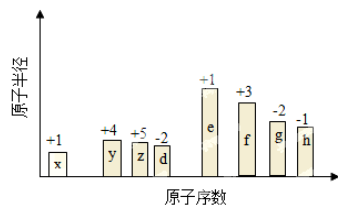
回答下列问题:
(1)H的离子结构示意图为
(2)由E和D两元素形成的原子个数比为1∶1的化合物的电子式为
(3)单质G易溶于YG2,则YG2的结构式为
(4)Z2X4是一种高效清洁的火箭燃料,8g该物质含有的共用电子对数目为
(5)上述元素可组成盐R:ZX4F(GD4)2。向盛有10mL1mol·L-1R溶液的烧杯中滴加1mol·L-1NaOH溶液,沉淀物质的量随NaOH溶液体积的变化如图所示,则m点对应的离子方程式为

| 元素 | 结构、性质等信息 |
| A | 是短周期中(除稀有气体外)原子半径最大的元素,该元素的某种合金是原子反应堆的导热剂 |
| B | 与A同周期,其最高价氧化物的水化物呈两性 |
| C | 元素的气态氢化物极易溶于水,可用作制冷剂 |
| D | 是海水中除氢、氧元素外含量最多的元素,其单质或化合物是自来水生产过程中常用的消毒杀菌剂 |
(1)A的原子结构示意图是
(2)元素B在周期表中的位置是
(3)单质C的结构式是
(4)A、B的最高价氧化物对应的水化物相互反应的离子方程式为
(5)C、D的氢化物相互反应后,将产物溶于水,水溶液呈
【推荐1】在2008年初我国南方遭遇的冰雪灾害中,使用了一种融雪剂,其主要成分的化学式为XY2,X、Y均为周期表前20号元素,其阳离子和阴离子的电子层结构相同,且1mol XY2含有54mol电子。
(1)该融雪剂的化学式是
(2)元素D、E原子的最外层电子数是其电子层数的2倍,D与Y相邻,则D的离子结构示意图是
(3)Z与Y同主族,Z、Y位于相邻周期,且Z的原子半径大,则Z单质常温下呈
(4)元素W与D同主族,且W与D可形成两种常见化合物,其中能使品红溶液褪色的是
(5)元素R与Y同主族,其氢化物能用于刻蚀玻璃,R2与NaOH溶液反应的产物之一是OR2(R为1价),该反应的离子方程式为
(1)E元素的离子结构示意图为
(2)比较元素C、E的氢化物沸点高低,HnC
(3)B的氢化物与其最高价氧化物对应的水化物反应生成盐的化学方程式
(4)由C、D、E中的两种元素组成的两种化合物发生的反应既属于化合反应又属于氧化还原反应,该反应的化学方程式为
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA |  |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 四 | ⑩ | ⑪ | ⑫ |
(2)写出元素①对应气态氢化物的化学式和电子式:
(3)在元素③和④中,单质与水反应较剧烈的是
(4)在元素③、④与⑤的最高价氧化物对应的水化物中,碱性最弱是
(5)能证明⑧和⑫单质氧化性强弱的实验事实
 用离子方程式表示)是
用离子方程式表示)是(1)A在元素周期表中的位置为
(2)上述元素的最高价氧化物对应的水化物中碱性最强的是
(3)写出C2B2的电子式:
(4)写出D的最高价氧化物对应水化物溶于稀硫酸的离子方程式:
(5)写出单质E与NaOH溶液反应的化学方程式:
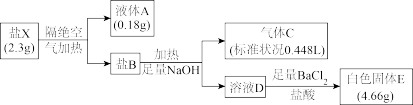
已知:气体C能使湿润红色石蕊变蓝。
请回答:
(1)盐X含
(2)盐X与足量NaOH溶液在加热条件下的离子方程式
(3)盐B对应的酸常温常压下为无色结晶性粉末,主要用于氧化剂、磺化剂及硝化反应中的脱水剂,制染料、炸药,石油产品精制和其他有机磺酸化合物。根据以上信息判断,下列物质中一定条件下能与该酸反应的是_______。
| A.甲苯 | B. | C. | D.Cu |
 反应的化学方程式
反应的化学方程式(1)D在周期表中的位置
(2)E元素形成最高价氧化物对应的水化物的化学式为
(3)元素C、D、E形成的原子半径大小关系是
(4)C、D可形成化合物D2C2,D2C2含有的化学键是
(5)A、C两种元素形成的原子个数之比为1:1的化合物电子式
(6)B的氢化物与B的最高价氧化物的水化物反应的离子方程式

回答下列问题:
(1)h元素的名称是
(2)f的最高价氧化物对应的水化物的化学式
(3)b、c、d、e的原子半径依次
(4)e、h元素的氢化物中,热稳定性大的是
(5)化合物f2d2与化合物 a2d 反应的离子方程式
(6)工业上冶炼g元素的单质的化学方程式
(1)硅原子核外电子的运动状态有
(2)非金属性:S小于O。试用一个实验事实说明
(3)一定温度下,对于可逆反应N2(g)+3H2(g)
 2NH3(g)(正反应放热)的下列叙述,不能说明反应已达化学平衡状态的是_____。
2NH3(g)(正反应放热)的下列叙述,不能说明反应已达化学平衡状态的是_____。| A.单位时间内断裂amolN≡N键,同时断裂6amolN—H键 |
| B.NH3的生成速率与H2的生成速率之比为2∶3 |
| C.恒压容器内混合气体的总物质的量不再变化 |
| D.恒容容器内混合气体的密度不再变化 |

(1)⑨的阴离子结构示意图为
(2)⑤和⑥形成的化合物的电子式为
(3)③、⑧的最高价氧化物对应水化物的酸性由强到弱的顺序为
II.某同学欲利用下图装置验证同周期或同主族元素性质递变规律。

(4)干燥管D的作用是
(5)证明非金属性:Cl>I。在A中加浓盐酸,B中加KMnO4(KMnO4与浓盐酸常温下反应生成氯气),C中加淀粉碘化钾混合溶液,观察到C中溶液变蓝,则C试管中发生反应的离子方程式为
(6)证明非金属性:S>C,在A中加稀硫酸,B中加碳酸钠,C中加澄清石灰水;观察到C中溶液变浑浊的现象,该实验设计的原理是利用



