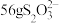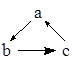从某阳极泥经焙烧后得到的烧渣(成分为CuO、 、
、 、Ag、Au和Pt)中回收贵重金属的工艺流程如图所示。下列说法正确的是
、Ag、Au和Pt)中回收贵重金属的工艺流程如图所示。下列说法正确的是

 、
、 、Ag、Au和Pt)中回收贵重金属的工艺流程如图所示。下列说法正确的是
、Ag、Au和Pt)中回收贵重金属的工艺流程如图所示。下列说法正确的是
A.“酸浸氧化”时 发生反应的离子方程式: 发生反应的离子方程式: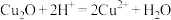 |
B.“滤液”中的金属阳离子有 、 、 和 和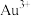 |
C.若“酸溶”得到的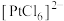 和 和 的物质的量均为1mol,则消耗的氯气至少为3.5mol 的物质的量均为1mol,则消耗的氯气至少为3.5mol |
D.“转化”时发生的反应中 作还原剂 作还原剂 |
更新时间:2021-10-10 14:23:26
|
相似题推荐
单选题
|
较难
(0.4)
【推荐1】解释下列事实的方程式正确的是
A.加热可增强纯碱溶液去污能力:CO32﹣+2H2O H2CO3+2OH﹣ H2CO3+2OH﹣ |
| B.用醋酸溶液除水垢中的CaCO3:CaCO3+2H+=Ca2++H2O+CO2↑ |
C.向煤中加入石灰石可减少煤燃烧时SO2的排放:2CaCO3+O2+2SO2 2CO2+2CaSO4 2CO2+2CaSO4 |
| D.用FeS 除去工业废水中的Hg2+:Hg2++S2-=HgS↓ |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】下列各组溶液,无论将少量前者滴入后者,还是将少量后者滴入前者,生成物一定相同的是
| A.NaOH溶液和AlCl3溶液 | B.FeBr2溶液和氯水 |
| C.NaHCO3溶液和澄清石灰水 | D.Ca(HCO3)2溶液和澄清石灰水 |
您最近一年使用:0次
【推荐1】用0.2mol/L Na2SO3溶液32mL,还原含4×10-3mol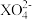 的溶液,过量的Na2SO3用0.2mol/L KMnO4酸性溶液氧化(其中KMnO4被还原成Mn2+),共消耗KMnO4溶液0.8mL,则元素X在还原产物中的化合价是
的溶液,过量的Na2SO3用0.2mol/L KMnO4酸性溶液氧化(其中KMnO4被还原成Mn2+),共消耗KMnO4溶液0.8mL,则元素X在还原产物中的化合价是
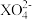 的溶液,过量的Na2SO3用0.2mol/L KMnO4酸性溶液氧化(其中KMnO4被还原成Mn2+),共消耗KMnO4溶液0.8mL,则元素X在还原产物中的化合价是
的溶液,过量的Na2SO3用0.2mol/L KMnO4酸性溶液氧化(其中KMnO4被还原成Mn2+),共消耗KMnO4溶液0.8mL,则元素X在还原产物中的化合价是| A.+1 | B.+2 | C.+3 | D.+4 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】把22.4g铁粉完全溶解于某浓度的硝酸中,如反应只收集到0.3 mol NO2和0.2 mol NO,下列说法正确的是
| A.反应后生成的盐只为Fe(NO3)3 |
| B.反应后生成的盐只为Fe(NO3)2 |
| C.反应后生成的盐为Fe(NO3)3和Fe(NO3)2,其物质的量之比为1∶3 |
| D.反应后生成的盐为Fe(NO3)3和Fe(NO3)2,其物质的量之比为3∶1 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】某固体粉末含Fe3O4、CuCO3、Cu2O、Al2O3、MgCO3中的一种或几种,某化学兴趣小组按如下方案进行实验探究。已知:Cu2O+2HCl=Cu+CuCl2+H2O,下列对实验结果的分析合理的是( )
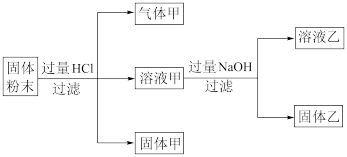

| A.溶液乙中溶质至少2种及以上 |
| B.固体乙中成分至少2种及以上 |
| C.固体粉末中一定含有Cu2O、Al2O3、MgCO3 |
| D.溶液甲中可能含有Fe3+ |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】CuCO3和Cu2(OH)2CO3的混合物34.6g,可恰好完全溶解于300mL 2mol /L的盐酸中,若加热分解等量的这种混合物可得CuO固体质量为
| A.16.0g | B.19.2g | C.24.0g | D.30.6g |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】锌冶炼过程中会产生大量的铅浮渣,其主要成分是PbO、Pb,还含有少量Ag、Zn、CaO和其他不溶于硝酸的杂质。利用铅浮渣生产硫酸铅的流程如下。下列说法不正确的是
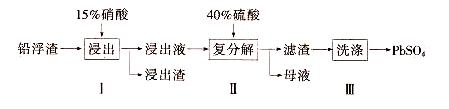

A.步骤Ⅰ中反应的离子方程式是:Pb+4H++2NO =Pb2++2NO↑+2H2O =Pb2++2NO↑+2H2O |
| B.复分解反应的方程式是:Pb(NO3)2+H2SO4= PbSO4↓+2HNO3 |
| C.为保证产品纯度,需控制硝酸的量以为防止Ag被溶解 |
| D.步骤Ⅱ得到的粗产品PbSO4 含有少量CaSO4杂质,还需用Pb(NO3)2溶液多次洗涤 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】下列除去杂质的方法不正确的是
| A.镁粉中混有少量铝粉:加入过量烧碱溶液充分反应,过滤、洗涤、干燥 |
| B.用过量氨水除去Fe3+溶液中的少Al3+ |
| C.Al(OH)3中混有少量Mg(OH)2:加入足量烧碱溶液,充分反应,过滤,向滤液中通过量CO2后过滤 |
| D.CO气体中混有CO2气体:通过NaOH溶液洗气后干燥 |
您最近一年使用:0次

 +
+ +Ba2++OH-=BaSO4↓+NH3·H2O
+Ba2++OH-=BaSO4↓+NH3·H2O +OH-=H2O+CaCO3↓
+OH-=H2O+CaCO3↓ 纳米颗粒的总反应如下:3Fe2++2
纳米颗粒的总反应如下:3Fe2++2 +O2+4OH-=Fe3O4+
+O2+4OH-=Fe3O4+ +2H2O。下列说法正确的是
+2H2O。下列说法正确的是 氧化了
氧化了

 和
和