工业上,常用过二硫酸铵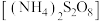 溶液检验废水中的
溶液检验废水中的 (无色)。离子方程式为
(无色)。离子方程式为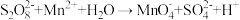 (未配平)。
(未配平)。
(1)已知 分子中S元素为最高价态,则分子中
分子中S元素为最高价态,则分子中 价O与
价O与 价O的个数比为
价O的个数比为___________ 。
(2)上述反应中,还原产物是___________ 。
(3)某实验需要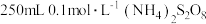 溶液,用
溶液,用 固体配制该溶液时,如果配制过程中,漏掉了“洗涤烧杯和玻璃棒”步骤,配制的浓度将
固体配制该溶液时,如果配制过程中,漏掉了“洗涤烧杯和玻璃棒”步骤,配制的浓度将___________ (填“偏高”、“偏低”或“无影响”)。
(4)测定废水中 的浓度:取
的浓度:取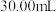 废水于锥形瓶中,滴加
废水于锥形瓶中,滴加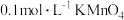 溶液产生黑色
溶液产生黑色 浑浊,至溶液变为浅红色且半分钟内不褪色时,消耗
浑浊,至溶液变为浅红色且半分钟内不褪色时,消耗 溶液
溶液 (假设废水中其他杂质不参与反应)。该废水中
(假设废水中其他杂质不参与反应)。该废水中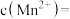
___________  。
。
(5)设计简易实验证明处理后的废水中含有 :
:___________ 。
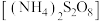 溶液检验废水中的
溶液检验废水中的 (无色)。离子方程式为
(无色)。离子方程式为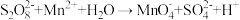 (未配平)。
(未配平)。(1)已知
 分子中S元素为最高价态,则分子中
分子中S元素为最高价态,则分子中 价O与
价O与 价O的个数比为
价O的个数比为(2)上述反应中,还原产物是
(3)某实验需要
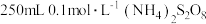 溶液,用
溶液,用 固体配制该溶液时,如果配制过程中,漏掉了“洗涤烧杯和玻璃棒”步骤,配制的浓度将
固体配制该溶液时,如果配制过程中,漏掉了“洗涤烧杯和玻璃棒”步骤,配制的浓度将(4)测定废水中
 的浓度:取
的浓度:取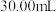 废水于锥形瓶中,滴加
废水于锥形瓶中,滴加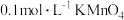 溶液产生黑色
溶液产生黑色 浑浊,至溶液变为浅红色且半分钟内不褪色时,消耗
浑浊,至溶液变为浅红色且半分钟内不褪色时,消耗 溶液
溶液 (假设废水中其他杂质不参与反应)。该废水中
(假设废水中其他杂质不参与反应)。该废水中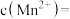
 。
。(5)设计简易实验证明处理后的废水中含有
 :
:
更新时间:2021-10-15 00:02:25
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】利用“价类二维图”研究物质的性质是化学研究的重要手段。如图是氯元素的化合价与部分物质类别的对应关系。
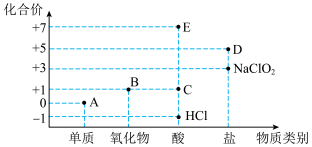
(1)物质E的化学式为___________
(2)A、B、C、D(钾盐)四种物质中,属于电解质的是___________ (填化学式)
(3)A与水反应的离子方程式为___________
(4)B为酸性氧化物,则B与氢氧化钠溶液反应的化学方程式为___________
(5)已知A与氢氧化钠溶液反应生成 和
和 的混合物,若
的混合物,若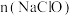 与
与 之比为2:3,则氧化剂与还原剂的物质的量之比为
之比为2:3,则氧化剂与还原剂的物质的量之比为___________
(6)已知二氧化氯( )为高效无毒的消毒剂,实际消毒效果比物质A要好。在室温及标准大气压的条件下,等物质的量的
)为高效无毒的消毒剂,实际消毒效果比物质A要好。在室温及标准大气压的条件下,等物质的量的 和物质A比较,所含的原子总数之比为
和物质A比较,所含的原子总数之比为___________ ,电子数目之比为___________ 。
(7)氯碱工业指的是工业上用电解饱和食盐水的方法,制取氯气和烧碱等主要产品,在国民经济和国防建设中占有重要地位。请写出氯化钠溶液在通电条件下,发生反应的离子方程式___________ 。

(1)物质E的化学式为
(2)A、B、C、D(钾盐)四种物质中,属于电解质的是
(3)A与水反应的离子方程式为
(4)B为酸性氧化物,则B与氢氧化钠溶液反应的化学方程式为
(5)已知A与氢氧化钠溶液反应生成
 和
和 的混合物,若
的混合物,若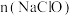 与
与 之比为2:3,则氧化剂与还原剂的物质的量之比为
之比为2:3,则氧化剂与还原剂的物质的量之比为(6)已知二氧化氯(
 )为高效无毒的消毒剂,实际消毒效果比物质A要好。在室温及标准大气压的条件下,等物质的量的
)为高效无毒的消毒剂,实际消毒效果比物质A要好。在室温及标准大气压的条件下,等物质的量的 和物质A比较,所含的原子总数之比为
和物质A比较,所含的原子总数之比为(7)氯碱工业指的是工业上用电解饱和食盐水的方法,制取氯气和烧碱等主要产品,在国民经济和国防建设中占有重要地位。请写出氯化钠溶液在通电条件下,发生反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氧化还原反应和离子反应在生产生活中有重要的应用,请用所学知识回答问题。
Ⅰ.实验室模拟工业处理含铬废水,操作及现象如图甲所示,反应过程中铬元素的化合价变化如图乙。已知:深蓝色溶液中生成了 。
。
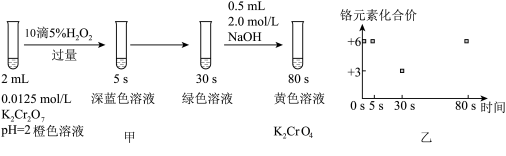
(1)0s~80s时,溶液中含铬微粒依次发生_______ 反应、_______ 反应和_______ 反应(选填“氧化”“还原”“既有氧化又有还原”、“非氧化还原”)
(2)实验开始至30s,溶液中发生的总反应离子方程式为: ,补全并配平反应方程式
,补全并配平反应方程式______ 。标准状况下每生成2.24L 转移的电子数为:
转移的电子数为:_______ 。
Ⅱ.氯水具有杀菌消毒漂白的作用。
(3)写出氯气溶于水发生反应的离子方程式:_______ 。
(4)某学习小组拟用手持技术对新制饱和氯水进行检测,下列图像变化最有可能是其检测结果的是_______ 。
结合相应的化学用语,解释氯水久置后产生你所选择的图像变化的原因。_______ 。
Ⅰ.实验室模拟工业处理含铬废水,操作及现象如图甲所示,反应过程中铬元素的化合价变化如图乙。已知:深蓝色溶液中生成了
 。
。
(1)0s~80s时,溶液中含铬微粒依次发生
(2)实验开始至30s,溶液中发生的总反应离子方程式为:
 ,补全并配平反应方程式
,补全并配平反应方程式 转移的电子数为:
转移的电子数为:Ⅱ.氯水具有杀菌消毒漂白的作用。
(3)写出氯气溶于水发生反应的离子方程式:
(4)某学习小组拟用手持技术对新制饱和氯水进行检测,下列图像变化最有可能是其检测结果的是
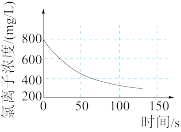 | 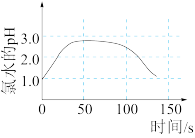 |
| A.溶液中氯离子浓度随时间的变 | B.氯水pH随时间的变化 |
 | 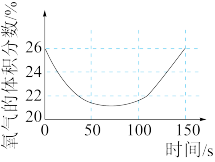 |
| C.氯水的导电能力随时间的变化 | D.液面上方氧气体积分数随时间的变化 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】新型陶瓷材料氮化硅(Si3N4)可用于制作火箭发动机中燃料的喷嘴。氮化硅可由石英、焦炭在高温氮气流中制取。完成下列填空:
SiO2 +______C +_____N2 ______Si3N4 + ________CO
______Si3N4 + ________CO
(1)试配平该化学反应方程式,在方程式上标出电子转移的方向和数目_____ 。
(2)反应中___________ 被还原,当氧化产物比还原产物多1mol时,反应中电子转移数为___________ 。
(3)在该反应体系中:所涉及物质属于单质的电子式为___________ ;所涉及元素中原子半径最大的原子的结构示意图为___________ 。
SiO2 +______C +_____N2
 ______Si3N4 + ________CO
______Si3N4 + ________CO(1)试配平该化学反应方程式,在方程式上标出电子转移的方向和数目
(2)反应中
(3)在该反应体系中:所涉及物质属于单质的电子式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】臭氧有强氧化性能在一定条件下将烟气中的 、
、 分别氧化为
分别氧化为 和
和 。臭氧可用于净化空气,饮用水消毒,处理工业废物和作为漂白剂。
。臭氧可用于净化空气,饮用水消毒,处理工业废物和作为漂白剂。
(1) 中心原子轨道的杂化类型为
中心原子轨道的杂化类型为_______ ; 的空间构型为
的空间构型为_______ (用文字描述)。
(2) 基态核外外层电子排布式为
基态核外外层电子排布式为_______ 。
(3)臭氧可用于含 碱性电镀废水的处理。第ⅰ步:
碱性电镀废水的处理。第ⅰ步: 转化为
转化为 ;第ⅱ步:
;第ⅱ步: 继续转化为
继续转化为 及两种单质气体。若第ⅱ步转化时,
及两种单质气体。若第ⅱ步转化时, 与
与 物质的量之比为3:2,该步反应的离子方程式为
物质的量之比为3:2,该步反应的离子方程式为_______ 。
(4)为测定大气中臭氧( )含量,将0℃、
)含量,将0℃、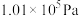 的空气V L慢慢通过足量KI溶液,使臭氧完全反应:然后将所得溶液用a mL的c mol/L
的空气V L慢慢通过足量KI溶液,使臭氧完全反应:然后将所得溶液用a mL的c mol/L 溶液进行滴定恰好到达终点。(已知:
溶液进行滴定恰好到达终点。(已知: )
)
① 与KI溶液反应生成两种单质,则反应的化学方程式
与KI溶液反应生成两种单质,则反应的化学方程式_______ 。
②该滴定实验中除烧杯、锥形瓶外,还需要的玻璃仪器是_______ ;
③该实验中可选用_______ (填物质名称)作指示剂。空气中臭氧的体积分数为_______ 。
④甲同学认为在滴定前应微热溶液、以排除溶液中溶解的 和
和 ,不然会使滴定结果偏
,不然会使滴定结果偏_______ (填“低”或“高”)。
 、
、 分别氧化为
分别氧化为 和
和 。臭氧可用于净化空气,饮用水消毒,处理工业废物和作为漂白剂。
。臭氧可用于净化空气,饮用水消毒,处理工业废物和作为漂白剂。(1)
 中心原子轨道的杂化类型为
中心原子轨道的杂化类型为 的空间构型为
的空间构型为(2)
 基态核外外层电子排布式为
基态核外外层电子排布式为(3)臭氧可用于含
 碱性电镀废水的处理。第ⅰ步:
碱性电镀废水的处理。第ⅰ步: 转化为
转化为 ;第ⅱ步:
;第ⅱ步: 继续转化为
继续转化为 及两种单质气体。若第ⅱ步转化时,
及两种单质气体。若第ⅱ步转化时, 与
与 物质的量之比为3:2,该步反应的离子方程式为
物质的量之比为3:2,该步反应的离子方程式为(4)为测定大气中臭氧(
 )含量,将0℃、
)含量,将0℃、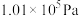 的空气V L慢慢通过足量KI溶液,使臭氧完全反应:然后将所得溶液用a mL的c mol/L
的空气V L慢慢通过足量KI溶液,使臭氧完全反应:然后将所得溶液用a mL的c mol/L 溶液进行滴定恰好到达终点。(已知:
溶液进行滴定恰好到达终点。(已知: )
)①
 与KI溶液反应生成两种单质,则反应的化学方程式
与KI溶液反应生成两种单质,则反应的化学方程式②该滴定实验中除烧杯、锥形瓶外,还需要的玻璃仪器是
③该实验中可选用
④甲同学认为在滴定前应微热溶液、以排除溶液中溶解的
 和
和 ,不然会使滴定结果偏
,不然会使滴定结果偏
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】KBr可用于光谱分析和化学分析等。
(1)制备KBr的一种方法如下:80℃时,向溶有CO(NH2)2的KOH溶液中缓慢加入Br2,至pH为6~7时反应完全,生成CO2、N2等。该反应的化学方程式为_____ 。
(2)KBr可用于测定苯酚(C6H5OH)样品的纯度,方法如下:取0.5000g苯酚试样,用NaOH溶液溶解后定容成250.00mL溶液;移取25.00mL该溶液,加入25.00mL0.03000mol•L﹣1的KBrO3(含过量KBr)标准溶液,然后加入足量盐酸,充分反应后再加足量KI溶液,充分反应;用0.1000mol•L﹣1Na2S2O3溶液滴定至淡黄色,加入指示剂,继续滴定至终点,用去16.20mL。测定过程中物质的转化关系如下:

①加入的指示剂为_____ 。
②计算苯酚样品的纯度(写出计算过程)_____ 。
(1)制备KBr的一种方法如下:80℃时,向溶有CO(NH2)2的KOH溶液中缓慢加入Br2,至pH为6~7时反应完全,生成CO2、N2等。该反应的化学方程式为
(2)KBr可用于测定苯酚(C6H5OH)样品的纯度,方法如下:取0.5000g苯酚试样,用NaOH溶液溶解后定容成250.00mL溶液;移取25.00mL该溶液,加入25.00mL0.03000mol•L﹣1的KBrO3(含过量KBr)标准溶液,然后加入足量盐酸,充分反应后再加足量KI溶液,充分反应;用0.1000mol•L﹣1Na2S2O3溶液滴定至淡黄色,加入指示剂,继续滴定至终点,用去16.20mL。测定过程中物质的转化关系如下:

①加入的指示剂为
②计算苯酚样品的纯度(写出计算过程)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】分析、归纳、探究是学习化学的重要方法和手段之一、下面就电解质A回答有关问题(假定以下都是室温时的溶液)。
(1)电解质A的化学式为NanB,测得浓度为c mol/L的A溶液的pH=a。
①试说明HnB的酸性强弱_______ 。
②当a=10时,A溶液呈碱性的原因是(用离子方式程式表示)_______ 。
③当a=10、n=1时,A溶液中各种离子浓度由大到小的顺序为_______ 。c(OH-)-c(HB)=_______ 。
④当n=1、c=0.1、溶液中c(HB)∶c(B-)=1∶99时,A溶液的pH为_______ (保留整数值)。
(2)已知难溶电解质A的化学式为XnYm,相对分子质量为M,测得其饱和溶液的密度为ρ g/cm3,Xm+离子的浓度为c mol/L,则该难溶物XnYm的溶度积常数为Ksp=_______ ,该温度下XnYm的溶解度S=_______ 。
(1)电解质A的化学式为NanB,测得浓度为c mol/L的A溶液的pH=a。
①试说明HnB的酸性强弱
②当a=10时,A溶液呈碱性的原因是(用离子方式程式表示)
③当a=10、n=1时,A溶液中各种离子浓度由大到小的顺序为
④当n=1、c=0.1、溶液中c(HB)∶c(B-)=1∶99时,A溶液的pH为
(2)已知难溶电解质A的化学式为XnYm,相对分子质量为M,测得其饱和溶液的密度为ρ g/cm3,Xm+离子的浓度为c mol/L,则该难溶物XnYm的溶度积常数为Ksp=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】碘是人体不可缺少的元素,为了防止碘缺乏,现在市场上流行一种加碘盐,就是在精盐中添加一定量的KIO3进去。某研究小组为了检测某加碘盐中是否含有碘,查阅了有关的资料,发现其检测原理是:在溶液中KIO3+5KI+3H2SO4=3I2+3H2O+3K2SO4。
(1)用双线桥表示该反应中电子转移的方向和数目__ ,该反应中还原产物与氧化产物的物质的量比是__ 。
(2)0.5 mol KIO3参加反应时转移电子__ mol。
(3)上面实验中用到一定物质的量浓度的稀硫酸,若配制1 mol/L的稀硫酸溶液480 mL,需用18 mol/L浓H2SO4__ mL。
(4)下面操作造成所配稀硫酸溶液浓度偏高的是__ 。
A.溶解后溶液没有冷却到室温就转移
B.转移时没有洗涤烧杯、玻璃棒
C.向容量瓶加水定容时眼睛俯视液面
D.用量筒量取浓硫酸后洗涤量筒并把洗涤液转移到容量瓶
E.摇匀后发现液面低于刻度线,又加蒸馏水至刻度线
(1)用双线桥表示该反应中电子转移的方向和数目
(2)0.5 mol KIO3参加反应时转移电子
(3)上面实验中用到一定物质的量浓度的稀硫酸,若配制1 mol/L的稀硫酸溶液480 mL,需用18 mol/L浓H2SO4
(4)下面操作造成所配稀硫酸溶液浓度偏高的是
A.溶解后溶液没有冷却到室温就转移
B.转移时没有洗涤烧杯、玻璃棒
C.向容量瓶加水定容时眼睛俯视液面
D.用量筒量取浓硫酸后洗涤量筒并把洗涤液转移到容量瓶
E.摇匀后发现液面低于刻度线,又加蒸馏水至刻度线
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】菜之魂在味,在“七味八滋”中,盐应是百味之首。粗盐中除了含有泥沙之外,还含有少量 、
、 、
、 等杂质离子,某同学设计如图实验方案提纯粗盐,同时验证可溶性杂质是否存在,请根据图示回答下列问题。
等杂质离子,某同学设计如图实验方案提纯粗盐,同时验证可溶性杂质是否存在,请根据图示回答下列问题。

(1)操作Ⅰ中用到玻璃棒,其作用是_____ 。
(2)操作Ⅲ中用到的玻璃仪器有玻璃棒、烧杯、_____ (填仪器名称);沉淀b的主要成分是碳酸钙、碳酸钡、_____ 。
(3)操作Ⅳ中加入盐酸的目的是_____ ,操作Ⅳ要得到精盐的操作是_____ 。
(4)操作Ⅱ至Ⅲ中加入除杂试剂的顺序还可以是_____ 。
(5)用NaCl固体配制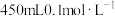 的NaCl溶液,实验中造成所配溶液浓度偏低的原因可能是_____。
的NaCl溶液,实验中造成所配溶液浓度偏低的原因可能是_____。
 、
、 、
、 等杂质离子,某同学设计如图实验方案提纯粗盐,同时验证可溶性杂质是否存在,请根据图示回答下列问题。
等杂质离子,某同学设计如图实验方案提纯粗盐,同时验证可溶性杂质是否存在,请根据图示回答下列问题。
(1)操作Ⅰ中用到玻璃棒,其作用是
(2)操作Ⅲ中用到的玻璃仪器有玻璃棒、烧杯、
(3)操作Ⅳ中加入盐酸的目的是
(4)操作Ⅱ至Ⅲ中加入除杂试剂的顺序还可以是
(5)用NaCl固体配制
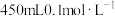 的NaCl溶液,实验中造成所配溶液浓度偏低的原因可能是_____。
的NaCl溶液,实验中造成所配溶液浓度偏低的原因可能是_____。| A.容量瓶中原来含有少量蒸馏水 |
| B.定容摇匀后少量溶液外流 |
| C.向容量瓶中加水定容时眼睛一直仰视刻度线 |
| D.称量NaCl固体时,砝码放在托盘天平左盘 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】用质量分数为36.5%的浓盐酸(密度为1.16 g·cm-3)配制成1 mol·L-1的稀盐酸。现实验室仅需要这种盐酸220 mL,试回答下列问题:
(1)配制稀盐酸时,应选用容量为___ mL的容量瓶。
(2)经计算需要___ mL浓盐酸,在量取时宜选用下列量筒中的___ (填字母)。
A.5 mL量筒 B.10 mL量筒
C.25 mL量筒 D.50 mL量筒
(3)在量取浓盐酸后,进行了下列操作:
①等稀释的盐酸的温度与室温一致后,沿玻璃棒注入选定规格的容量瓶中。
②往容量瓶中小心加蒸馏水至液面离容量瓶刻度线1~2 cm时,改用胶头滴管加蒸馏水,使溶液的液面与瓶颈的刻度线相切。
③在盛盐酸的烧杯中注入蒸馏水,并用玻璃棒搅动,使其混合均匀。
④用蒸馏水洗涤烧杯和玻璃棒2~3次,并将洗涤液全部注入容量瓶。
上述操作中,正确的顺序是___________ (填序号)。
(4)在上述配制过程中,用刚刚洗涤洁净的量筒来量取浓盐酸,则配制的稀盐酸浓度___________ (填“偏高”“偏低”或“无影响”)。若未用蒸馏水洗涤烧杯内壁或未将洗涤液注入容量瓶,则配制的稀盐酸浓度___________ (填“偏高”“偏低”或“无影响”)。
(1)配制稀盐酸时,应选用容量为
(2)经计算需要
A.5 mL量筒 B.10 mL量筒
C.25 mL量筒 D.50 mL量筒
(3)在量取浓盐酸后,进行了下列操作:
①等稀释的盐酸的温度与室温一致后,沿玻璃棒注入选定规格的容量瓶中。
②往容量瓶中小心加蒸馏水至液面离容量瓶刻度线1~2 cm时,改用胶头滴管加蒸馏水,使溶液的液面与瓶颈的刻度线相切。
③在盛盐酸的烧杯中注入蒸馏水,并用玻璃棒搅动,使其混合均匀。
④用蒸馏水洗涤烧杯和玻璃棒2~3次,并将洗涤液全部注入容量瓶。
上述操作中,正确的顺序是
(4)在上述配制过程中,用刚刚洗涤洁净的量筒来量取浓盐酸,则配制的稀盐酸浓度
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】(1)如何运用最简方法检验NaCl溶液中有无 离子?
离子?_________ 。
(2)在同温同压下,相等质量的氧气和臭氧,它们的物质的量之比为________ ,分子个数比为________ ,原子个数比为________ 。
(3)在一密闭容器中充入a mol NO和b mol O2,可发生如下反应:2NO+O2===2NO2,充分反应后容器中氮原子和氧原子的个数之比为________ 。
 离子?
离子?(2)在同温同压下,相等质量的氧气和臭氧,它们的物质的量之比为
(3)在一密闭容器中充入a mol NO和b mol O2,可发生如下反应:2NO+O2===2NO2,充分反应后容器中氮原子和氧原子的个数之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】某无色透明溶液中可能含有下列离子中的一种或几种:Na+、Mg2+、Cu2+、OH-、Cl-、 、
、 、
、 。现进行如下实验:
。现进行如下实验:
①滴加紫色石蕊溶液检验,溶液变蓝色。
②另取少量溶液逐滴滴加盐酸至过量,无气体放出,再加入BaCl2溶液后,有白色沉淀生成。
③另取少量溶液用硝酸酸化后,加入AgNO3溶液有白色沉淀生成。
(1)根据上述实验推断:原溶液中肯定有___ 离子,肯定没有___ 离子,不能肯定存在___ 离子。
(2)写出相关反应的离子方程式____
 、
、 、
、 。现进行如下实验:
。现进行如下实验:①滴加紫色石蕊溶液检验,溶液变蓝色。
②另取少量溶液逐滴滴加盐酸至过量,无气体放出,再加入BaCl2溶液后,有白色沉淀生成。
③另取少量溶液用硝酸酸化后,加入AgNO3溶液有白色沉淀生成。
(1)根据上述实验推断:原溶液中肯定有
(2)写出相关反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】氮及其化合物的相互转化对生命、生产生活意义重大。  是重要的化工原料,可发生如下转化:
是重要的化工原料,可发生如下转化:
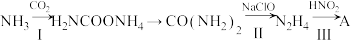
已知: 可被弱氧化剂氧化。
可被弱氧化剂氧化。
(1)氨气和光气 反应也可生成
反应也可生成  和一种盐,请写出该盐的化学式:
和一种盐,请写出该盐的化学式:_________ 。
(2)下列说法正确的是 。
(3)请预测物质的稳定性:
_________________  (填“
(填“ ”或“
”或“ ”),理由是
”),理由是_____________________ 。
(4)反应Ⅲ消耗 与
与  的物质的量相等,产物
的物质的量相等,产物  不含氧元素,请写出该反应的化学方程式
不含氧元素,请写出该反应的化学方程式_________________ 。
(5)反应Ⅱ在碱性条件下按方程式计量数之比投料,且恰好完全反应。请设计实验检验还原产物中的阴离子_________________ 。
 是重要的化工原料,可发生如下转化:
是重要的化工原料,可发生如下转化: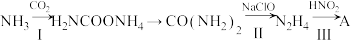
已知:
 可被弱氧化剂氧化。
可被弱氧化剂氧化。(1)氨气和光气
 反应也可生成
反应也可生成  和一种盐,请写出该盐的化学式:
和一种盐,请写出该盐的化学式:(2)下列说法正确的是 。
| A.实验室可用加热氯化铵固体来制取氨气 |
B. 在水、醇中的溶解度较大 在水、醇中的溶解度较大 |
C.硝酸工业排放的  可用 可用  处理生成无污染的物质 处理生成无污染的物质 |
D.为反应完全,反应Ⅱ所加  应过量 应过量 |

 (填“
(填“ ”或“
”或“ ”),理由是
”),理由是(4)反应Ⅲ消耗
 与
与  的物质的量相等,产物
的物质的量相等,产物  不含氧元素,请写出该反应的化学方程式
不含氧元素,请写出该反应的化学方程式(5)反应Ⅱ在碱性条件下按方程式计量数之比投料,且恰好完全反应。请设计实验检验还原产物中的阴离子
您最近一年使用:0次



