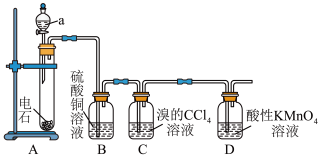
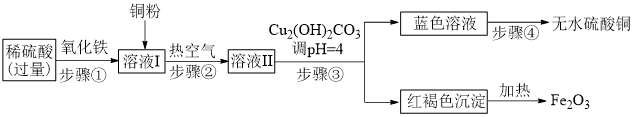
工业上以稀硫酸、氧化铁、铜粉为原料制备硫酸铜的流程如下:
已知:①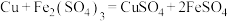 ;
;
②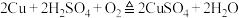 ;
;
③Fe2+易被氧化成Fe3+。
(1)步骤①发生的化学方程式是_______ 。
(2)溶液Ⅱ中溶质的成分是_______ (填化学式)。
(3)步骤③的名称是_______ ,用到的玻璃仪器有烧杯、_______ 、玻璃棒。
(4)上述流程中可以循环使用的物质是_______ (填名称)。

已知:①
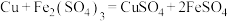 ;
;②
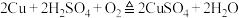 ;
;③Fe2+易被氧化成Fe3+。
(1)步骤①发生的化学方程式是
(2)溶液Ⅱ中溶质的成分是
(3)步骤③的名称是
(4)上述流程中可以循环使用的物质是
更新时间:2021-10-12 09:51:51
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】盐泥是氯碱工业的废渣,主要成分为Mg(OH)2、CaCO3(含少量的FeO、Fe2O3、Al2O3及SiO2)。为充分利用资源,变废为宝,在实验室中采用盐泥来制备无水MgSO4,流程如下:
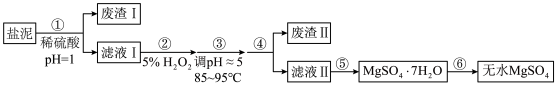
已知:硫酸钙微溶于水,溶解度随温度的升高而降低。
回答下列问题:
(1)从下图中选择合适的仪器,按上述流程制备无水MgSO4.仪器首次使用的先后顺序为___________ (填标号)。

(2)步骤①中产生的废渣Ⅰ的主要成分为___________ (填化学式)。
(3)步骤③需要加热的目的是___________ ,温度保持85~95℃,采用的合适加热方式是___________ 。
(4)步骤⑤的具体实验操作有___________ 。

已知:硫酸钙微溶于水,溶解度随温度的升高而降低。
回答下列问题:
(1)从下图中选择合适的仪器,按上述流程制备无水MgSO4.仪器首次使用的先后顺序为

(2)步骤①中产生的废渣Ⅰ的主要成分为
(3)步骤③需要加热的目的是
(4)步骤⑤的具体实验操作有
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】明朝宋应星所著的《天工开物》中记载了世界上最早的炼锌技术:“罐中炉甘石熔化成团,冷定毁罐取出。每十耗去其二,即倭铅也。”这里炉甘石即菱锌矿(含85%ZnCO3,其余为SiO2、Fe3O4、CuO、CaO和MgO杂质)。硒化锌是一种半导体材料,以菱锌矿为原料制备硒化锌的流程如下:

已知部分信息如下:
①常温下,几种离子形成氢氧化物的pH如表所示。
②锌的性质和铝、铜相似,如Zn(OH)2是两性氢氧化物,Zn(OH)2溶于氨水形成 。
。
回答下列问题:
(1)为增大“酸浸”速率,可采取的措施是_______ (填一条即可),“酸浸”中溶解Fe3O4的离子方程式为_______ 。
(2)“滤渣1”的主要成分为_______ (填化学式)。
(3)常温下,“调pH”的范围为_______ 。
(4)“反萃取”中稀硫酸的主要作用是_______ 。
(5)“电解”中以石墨为电极,阳极的电极反应式为_______ ,废液可以循环用于_______ (填名称)工序。
(6)合成ZnSe宜在氩气氛围中进行,氩气的作用是_______ 。
(7)某工厂用10t该菱锌矿来生产ZnSe,若最终制得8.64tZnSe,则Zn的损耗率为_______ 。(设“还原”时消耗的Zn为65kg,保留三位有效数字)

已知部分信息如下:
①常温下,几种离子形成氢氧化物的pH如表所示。
| 金属离子 |  |  |  |  |  |
| 开始沉淀的pH | 1.9 | 7.0 | 6.0 | 6.2 | 8.8 |
| 完全沉淀的pH | 3.2 | 9.0 | 8.0 | 8.2 | 10.9 |
 。
。回答下列问题:
(1)为增大“酸浸”速率,可采取的措施是
(2)“滤渣1”的主要成分为
(3)常温下,“调pH”的范围为
(4)“反萃取”中稀硫酸的主要作用是
(5)“电解”中以石墨为电极,阳极的电极反应式为
(6)合成ZnSe宜在氩气氛围中进行,氩气的作用是
(7)某工厂用10t该菱锌矿来生产ZnSe,若最终制得8.64tZnSe,则Zn的损耗率为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】计算机记忆材料生产中产生大量的钌废料,一种从钌废料[含Ru(OH)3、FeO、MnO、SiO2及少量的Au]中合成六氯钌酸铵[(NH4)2RuCl6]的流程如下:

回答下列问题
(1)(NH4)2RuCl6中Ru的化合价为___________ 。
(2)滤渣1的成分是________ 。
(3)加入CrO3发生反应的离子方程式为______________ 。
(4)已知几种金属离子的氢氧化物开始沉淀和完全沉淀的pH如下表,调pH时,应调整的pH范围为_________ 。
(5)加入NaClO后,Mn以MnO2的形式沉淀而除去,该反应中氧化剂与还原剂的物质的量之比为________ 。
(6)氨化时发生反应的化学方程式为____________
(7)氨化时,投料比 对(NH4)2RuCl6产率的影响如图所示:
对(NH4)2RuCl6产率的影响如图所示:
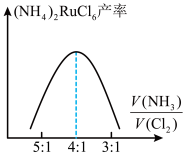
(NH4)2RuCl6的产率在 为4:1后降低,其原因可能是
为4:1后降低,其原因可能是_______________ 。
(8)已知钌废料中钌含量为53%,氨化时产率为91%,其余步骤损失率合计为11%,则2吨钌废料可制得(NH4)2RuCl6________ kg。

回答下列问题
(1)(NH4)2RuCl6中Ru的化合价为
(2)滤渣1的成分是
(3)加入CrO3发生反应的离子方程式为
(4)已知几种金属离子的氢氧化物开始沉淀和完全沉淀的pH如下表,调pH时,应调整的pH范围为
| 金属离子 | 开始沉淀的pH | 完全沉淀的pH |
| Fe3+ | 1.8 | 3.2 |
| Cr3+ | 4.6 | 5.9 |
| Fe2+ | 5.8 | 11.2 |
| Mn2+ | 8.8 | 10.9 |
| Ru3+ | 7.9 | 11.3 |
(5)加入NaClO后,Mn以MnO2的形式沉淀而除去,该反应中氧化剂与还原剂的物质的量之比为
(6)氨化时发生反应的化学方程式为
(7)氨化时,投料比
 对(NH4)2RuCl6产率的影响如图所示:
对(NH4)2RuCl6产率的影响如图所示:
(NH4)2RuCl6的产率在
 为4:1后降低,其原因可能是
为4:1后降低,其原因可能是(8)已知钌废料中钌含量为53%,氨化时产率为91%,其余步骤损失率合计为11%,则2吨钌废料可制得(NH4)2RuCl6
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】硫酸铁铵是分析化学中常用试剂,其晶体化学式为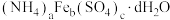 。实验室模拟用废铁屑[成分为铁和少量铁锈(用
。实验室模拟用废铁屑[成分为铁和少量铁锈(用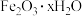 表示)]制取硫酸铁铵晶体,具体流程如下图所示:
表示)]制取硫酸铁铵晶体,具体流程如下图所示:

(1)步骤①中,铁锈与硫酸反应的离子方程式为_______ 。该步骤采用水浴加热,而不用明火加热,原因是_______ 。
(2)步骤②中加入足量 的目的是
的目的是_______ 。
(3)硫酸铁铵晶体组成的测定。
步骤1:准确称取质量为4.820g固体在酸性条件下溶于水配成100.00mL溶液A;
步骤2:取25.00mL溶液A,加入足量的 溶液,过滤得1.165g沉淀;
溶液,过滤得1.165g沉淀;
步骤3:取25.00mL溶液A,加入足量氢氧化钠溶液,过滤、洗涤并灼烧得到0.2g固体;
通过计算确定该晶体的化学式(写出计算过程)。_________
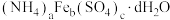 。实验室模拟用废铁屑[成分为铁和少量铁锈(用
。实验室模拟用废铁屑[成分为铁和少量铁锈(用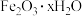 表示)]制取硫酸铁铵晶体,具体流程如下图所示:
表示)]制取硫酸铁铵晶体,具体流程如下图所示:
(1)步骤①中,铁锈与硫酸反应的离子方程式为
(2)步骤②中加入足量
 的目的是
的目的是(3)硫酸铁铵晶体组成的测定。
步骤1:准确称取质量为4.820g固体在酸性条件下溶于水配成100.00mL溶液A;
步骤2:取25.00mL溶液A,加入足量的
 溶液,过滤得1.165g沉淀;
溶液,过滤得1.165g沉淀;步骤3:取25.00mL溶液A,加入足量氢氧化钠溶液,过滤、洗涤并灼烧得到0.2g固体;
通过计算确定该晶体的化学式(写出计算过程)。
您最近一年使用:0次
【推荐2】某工厂酸性废液中含有Fe3+、Al3+、Fe2+、SO ,以该废液为原料制备Fe2O3的工艺流程如下(部分操作和条件略):
,以该废液为原料制备Fe2O3的工艺流程如下(部分操作和条件略):

回答下列问题:
(1)写出“还原”步骤中反应的离子方程式:Fe+2H+=Fe2++H2↑和_______ 。
(2)试剂X可选用_______ (写一种,填化学式),“滤渣”的主要成分是_______ 、_______ 。
(3)加入碳酸氢铵后,生成FeCO3沉淀,过滤,发现滤液有些浑浊,可能的操作失误的原因是_______ 。
(4)若在实验室中灼烧FeCO3应在_______ (填仪器名称)中进行,“灼烧氧化”在空气中进行,写出该反应的化学方程式_______ 。
 ,以该废液为原料制备Fe2O3的工艺流程如下(部分操作和条件略):
,以该废液为原料制备Fe2O3的工艺流程如下(部分操作和条件略):
回答下列问题:
(1)写出“还原”步骤中反应的离子方程式:Fe+2H+=Fe2++H2↑和
(2)试剂X可选用
(3)加入碳酸氢铵后,生成FeCO3沉淀,过滤,发现滤液有些浑浊,可能的操作失误的原因是
(4)若在实验室中灼烧FeCO3应在
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】铁是人体必需的微量元素,治疗缺铁性贫血的常见方法是服用补铁药物。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。某同学为了检测“速力菲”药片中Fe2+的存在,设计并进行了如下实验:

试回答下列问题:
(1)试剂1是__ ,试剂2是__ ,加入新制氯水后溶液中发生的离子反应方程式是__ 、_____ 。
(2)加入试剂2后溶液中颜色由淡黄色转变为淡红色是因为__ ,写出+2价Fe在空气中转化为+3价Fe的化学方程式__ 。
(3)该同学猜想红色溶液变为无色溶液的原因是溶液中的+3价铁被还原为+2价铁,你认为该同学的猜想合理吗?__ 。若你认为合理,请说明理由(若你认为不合理,该空不作答);若你认为不合理请提出你的猜想并设计一个简单的实验加以验证(若你认为合理,该空不作答)___ 。

试回答下列问题:
(1)试剂1是
(2)加入试剂2后溶液中颜色由淡黄色转变为淡红色是因为
(3)该同学猜想红色溶液变为无色溶液的原因是溶液中的+3价铁被还原为+2价铁,你认为该同学的猜想合理吗?
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如下:
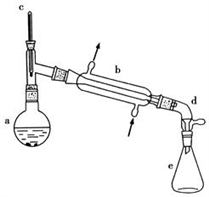

可能用到的有关数据如下:
(1)合成反应:在a中加入20g环己醇和2小片碎瓷片,冷却搅动下慢慢加入1mL浓硫酸,b中通入冷却水后,开始缓慢加热a,控制馏出物的温度不超过90℃。
(2)分离提纯:
反应粗产物倒入分液漏斗中,分别用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙,最终通过蒸馏得到纯净环己烯10g。
回答下列问题:
(1)装置b的名称____________
(2)如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是_________ (填正确答案标号)
A.立刻补加 B.冷却后补加 C.不需补加 D.重新配料
(3)本实验中最容易产生的副产物的结构简式为_______________________
(4)在本实验的分离过程中,产物应从分液漏斗的_________________ (填“上口倒出”或“下口倒出”)
(5)分离提纯过程中加入无水氯化钙的目的是________________________
(6)在蒸馏收集产品时, 控制的温度应在____________ 左右,实验制得的环己烯精品质量低于理论产量,可能的原因是______________ (填序号)
a.蒸馏时从70℃开始收集产品
b.环己醇实际用量多了
c.制备粗品时环己醇随产品一起蒸出


可能用到的有关数据如下:
| 相对分子质量 | 密度/(g·cm-3) | 沸点/℃ | 溶解性 | |
| 环己醇 | 100 | 0.9618 | 161 | 微溶于水 |
| 环己烯 | 82 | 0.8102 | 83 | 难溶于水 |
(2)分离提纯:
反应粗产物倒入分液漏斗中,分别用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙,最终通过蒸馏得到纯净环己烯10g。
回答下列问题:
(1)装置b的名称
(2)如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是
A.立刻补加 B.冷却后补加 C.不需补加 D.重新配料
(3)本实验中最容易产生的副产物的结构简式为
(4)在本实验的分离过程中,产物应从分液漏斗的
(5)分离提纯过程中加入无水氯化钙的目的是
(6)在蒸馏收集产品时, 控制的温度应在
a.蒸馏时从70℃开始收集产品
b.环己醇实际用量多了
c.制备粗品时环己醇随产品一起蒸出
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】掌握仪器的名称、组装及使用方法是中学化学实验的基础,下图为两套实验装置。

(1)写出下列仪器的名称:
①___________ ;②__________ ;④___________ ;
(2)若利用装置Ⅰ分离四氯化碳和酒精的混合物,还缺少的仪器有__________ ,将仪器补充完整后进行的实验操作的名称为;_________ 。冷凝管中的水流从______ 进______ 出(填字母代号)。
(3)现需配制250 mL 0.2 mol/L NaCl溶液,装置Ⅱ是某同学转移溶液的示意图,图中的错误是__________________________________ 。

(1)写出下列仪器的名称:
①
(2)若利用装置Ⅰ分离四氯化碳和酒精的混合物,还缺少的仪器有
(3)现需配制250 mL 0.2 mol/L NaCl溶液,装置Ⅱ是某同学转移溶液的示意图,图中的错误是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某工业废水中存在大量的  和
和 ,欲除去废水中的 Cu2+和
,欲除去废水中的 Cu2+和 ,设计工艺流程如图所示:
,设计工艺流程如图所示:

(1)操作1中不需要的仪器是___________ 。
a.烧杯 b.托盘天平 c.漏斗 d.玻璃棒 e.量筒
(2) 溶液和
溶液和 溶液分别是
溶液分别是___________ ,___________ (填溶质化学式)。
(3)溶液A→混合物 B过程中可观察到有白色沉淀___________ 生成(填化学式)。
(4)混合物B→溶液 C过程中所涉及的离子方程式是___________ 。
(5)加入适量盐酸的作用是___________ 。
 和
和 ,欲除去废水中的 Cu2+和
,欲除去废水中的 Cu2+和 ,设计工艺流程如图所示:
,设计工艺流程如图所示:
(1)操作1中不需要的仪器是
a.烧杯 b.托盘天平 c.漏斗 d.玻璃棒 e.量筒
(2)
 溶液和
溶液和 溶液分别是
溶液分别是(3)溶液A→混合物 B过程中可观察到有白色沉淀
(4)混合物B→溶液 C过程中所涉及的离子方程式是
(5)加入适量盐酸的作用是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】青蒿素是最好的抵抗疟疾的药物,可从黄花蒿茎叶中提取,它是无色针状晶体,可溶于乙醇、乙醚等有机溶剂,难溶于水。常见的提取方法如下

(1)操作I、II中,不会 用到的装置是________ (填序号)。
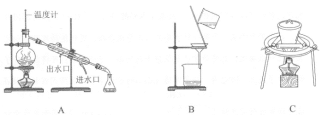
(2)向干燥、破碎后的黄花蒿中加入乙醚的作用是________ 。
(3)操作III的目的是_________ 。
(4)如图是几种实验中常用的仪器:
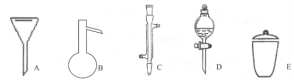
写出序号所代表的仪器的名称:
A.__________ ;B.__________ ;C.__________ ;D.__________ ;E.__________

(1)操作I、II中,

(2)向干燥、破碎后的黄花蒿中加入乙醚的作用是
(3)操作III的目的是
(4)如图是几种实验中常用的仪器:

写出序号所代表的仪器的名称:
A.
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】用如图方法回收废旧CPU中的单质Au(金),Ag和Cu。

已知:①浓硝酸不能单独将Au溶解。②HAuCl4=H++AuCl 。
。
(1)酸溶后经__ 操作,将混合物分离。
(2)浓、稀HNO3均可作酸溶试剂。溶解等量的Cu消耗HNO3的物质的量不同,写出消耗HNO3物质的量少的反应的化学方程式:__ 。
(3)HNO3—NaCl与王水[V(浓硝酸):V(浓盐酸)=1:3]溶金原理相同,还原产物遇空气变红棕色。
①将溶金反应的化学方程式补充完整:__ 。
Au+______NaCl+______HNO3=HAuCl4+______+______+______NaNO3
②关于溶金的下列说法正确的是__ 。
A.用到了HNO3的氧化性
B.王水中浓盐酸的主要作用是增强溶液的酸性
C.用浓盐酸与NaNO3也可使Au溶解
(4)用适当浓度的盐酸、NaCl溶液、氨水与铁粉,可按照如图方法从酸溶后的溶液中回收Cu和Ag(图中标注的试剂和物质均不同)。

试剂1是__ ,试剂2是__ 。

已知:①浓硝酸不能单独将Au溶解。②HAuCl4=H++AuCl
 。
。(1)酸溶后经
(2)浓、稀HNO3均可作酸溶试剂。溶解等量的Cu消耗HNO3的物质的量不同,写出消耗HNO3物质的量少的反应的化学方程式:
(3)HNO3—NaCl与王水[V(浓硝酸):V(浓盐酸)=1:3]溶金原理相同,还原产物遇空气变红棕色。
①将溶金反应的化学方程式补充完整:
Au+______NaCl+______HNO3=HAuCl4+______+______+______NaNO3
②关于溶金的下列说法正确的是
A.用到了HNO3的氧化性
B.王水中浓盐酸的主要作用是增强溶液的酸性
C.用浓盐酸与NaNO3也可使Au溶解
(4)用适当浓度的盐酸、NaCl溶液、氨水与铁粉,可按照如图方法从酸溶后的溶液中回收Cu和Ag(图中标注的试剂和物质均不同)。

试剂1是
您最近一年使用:0次