二氧化氯(ClO2)是一种广谱杀菌消毒剂。某工厂以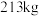
 固体、若干NaCl固体和876 kg一定溶质质量分数的稀硫酸为原料制取ClO2。反应的方程式如下:
固体、若干NaCl固体和876 kg一定溶质质量分数的稀硫酸为原料制取ClO2。反应的方程式如下: ,假设反应物均恰好完全反应。试计算:[已知:相对分子质量为
,假设反应物均恰好完全反应。试计算:[已知:相对分子质量为 106.5
106.5  142
142  98]
98]
(1)ClO2中氯、氧元素质量比为_______ (填最简整数比)。
(2)反应后所得溶液中Na2SO4的质量分数是_______ 。
(3)30℃时,将所得的硫酸钠溶液蒸发多少千克水可以恰好形成该温度下的饱和溶液_______ 。(已知:30℃时,Na2SO4的溶解度为40 g。)
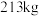
 固体、若干NaCl固体和876 kg一定溶质质量分数的稀硫酸为原料制取ClO2。反应的方程式如下:
固体、若干NaCl固体和876 kg一定溶质质量分数的稀硫酸为原料制取ClO2。反应的方程式如下: ,假设反应物均恰好完全反应。试计算:[已知:相对分子质量为
,假设反应物均恰好完全反应。试计算:[已知:相对分子质量为 106.5
106.5  142
142  98]
98](1)ClO2中氯、氧元素质量比为
(2)反应后所得溶液中Na2SO4的质量分数是
(3)30℃时,将所得的硫酸钠溶液蒸发多少千克水可以恰好形成该温度下的饱和溶液
更新时间:2021-10-25 09:48:02
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】(1)分别取wg钠、铁、铝与足量的稀盐酸反应,在相同条件下产生氢气的体积之比是__________ 。
(2)分别取0.1 mol钠、铁、铝与足量的稀盐酸反应,在相同条件下产生氢气的体积之比是___________ 。
(3)若产生相同物质的量的氢气,所需钠、铁、铝的质量之比是_________ 。
(4)若产生相同体积(同温同压下)的氢气,所需钠、铁、铝的物质的量之比是__________ 。
(2)分别取0.1 mol钠、铁、铝与足量的稀盐酸反应,在相同条件下产生氢气的体积之比是
(3)若产生相同物质的量的氢气,所需钠、铁、铝的质量之比是
(4)若产生相同体积(同温同压下)的氢气,所需钠、铁、铝的物质的量之比是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】常温下将Cl2缓慢通入水中至饱和,然后改向其中滴加浓NaOH溶液至恰好完全反应。上述整个实验过程中溶液的pH变化曲线如图所示(不考虑次氯酸的分解以及溶液体积的变化)。
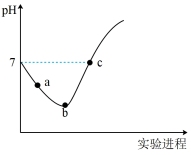
①请对图中pH的整个变化趋势作出解释(用离子方程式表示)________ 。
②写出b点对应溶液中的电荷守恒式___________ 。并且比较c(HClO) :a点___________ b点;c(Cl–):b点___________ c点(填>、<或=)
③Cl2O为淡棕黄色气体,是次氯酸的酸酐,可由新制的HgO和Cl2反应来制备,该反应为歧化反应(氧化剂和还原剂为同一种物质的反应)。上述制备Cl2O的化学方程式为___________ 。
④ClO2常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。一种有效成分为NaClO2、NaHSO4、NaHCO3的“二氧化氯泡腾片”,能快速溶于水,溢出大量气泡,得到ClO2溶液。上述过程中,生成ClO2的反应属于歧化反应,每生成1mol ClO2消耗NaClO2的量为______ mol; 产生“气泡”的化学方程式为____ 。
⑤“84消毒液“的有效成分为NaClO,不可与酸性清洁剂混用的原因是___________ (用离子方程式表示)。工业上是将氯气通入到30%的NaOH溶液中来制备NaClO溶液,若NaClO溶液中NaOH的质量分数为1%,则生产1000kg该溶液需消耗氯气的质量为 ___________ kg(保留整数)。

①请对图中pH的整个变化趋势作出解释(用离子方程式表示)
②写出b点对应溶液中的电荷守恒式
③Cl2O为淡棕黄色气体,是次氯酸的酸酐,可由新制的HgO和Cl2反应来制备,该反应为歧化反应(氧化剂和还原剂为同一种物质的反应)。上述制备Cl2O的化学方程式为
④ClO2常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。一种有效成分为NaClO2、NaHSO4、NaHCO3的“二氧化氯泡腾片”,能快速溶于水,溢出大量气泡,得到ClO2溶液。上述过程中,生成ClO2的反应属于歧化反应,每生成1mol ClO2消耗NaClO2的量为
⑤“84消毒液“的有效成分为NaClO,不可与酸性清洁剂混用的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
真题
【推荐1】黄铁矿主要成分是FeS2.某硫酸厂在进行黄铁矿成分测定时,取0.1000 g样品在空气中充分灼烧,将生成的SO2气体与足量‘Fe2(SO4)3溶液完全反应后,用浓度为0.02000 mol/L的K2Cr2O7标准溶液滴定至终点,消耗K2Cr2O7溶液25.00 mL 。
已知:SO2+2Fe3++2H2O= +2Fe2++4H+
+2Fe2++4H+
Cr2O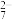 +6Fe2++14H+=2Cr3++6Fe3++7H2O
+6Fe2++14H+=2Cr3++6Fe3++7H2O
(1)样品中FeS2的质量分数是(假设杂质不参加反应)_______ 。
(2)若灼烧6 g FeS2产生的SO2全部转化为SO3气体时放出9.83 kJ热量,产生的SO3与水全部化合生成H2SO4,放出13.03 kJ热量,写出SO3气体转化为H2SO4的热化学方程式:_______ 。
(3)煅烧10 t上述黄铁矿,理论上产生SO2的体积(标准状况)为_______ L,制得98%的硫酸质量为_______ t ,SO2全部转化为H2SO4时放出的热量是_______ kJ。
已知:SO2+2Fe3++2H2O=
 +2Fe2++4H+
+2Fe2++4H+Cr2O
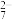 +6Fe2++14H+=2Cr3++6Fe3++7H2O
+6Fe2++14H+=2Cr3++6Fe3++7H2O(1)样品中FeS2的质量分数是(假设杂质不参加反应)
(2)若灼烧6 g FeS2产生的SO2全部转化为SO3气体时放出9.83 kJ热量,产生的SO3与水全部化合生成H2SO4,放出13.03 kJ热量,写出SO3气体转化为H2SO4的热化学方程式:
(3)煅烧10 t上述黄铁矿,理论上产生SO2的体积(标准状况)为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】元素分析是有机化合物的表征手段之一,按下图实验装置(部分装置略)对有机化合物进行C、H元素分析。
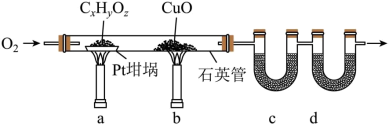
回答下列问题:
(1)将装有样品的Pt坩埚和CuO放入石英管中,先通入一定的O2,而后将已称重的U型管c、d与石英管连接,检查装置气密性。依次点燃煤气灯___________ (排a、b顺序),进行实验。
(2)O2的作用有为实验提供氧化剂、提供气流保证反应产物完全进入到U型管中。CuO的作用是___________ (举1例,用化学方程式表示)。
(3)c和d中的试剂分别是___________ 、___________ (填标号)。c和d中的试剂不可调换,理由是___________ 。
A.CaCl2 B.NaCl C.碱石灰(CaO+NaOH) D.Na2SO3
(4)Pt坩埚中样品CxHyOz反应完全后,应进行操作:___________ 。取下c和d管称重。
(5)若样品CxHyOz为0.0236g,实验结束后,c管增重0.0108g,d管增重0.0352g。质谱测得该有机物的相对分子量为118,其分子式为___________ 。

回答下列问题:
(1)将装有样品的Pt坩埚和CuO放入石英管中,先通入一定的O2,而后将已称重的U型管c、d与石英管连接,检查装置气密性。依次点燃煤气灯
(2)O2的作用有为实验提供氧化剂、提供气流保证反应产物完全进入到U型管中。CuO的作用是
(3)c和d中的试剂分别是
A.CaCl2 B.NaCl C.碱石灰(CaO+NaOH) D.Na2SO3
(4)Pt坩埚中样品CxHyOz反应完全后,应进行操作:
(5)若样品CxHyOz为0.0236g,实验结束后,c管增重0.0108g,d管增重0.0352g。质谱测得该有机物的相对分子量为118,其分子式为
您最近一年使用:0次
【推荐3】某厂平均每天产生约600m3废氨水(NH3的浓度为153mg·L-1,密度为1g·cm-3。)
(1)该废氨水中氨的物质的量浓度为_________ 。
(2)对废氨水进行加热蒸发得到NH3,使废氨水中的NH3的浓度降为17 mg·L-1。忽略蒸发前后废氨水体积变化,则上述体积的废氨水蒸发出来的NH3的物质的量为_________ 。(以下计算结果均保留两位小数)
(3)蒸发得到的NH3可用于制备NO。4NH3+5O2 →4NO+6H2O;(不考虑NO与氧气的反应),设空气中氧气的体积分数为0.20,氮气体积分数为0.80。
①为使NH3恰好完全氧化为NO,氨—空气混合物中氨的体积分数为________ 。
②氨催化氧化制取NO同时会发生副反应:4NH3+3O2→2N2+6H2O。将1L NH3混合10L空气后通入反应器,反应完成后,测得混合气体中不含NH3,而O2和N2的物质的量之比为1∶10,试求参加主反应的氨占原料氨的体积百分含量_______ 。
(4)废氨水可用于脱除烟气中的SO2。氨水吸收烟气中SO2经氧化后生成(NH4)2SO4和NH4HSO4混合物。现称取不同质量的混合物进行实验,结果如下:
试计算生成氨气的质量最大时样品的质量________ 。
(1)该废氨水中氨的物质的量浓度为
(2)对废氨水进行加热蒸发得到NH3,使废氨水中的NH3的浓度降为17 mg·L-1。忽略蒸发前后废氨水体积变化,则上述体积的废氨水蒸发出来的NH3的物质的量为
(3)蒸发得到的NH3可用于制备NO。4NH3+5O2 →4NO+6H2O;(不考虑NO与氧气的反应),设空气中氧气的体积分数为0.20,氮气体积分数为0.80。
①为使NH3恰好完全氧化为NO,氨—空气混合物中氨的体积分数为
②氨催化氧化制取NO同时会发生副反应:4NH3+3O2→2N2+6H2O。将1L NH3混合10L空气后通入反应器,反应完成后,测得混合气体中不含NH3,而O2和N2的物质的量之比为1∶10,试求参加主反应的氨占原料氨的体积百分含量
(4)废氨水可用于脱除烟气中的SO2。氨水吸收烟气中SO2经氧化后生成(NH4)2SO4和NH4HSO4混合物。现称取不同质量的混合物进行实验,结果如下:
| NaOH溶液体积/mL | 40.00 | 40.00 | 40.00 |
| 样品质量/g | 7.75 | 15.50 | 23.25 |
| 氨气质量/g | 1.87 | 1.87 | 1.7 |
试计算生成氨气的质量最大时样品的质量
您最近一年使用:0次

 的反应中,已知
的反应中,已知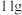 物质A完全反应生成
物质A完全反应生成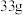 物质C和
物质C和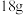 物质D.若B的相对分子质量为32,试计算物质A的相对分子质量
物质D.若B的相对分子质量为32,试计算物质A的相对分子质量

