根据题目要求填空。
(1)下列变化过程,属于放热反应的是__________ (填序号)。
①酸碱中和反应; ②H2在Cl2中燃烧; ③Ba(OH)2•8H2O与NH4Cl;
④铝热反应; ⑤碳高温条件下还原CO2 。
(2)0.5molCH4完全燃烧生成CO2和液态水时,放出445kJ的热量。写出CH4燃烧的热化学方程式_______ 。
(3)通常人们把拆开1mol某化学键吸收的能量看成该化学键的键能。表中是一些化学键的键能。
根据键能数据估算下列反应:则CH4(g)+4F2(g)=CF4(g)+4HF(g) △H=___ kJ·mol-1。
(4)氢能的存储是氢能利用的前提,科学家研究出一种储氢合金Mg2Ni;
已知:
①Mg(s)+H2(g)=MgH2(s) △H1
②Mg2Ni(s)+2MgH2(s)=2Mg(s)+Mg2NiH4(s) △H2
求 Mg2Ni(s)+2H2(g)=Mg2NiH4(s) △H=____________ 。
(1)下列变化过程,属于放热反应的是
①酸碱中和反应; ②H2在Cl2中燃烧; ③Ba(OH)2•8H2O与NH4Cl;
④铝热反应; ⑤碳高温条件下还原CO2 。
(2)0.5molCH4完全燃烧生成CO2和液态水时,放出445kJ的热量。写出CH4燃烧的热化学方程式
(3)通常人们把拆开1mol某化学键吸收的能量看成该化学键的键能。表中是一些化学键的键能。
化学键 | C—H | C—F | H—F | F—F |
键能kJ/mol | 414 | 489 | 565 | 155 |
根据键能数据估算下列反应:则CH4(g)+4F2(g)=CF4(g)+4HF(g) △H=
(4)氢能的存储是氢能利用的前提,科学家研究出一种储氢合金Mg2Ni;
已知:
①Mg(s)+H2(g)=MgH2(s) △H1
②Mg2Ni(s)+2MgH2(s)=2Mg(s)+Mg2NiH4(s) △H2
求 Mg2Ni(s)+2H2(g)=Mg2NiH4(s) △H=
更新时间:2021-10-27 18:52:11
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】获取能量变化的途径
(1)通过化学键的键能计算。已知:
则

_______  。
。
(2)通过物质所含能量计算。已知反应 中A、B、C、D所具有的能量依次可表示为
中A、B、C、D所具有的能量依次可表示为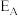 、
、 、
、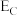 、
、 ,该反应
,该反应
_______ (用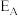 、
、 、
、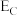 、
、 表示)。
表示)。
(3)通过盖斯定律计算。已知在25℃、101KPa时:
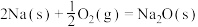



写出 与
与 反应生成
反应生成 的热化学方程式
的热化学方程式_______ 。
(1)通过化学键的键能计算。已知:
| 化学键 |  |  |  |
键能 | 436 | 496 | 463.4 |


 。
。(2)通过物质所含能量计算。已知反应
 中A、B、C、D所具有的能量依次可表示为
中A、B、C、D所具有的能量依次可表示为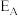 、
、 、
、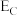 、
、 ,该反应
,该反应
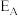 、
、 、
、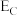 、
、 表示)。
表示)。(3)通过盖斯定律计算。已知在25℃、101KPa时:
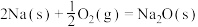



写出
 与
与 反应生成
反应生成 的热化学方程式
的热化学方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】I.下表是几种常用燃料(1mol)完全燃烧时放出的热量:
(1)从热量角度分析,目前最适合家庭使用的优质气体燃料是___________ 。
(2)写出管道煤气中的一氧化碳燃烧的热化学方程式___________ 。
(3)充分燃烧 1mol 表中各种燃料,排放出二氧化碳的量最多的是___________ 。
(4)矿物燃料储量有限,而且在燃烧过程中会产生污染。根据能源多样化的发展战略,我国开发利用的绿色能源有氢能、___________ 等。
II.在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能 发生化学反应,这些分子称为活化分子,使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用 kJ·mol-1表示。请认真观察下图,然后回答问题:
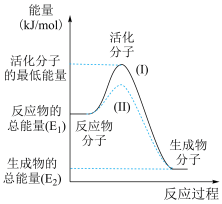
(5)图中所示反应是___________ (填“吸热”或“放热”)反应,该反应的ΔH=___________ (用含 E1、E2 的代数式表示)。
(6)下列 4 个反应中符合示意图描述的反应的是___________(填代号)。
| 物质 | 炭粉(C) | 一氧化碳(CO) | 氢气(H2) | 甲烷(CH4) | 乙醇(C2H5OH) |
| 状态 | 固体 | 气体 | 气体 | 气体 | 液体 |
| 热量(kJ) | 392.8 | 282.6 | 285.8 | 890.3 | 1367 |
(2)写出管道煤气中的一氧化碳燃烧的热化学方程式
(3)充分燃烧 1mol 表中各种燃料,排放出二氧化碳的量最多的是
(4)矿物燃料储量有限,而且在燃烧过程中会产生污染。根据能源多样化的发展战略,我国开发利用的绿色能源有氢能、
II.在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能 发生化学反应,这些分子称为活化分子,使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用 kJ·mol-1表示。请认真观察下图,然后回答问题:

(5)图中所示反应是
(6)下列 4 个反应中符合示意图描述的反应的是___________(填代号)。
| A.水蒸气与炭反应 | B.用水稀释氢氧化钠溶液 | C.铝粉与四氧化三铁反应 | D.灼热的炭与 CO2反应 |
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】在日常生活和工农业生产中经常涉及到吸热反应和放热反应,回答下面问题:
(1)下列反应一定属于吸热反应的是___________ 。
A. 酸碱中和反应 B. 燃烧反应
C. 铝热反应 D. C(s)+CO2(g) 2CO(g)
2CO(g)
(2)在101kPa时,H2在1.0molO2中完全燃烧,生成2.0mol液态水,放出571.6k的热量,表示氢气燃烧的热化学方程式为___________ ,氢气的燃烧热为___________ kJ•mol-1。
(3)我国科学家利用计算机模拟了甲醇(CH3OH)与水在铜基催化剂上的反应机理和能量图如图:

①反应I的△H___________ 0(填“<”“>”或“=”),反应Ⅱ的活化能是___________ kJ•mol-1。
②在相同条件下反应I的反应速率___________ (填“<”“>”或“=”)反应Ⅱ的反应速率。
③写出反应Ⅱ的热化学方程式___________ 。
(4)取30mL0.5mol•L-1H2SO4溶液与50mL0.5mol•L-1NaOH溶液于小烧杯中,用如图所示:装置进行中和反应反应热的测定实验。

①仪器a的名称是___________ 。
②若实验中测得中和热数值总是偏小,可能的原因是___________ (答出一条即可)。
(1)下列反应一定属于吸热反应的是
A. 酸碱中和反应 B. 燃烧反应
C. 铝热反应 D. C(s)+CO2(g)
 2CO(g)
2CO(g) (2)在101kPa时,H2在1.0molO2中完全燃烧,生成2.0mol液态水,放出571.6k的热量,表示氢气燃烧的热化学方程式为
(3)我国科学家利用计算机模拟了甲醇(CH3OH)与水在铜基催化剂上的反应机理和能量图如图:

①反应I的△H
②在相同条件下反应I的反应速率
③写出反应Ⅱ的热化学方程式
(4)取30mL0.5mol•L-1H2SO4溶液与50mL0.5mol•L-1NaOH溶液于小烧杯中,用如图所示:装置进行中和反应反应热的测定实验。

①仪器a的名称是
②若实验中测得中和热数值总是偏小,可能的原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】(1)写出下列反应的热化学方程式:8g甲烷在空气中燃烧,恢复常温,测得放出热量445kJ。_____________________________________________________ 。
(2)实验测得1mol H2与1mol Cl2完全反应放出184.6kJ的热量,又知1mol H2分子中化学键断裂时需要吸收436kJ的能量,1mol Cl2分子中化学键断裂需要吸收243kJ的能量。则1mol HCl分子中化学键断裂时需要吸收___________________ 的能量。
(3)CO2可转化为甲醇:CO2(g)+3H2(g) CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
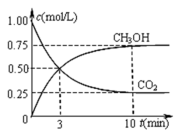
①在一恒温恒容密闭容器中充入1mol CO2和3mol H2进行上述反应。测得CO2和CH3OH(g)浓度随时间变化如图所示。回答:0~10min内,氢气的平均反应速率为________________ 。
②若反应在容积可变的容器中进行。缩小容器体积使压强增大,该反应的速率_________ (填“增大”、“减小”或“不变”)。
(2)实验测得1mol H2与1mol Cl2完全反应放出184.6kJ的热量,又知1mol H2分子中化学键断裂时需要吸收436kJ的能量,1mol Cl2分子中化学键断裂需要吸收243kJ的能量。则1mol HCl分子中化学键断裂时需要吸收
(3)CO2可转化为甲醇:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
①在一恒温恒容密闭容器中充入1mol CO2和3mol H2进行上述反应。测得CO2和CH3OH(g)浓度随时间变化如图所示。回答:0~10min内,氢气的平均反应速率为
②若反应在容积可变的容器中进行。缩小容器体积使压强增大,该反应的速率
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】氮的氧化物是造成大气污染的主要物质。研究氮氧化物的反应机理对于消除环境污染有重要意义。NO在空气中存在如下反应:2NO(g)+O2(g) 2NO2(g) △H,上述反应分两步完成,其反应历程如图所示:
2NO2(g) △H,上述反应分两步完成,其反应历程如图所示:

回答下列问题:
(1)写出反应I的热化学方程式___ 。
(2)反应I和反应Ⅱ中,一个是快反应,会快速建立平衡状态,而另一个是慢反应。决定2NO(g)+O2(g) 2NO2(g)反应速率的是
2NO2(g)反应速率的是___ (填“反应I”或“反应Ⅱ”);对该反应体系升高温度,发现总反应速率反而变慢,其原因可能是___ (反应未使用催化剂)。
 2NO2(g) △H,上述反应分两步完成,其反应历程如图所示:
2NO2(g) △H,上述反应分两步完成,其反应历程如图所示:
回答下列问题:
(1)写出反应I的热化学方程式
(2)反应I和反应Ⅱ中,一个是快反应,会快速建立平衡状态,而另一个是慢反应。决定2NO(g)+O2(g)
 2NO2(g)反应速率的是
2NO2(g)反应速率的是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】下列反应中,属于放热反应的是__________ ,属于吸热反应的是___________
①食物在空气中腐败 ②生石灰与水作用制熟石灰 ③碳和二氧化碳化合生成CO ④酸与碱中和反应 ⑤加热KClO3和MnO2的混合物制O2⑥将氯化铵晶体和氢氧化钡晶体混合均匀放在日光下暴晒
①食物在空气中腐败 ②生石灰与水作用制熟石灰 ③碳和二氧化碳化合生成CO ④酸与碱中和反应 ⑤加热KClO3和MnO2的混合物制O2⑥将氯化铵晶体和氢氧化钡晶体混合均匀放在日光下暴晒
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】在化学反应

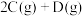
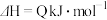 过程中的能量变化如图所示,回答下列问题。
过程中的能量变化如图所示,回答下列问题。

(1)Q________ 0(填“>”“<”或“=”)。
(2)熵变
________ 0(填“>”“<”或“=”)。
(3)该反应________ 自发进行(填“能”或“不能”)。
(4)升高温度平衡常数K________ (填“增大”“减小”或“不变”),平衡向________ (填“正反应”或“逆反应”)方向移动。


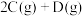
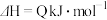 过程中的能量变化如图所示,回答下列问题。
过程中的能量变化如图所示,回答下列问题。
(1)Q
(2)熵变

(3)该反应
(4)升高温度平衡常数K
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】某温度时,在2L的密闭容器中,X、Y、Z(均为气体)的物质的量随时间的变化曲线如图所示。请回答下列问题:
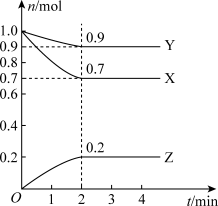
(1)由图中所给数据进行分析,该反应的化学方程式为___________ 。
(2)反应从开始至2min,用Z的浓度变化表示的平均反应速率υ(Z)=___________ 。
(3)下列措施能加快反应速率的是___ (填序号,下同)。
A.恒压时充入He B.恒容时充入He
C.恒容时充入X D.及时分离出Z
E.升高温度 F.选择高效的催化剂
(4)下列选项发生放热反应的是___ (填序号)。
①干冰的气化
②浓硫酸和水混合
③Ba(OH)2·8H2O和NH4Cl的反应
④盐酸和氢氧化钠混合
(5)H2(g)+ I2(g) 2HI(g)已经达到平衡状态的标志是
2HI(g)已经达到平衡状态的标志是___________ (填序号)。
①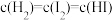
②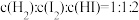
③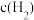 、
、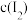 、
、 不再随时间而改变
不再随时间而改变
④单位时间内生成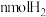 的同时生成2nmolHI
的同时生成2nmolHI
⑤单位时间内生成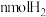 的同时生成1nmolI2
的同时生成1nmolI2
⑥反应速率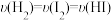
⑦一个H−H键断裂的同时有两个H−I键断裂
⑧温度和体积一定时,容器内压强不再变化
⑨温度和体积一定时,混合气体的颜色不再变化

(1)由图中所给数据进行分析,该反应的化学方程式为
(2)反应从开始至2min,用Z的浓度变化表示的平均反应速率υ(Z)=
(3)下列措施能加快反应速率的是
A.恒压时充入He B.恒容时充入He
C.恒容时充入X D.及时分离出Z
E.升高温度 F.选择高效的催化剂
(4)下列选项发生放热反应的是
①干冰的气化
②浓硫酸和水混合
③Ba(OH)2·8H2O和NH4Cl的反应
④盐酸和氢氧化钠混合
(5)H2(g)+ I2(g)
 2HI(g)已经达到平衡状态的标志是
2HI(g)已经达到平衡状态的标志是①
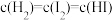
②
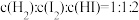
③
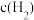 、
、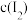 、
、 不再随时间而改变
不再随时间而改变 ④单位时间内生成
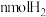 的同时生成2nmolHI
的同时生成2nmolHI⑤单位时间内生成
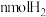 的同时生成1nmolI2
的同时生成1nmolI2⑥反应速率
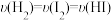
⑦一个H−H键断裂的同时有两个H−I键断裂
⑧温度和体积一定时,容器内压强不再变化
⑨温度和体积一定时,混合气体的颜色不再变化
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】已知:
C(石墨,s)+O2(g)=CO2(g) ΔH1=-akJ∙mol-1
2H2(g)+O2(g)=2H2O(l) ΔH2=-bkJ∙mol-1
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) ΔH3=-ckJ∙mol-1
根据盖斯定律,计算298K时由C(石墨,s)和H2(g)生成1molC2H2(g)反应的焓变ΔH=______________________ (用含有a,b,c的式子表示)
C(石墨,s)+O2(g)=CO2(g) ΔH1=-akJ∙mol-1
2H2(g)+O2(g)=2H2O(l) ΔH2=-bkJ∙mol-1
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) ΔH3=-ckJ∙mol-1
根据盖斯定律,计算298K时由C(石墨,s)和H2(g)生成1molC2H2(g)反应的焓变ΔH=
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】自热化学链重整制氢CLR(a)工艺的原理如图所示:
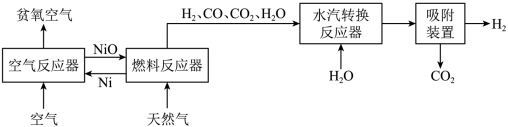
回答下列问题:
(1)25℃、101 kPa时,1.0 g Ni与足量O2反应生成NiO放出8.0 kJ的热量,则在“空气反应器”中发生反应的热化学方程式为_______________ 。
(2)“燃料反应器”中发生的部分反应有:
(I)CO(g)+NiO(s)=CO2(g)+Ni(s) △H1=-47.0 kJ∙mol−1
(II)CH4(g)+4NiO(s)=CO2(g)+2H2O(g)+4Ni(s) △H2=+137.7 kJ∙mol−1
(III)CH4(g)+H2O(g)=CO(g)+3H2(g) △H3=+225.5 kJ∙mol−1
则反应CH4(g)+NiO(s)=CO(g)+2H2(g)+Ni(s)的△H=______ kJ∙mol−1。
(3)“水汽转换反应器”中发生的反应为CO(g)+H2O(g) H2(g)+CO2(g)(平衡常数K=0.75),将天然气看作是纯净的CH4(假定向水汽转换反应器中补充的水的物质的量等于甲烷的物质的量),若在t℃时进行转换,水汽转换反应器中某时刻CO、H2O、H2、CO2浓度之比为1:x:2:1,此时υ(正)
H2(g)+CO2(g)(平衡常数K=0.75),将天然气看作是纯净的CH4(假定向水汽转换反应器中补充的水的物质的量等于甲烷的物质的量),若在t℃时进行转换,水汽转换反应器中某时刻CO、H2O、H2、CO2浓度之比为1:x:2:1,此时υ(正) ______ υ(逆)(填“>”“=”或“<”),理由是__________ 。
(4)甲烷制氢传统工艺有水蒸气重整、部分氧化重整以及联合重整等,CLR(a)工艺重整是一种联合重整,涉及反应的热化学方程式如下:
水蒸气重整反应:CH4(g)+2H2O(g)=CO2(g)+4H2(g) △H=+192 kJ∙mol−1
部分氧化重整反应:CH4(g)+O2(g)=CO2(g)+2H2(g) △H=-748 kJ∙mol−1
采用水蒸气重整的优点是__________ ;若上述两个反应在保持自热条件下(假设无热量损失),理论上1 mol CH4至多可获得H2的物质的量为____________ (结果保留1位小数)。

回答下列问题:
(1)25℃、101 kPa时,1.0 g Ni与足量O2反应生成NiO放出8.0 kJ的热量,则在“空气反应器”中发生反应的热化学方程式为
(2)“燃料反应器”中发生的部分反应有:
(I)CO(g)+NiO(s)=CO2(g)+Ni(s) △H1=-47.0 kJ∙mol−1
(II)CH4(g)+4NiO(s)=CO2(g)+2H2O(g)+4Ni(s) △H2=+137.7 kJ∙mol−1
(III)CH4(g)+H2O(g)=CO(g)+3H2(g) △H3=+225.5 kJ∙mol−1
则反应CH4(g)+NiO(s)=CO(g)+2H2(g)+Ni(s)的△H=
(3)“水汽转换反应器”中发生的反应为CO(g)+H2O(g)
 H2(g)+CO2(g)(平衡常数K=0.75),将天然气看作是纯净的CH4(假定向水汽转换反应器中补充的水的物质的量等于甲烷的物质的量),若在t℃时进行转换,水汽转换反应器中某时刻CO、H2O、H2、CO2浓度之比为1:x:2:1,此时υ(正)
H2(g)+CO2(g)(平衡常数K=0.75),将天然气看作是纯净的CH4(假定向水汽转换反应器中补充的水的物质的量等于甲烷的物质的量),若在t℃时进行转换,水汽转换反应器中某时刻CO、H2O、H2、CO2浓度之比为1:x:2:1,此时υ(正) (4)甲烷制氢传统工艺有水蒸气重整、部分氧化重整以及联合重整等,CLR(a)工艺重整是一种联合重整,涉及反应的热化学方程式如下:
水蒸气重整反应:CH4(g)+2H2O(g)=CO2(g)+4H2(g) △H=+192 kJ∙mol−1
部分氧化重整反应:CH4(g)+O2(g)=CO2(g)+2H2(g) △H=-748 kJ∙mol−1
采用水蒸气重整的优点是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】2013年12月2日,“嫦娥三号”探测器由长征三号乙运载火箭从西昌卫星发射中心发射,首次实现月球软着陆和月面巡视勘察。“长征”系列火箭用偏二甲肼(C2H8N2)作燃料,四氧化二氮作氧化剂,生成氮气和二氧化碳气体。
(1)写出反应的化学方程式:_____________________________________________ 。
(2)该反应是________ (填“放热”或“吸热”)反应,反应物的总能量________ (填“大于”“小于”或“等于”)生成物的总能量,断开化学键________ 的总能量小于形成化学键________ 的总能量(填“吸收”或“放出”)。
(3)如果一个反应可以分几步进行,则各分步反应的反应热之和与该反应一步完成时的反应热是相同的,这个规律称为盖斯定律。据此回答下列问题。
已知:Na2CO3·10H2O(s)===Na2CO3(s)+10H2O(g)ΔH1=+532.36kJ·mol-1
Na2CO3·10H2O(s)===Na2CO3·H2O(s)+9H2O(g) ΔH2=+473.63kJ·mol-1
写出Na2CO3·H2O脱水反应的热化学方程式____________________ 。
(1)写出反应的化学方程式:
(2)该反应是
(3)如果一个反应可以分几步进行,则各分步反应的反应热之和与该反应一步完成时的反应热是相同的,这个规律称为盖斯定律。据此回答下列问题。
已知:Na2CO3·10H2O(s)===Na2CO3(s)+10H2O(g)ΔH1=+532.36kJ·mol-1
Na2CO3·10H2O(s)===Na2CO3·H2O(s)+9H2O(g) ΔH2=+473.63kJ·mol-1
写出Na2CO3·H2O脱水反应的热化学方程式
您最近一年使用:0次



