在化学反应

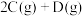
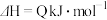 过程中的能量变化如图所示,回答下列问题。
过程中的能量变化如图所示,回答下列问题。

(1)Q________ 0(填“>”“<”或“=”)。
(2)熵变
________ 0(填“>”“<”或“=”)。
(3)该反应________ 自发进行(填“能”或“不能”)。
(4)升高温度平衡常数K________ (填“增大”“减小”或“不变”),平衡向________ (填“正反应”或“逆反应”)方向移动。


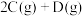
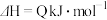 过程中的能量变化如图所示,回答下列问题。
过程中的能量变化如图所示,回答下列问题。
(1)Q
(2)熵变

(3)该反应
(4)升高温度平衡常数K
17-18高二上·湖北荆州·期中 查看更多[10]
内蒙古科尔沁左翼中旗实验高级中学2022-2023学年高二下学期期末考试化学试题第三节 化学反应的方向海南省三亚华侨学校(南新校区)2021-2022学年高二上学期期中考试化学试题黑龙江省牡丹江市海林市朝鲜族中学2021-2022学年上学期高二10月月考化学试题甘肃省庆阳市镇原县第二中学2020-2021学年高二上学期期末考试化学试题(已下线)第02章 化学反应速率与化学平衡(A卷基础强化篇)-2020-2021学年高二化学选择性必修1同步单元AB卷(新教材人教版)步步为赢 高二化学寒假作业:作业三 化学反应的方向与平衡常数的应用【全国百强校】内蒙古自治区杭锦后旗奋斗中学2018-2019学年高二上学期期末考试化学试题(已下线)2018年10月25日 《每日一题》人教选修4--化学反应方向的判断湖北省监利县实验高中2017-2018学年高二上学期期中考试化学试题
更新时间:2019-12-14 14:25:45
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】在一个小烧杯里加入 20 g Ba(OH)2·8H2O晶体,将小烧杯放在事先已滴有3~4滴水的玻璃片上。然后加入10 g NH4Cl晶体,并用玻璃棒迅速搅拌。
(1)实验中观察到的现象有_______ 、_______ 和反应混合物呈糊状。反应呈糊状的原因是_______ 。
(2)通过_______ 现象,说明该反应为_______ (填“吸”或“放”)热反应,这是由于反应物的总能量_______ (填“高”或“低”)于生成物的总能量。
(3)写出这个反应的化学方程式_______
(1)实验中观察到的现象有
(2)通过
(3)写出这个反应的化学方程式
您最近一年使用:0次
【推荐2】化学反应都伴随着能量的变化。回答下列问题:
(1)可用焓变和熵变来判断化学反应进行的方向,下列都是能自发进行的化学反应,其中是吸热反应且反应后熵增的是___________(填字母)。
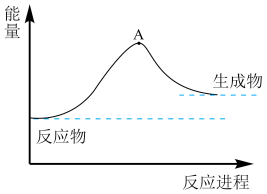
(2)一种分解海水制氢气的方法为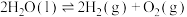 。如图为该反应的能量变化示意图,使用催化剂
。如图为该反应的能量变化示意图,使用催化剂 后,图中A点将
后,图中A点将_______ (填“升高”、“降低”或“不变”)。
(3)已知: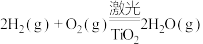
 ,部分化学键的键能数据如表:
,部分化学键的键能数据如表:
由此计算x=___________ 。(用含a、c、d的代数式表示)
(1)可用焓变和熵变来判断化学反应进行的方向,下列都是能自发进行的化学反应,其中是吸热反应且反应后熵增的是___________(填字母)。
A. | B. |
C. | D.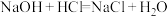 |
(2)一种分解海水制氢气的方法为
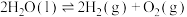 。如图为该反应的能量变化示意图,使用催化剂
。如图为该反应的能量变化示意图,使用催化剂 后,图中A点将
后,图中A点将
(3)已知:
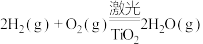
 ,部分化学键的键能数据如表:
,部分化学键的键能数据如表:| 化学键 |  |  |  |
 | x | c | d |
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】化学反应伴随着能量变化是化学反应的基本特征之一。
(1)有反应H2 + I2 = 2HI。已知拆开1 mol H—H键、1 mol I—I键、1 mol H—I键分别需要吸收的能量为436 kJ、151 kJ、299 kJ。由1 mol H2和1 mol I2反应生成2 molHI会___ (填“放出”或 “吸收”) ___ kJ的热量。
(2)下列反应中属于放热反应的是_______ (填序号,下同),属于吸热反应的是_______ 。
①物质燃烧 ②炸药爆炸 ③酸碱中和反应 ④二氧化碳通过炽热的炭 ⑤食物因氧化而腐败 ⑥Ba(OH)2·8H2O与NH4Cl反应 ⑦铁粉与稀盐酸反应
(1)有反应H2 + I2 = 2HI。已知拆开1 mol H—H键、1 mol I—I键、1 mol H—I键分别需要吸收的能量为436 kJ、151 kJ、299 kJ。由1 mol H2和1 mol I2反应生成2 molHI会
(2)下列反应中属于放热反应的是
①物质燃烧 ②炸药爆炸 ③酸碱中和反应 ④二氧化碳通过炽热的炭 ⑤食物因氧化而腐败 ⑥Ba(OH)2·8H2O与NH4Cl反应 ⑦铁粉与稀盐酸反应
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】目前工业上有一种方法是用CO2来生产燃料甲醇。
CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH=-49.0kJ/mol,为探究反应原理,现进行如下实验:
CH3OH(g)+H2O(g) ΔH=-49.0kJ/mol,为探究反应原理,现进行如下实验:
在体积为1 L的密闭容器中,充入1mol CO2和4 mol H2,一定条件下发生反应:测得CO2和CH3OH(g)的浓度随时间变化如图所示。
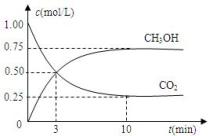
(1)从反应开始到平衡,氢气的平均反应速率v(H2)=_____________ mol/(L·min)。
(2)该反应的平衡常数表达式为_________________ 。
(3)下列措施中能使n(CH3OH)/n(CO2)增大的是__________ 。
A.升高温度 B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离 D.再充入1 mol CO2和4 mol H2
(4)如果在相同的容器中事先充入1 mol CH3OH和1 mol H2O,为了使反应达到的化学平衡和上述一样,则起始还需加入H2的物质的量为_____________ 。
CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH=-49.0kJ/mol,为探究反应原理,现进行如下实验:
CH3OH(g)+H2O(g) ΔH=-49.0kJ/mol,为探究反应原理,现进行如下实验:在体积为1 L的密闭容器中,充入1mol CO2和4 mol H2,一定条件下发生反应:测得CO2和CH3OH(g)的浓度随时间变化如图所示。

(1)从反应开始到平衡,氢气的平均反应速率v(H2)=
(2)该反应的平衡常数表达式为
(3)下列措施中能使n(CH3OH)/n(CO2)增大的是
A.升高温度 B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离 D.再充入1 mol CO2和4 mol H2
(4)如果在相同的容器中事先充入1 mol CH3OH和1 mol H2O,为了使反应达到的化学平衡和上述一样,则起始还需加入H2的物质的量为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】CH3OH(g)+H2O(g) CO2(g)+3H2(g);该反应的正反应为吸热反应,请根据题目要求回答下列问题:
CO2(g)+3H2(g);该反应的正反应为吸热反应,请根据题目要求回答下列问题:
(1)在其它条件不变的情况下降低温度,则逆反应速率______ (填“增大”或“减小”或“不变”,下同);在其它条件不变的情况下加压,则正反应速率__________ 。
(2)一定条件下,向体积为2L的密闭容器中充入1molCH3OH(g)和3molH2O(g),20s 后,测得混合气体的压强是反应前的1.2倍,则用甲醇表示该反应的速率为__________ 。
(3)判断该可逆反应达到平衡状态的依据是(填序号)_____ 。
A. v正(CH3OH)=v正(CO2)
C. 混合气体的平均相对分子质量不变
(4)在一定条件下,当该反应处于化学平衡状态时,下列操作可使化学平衡向逆反应方 向移动的是_______________ (填序号)。
A.升高温度 B.降低温度 C.增大压强
 CO2(g)+3H2(g);该反应的正反应为吸热反应,请根据题目要求回答下列问题:
CO2(g)+3H2(g);该反应的正反应为吸热反应,请根据题目要求回答下列问题:(1)在其它条件不变的情况下降低温度,则逆反应速率
(2)一定条件下,向体积为2L的密闭容器中充入1molCH3OH(g)和3molH2O(g),20s 后,测得混合气体的压强是反应前的1.2倍,则用甲醇表示该反应的速率为
(3)判断该可逆反应达到平衡状态的依据是(填序号)
A. v正(CH3OH)=v正(CO2)
B. 混合气体的密度不变
C. 混合气体的平均相对分子质量不变
D .CH3OH、H2O、CO2、H2的浓度都不再发生变化
(4)在一定条件下,当该反应处于化学平衡状态时,下列操作可使化学平衡向逆反应方 向移动的是
A.升高温度 B.降低温度 C.增大压强
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】(1)合成氨的工业生产中,进行氨合成反应的装置名称是_______ ,该装置中设置热交换器的目的是_______ ,在生产工艺中,采用了原料气循环使用的方法,其目的是_______ 。
(2)在一定体积的密闭容器中,有如下化学反应:CO2(g) + H2(g)⇌CO(g) + H2O(g)其化学平衡常数K 和温度的关系如表:
(3)该反应的化学平衡常数表达式为 K=_______ 。
(4)该反应为_______ 反应(填“吸热”“放热”)。
(5)向上述平衡体系中加入 CO2,达新平衡后 H2 的转化率_______ (选填:“增大”“不变”“减小”)。
(6)反应达平衡后,向容器中通入与平衡混合气组成、比例相同的气体,达到新平衡时与原平衡相比,有关说法正确的是_______ 。
A.反应物转化率增大 B.逆反应速率增大
C.各物质的比例不变 D.c(CO2)增大、c(CO)减小
(7)某温度下,平衡浓度符合:3[c(CO2)·c(H2)]=5[c(CO)·c(H2O)],此温度为_______ ℃。
(2)在一定体积的密闭容器中,有如下化学反应:CO2(g) + H2(g)⇌CO(g) + H2O(g)其化学平衡常数K 和温度的关系如表:
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(3)该反应的化学平衡常数表达式为 K=
(4)该反应为
(5)向上述平衡体系中加入 CO2,达新平衡后 H2 的转化率
(6)反应达平衡后,向容器中通入与平衡混合气组成、比例相同的气体,达到新平衡时与原平衡相比,有关说法正确的是
A.反应物转化率增大 B.逆反应速率增大
C.各物质的比例不变 D.c(CO2)增大、c(CO)减小
(7)某温度下,平衡浓度符合:3[c(CO2)·c(H2)]=5[c(CO)·c(H2O)],此温度为
您最近一年使用:0次
【推荐1】氧化铁可以与一氧化碳发生反应:Fe2O3(s)+3CO(g) 2Fe(s)+3CO2(g)
2Fe(s)+3CO2(g)
①该反应的平衡常数表达式K=_______ ,△H_______ 0(填“>”、“<”或“=”)
②在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0mol,反应经过10min后达到平衡,则该时间范围内反应的平均反应速率υ(CO2)=_______ ,CO的平衡转化率为_______
③欲提高②中CO的平衡转化率,可采取的措施是_______
A.减少Fe的量
B.增加Fe2O3的量
C.移出部分CO2
D.提高反应温度
E.减小容器的容积
F.加入合适的催化剂
 2Fe(s)+3CO2(g)
2Fe(s)+3CO2(g)| 温度/℃ | 1000 | 1150 | 1300 |
| 平衡常数 | 64.0 | 50.7 | 42.9 |
②在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0mol,反应经过10min后达到平衡,则该时间范围内反应的平均反应速率υ(CO2)=
③欲提高②中CO的平衡转化率,可采取的措施是
A.减少Fe的量
B.增加Fe2O3的量
C.移出部分CO2
D.提高反应温度
E.减小容器的容积
F.加入合适的催化剂
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】 可用FeO吸收获得
可用FeO吸收获得 .有关反应:
.有关反应:
①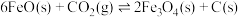
②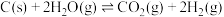
(1)反应①的化学平衡常数表达式为________ 。
(2)若 时反应①达到平衡,此时
时反应①达到平衡,此时 的浓度为
的浓度为 ,保持其他条件不变,再加入一定量的
,保持其他条件不变,再加入一定量的 ,再次达到平衡后
,再次达到平衡后 的浓度为
的浓度为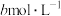 ,则a
,则a________ b(选填“>”、“<”或“=”)。请说明理由________ 。
 可用FeO吸收获得
可用FeO吸收获得 .有关反应:
.有关反应:①
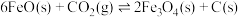
②
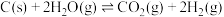
(1)反应①的化学平衡常数表达式为
(2)若
 时反应①达到平衡,此时
时反应①达到平衡,此时 的浓度为
的浓度为 ,保持其他条件不变,再加入一定量的
,保持其他条件不变,再加入一定量的 ,再次达到平衡后
,再次达到平衡后 的浓度为
的浓度为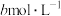 ,则a
,则a
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】在温度 和
和 下,
下, 和
和 反应生成
反应生成 的平衡常数如下表:
的平衡常数如下表:
(1)已知,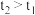 ,HX的生成反应是
,HX的生成反应是___________ 反应(填“吸热”或“放热”)。
(2)HX的电子式是___________ 。
(3)共价键的极性随共用电子对偏移程度的增大而增强,HX共价键的极性由强到弱的顺序是___________ 。
(4)X2都能与H2反应生成HX,用原子结构解释原因:___________ 。
(5)K的变化体现出X2化学性质的递变性,用原子结构解释原因:___________ ,原子半径逐渐增大,得电子能力逐渐减弱。
(6)仅依据K的变化,可以推断出:随着卤素原子核电荷数的增加,___________ (填字母序号)。
a.在相同条件下,平衡时X2的转化率逐渐降低
b.X2与H2反应的剧烈程度逐渐减弱
c.HX的还原性逐渐减弱
d.HX的稳定性逐渐减弱
(7)为验证VIIA族部分元素非金属性的递变规律,设计如图装置进行实验,请回答:
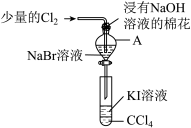
①棉花中浸有 溶液的作用是
溶液的作用是___________ (用离子方程式表示)。
②验证溴与碘的非金属性强弱:通入少量氯气,充分反应后,将A中液体滴入试管内,取下试管,充分振荡、静置,可观察到___________ ;该实验必须控制氯气的加入量,否则得不出溴的非金属性比碘强的结论,理由是___________ 。
 和
和 下,
下, 和
和 反应生成
反应生成 的平衡常数如下表:
的平衡常数如下表:| 化学方程式 | 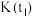 |  |
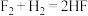 | 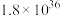 | 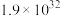 |
 | 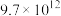 | 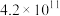 |
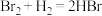 |  |  |
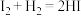 | 43 | 34 |
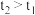 ,HX的生成反应是
,HX的生成反应是(2)HX的电子式是
(3)共价键的极性随共用电子对偏移程度的增大而增强,HX共价键的极性由强到弱的顺序是
(4)X2都能与H2反应生成HX,用原子结构解释原因:
(5)K的变化体现出X2化学性质的递变性,用原子结构解释原因:
(6)仅依据K的变化,可以推断出:随着卤素原子核电荷数的增加,
a.在相同条件下,平衡时X2的转化率逐渐降低
b.X2与H2反应的剧烈程度逐渐减弱
c.HX的还原性逐渐减弱
d.HX的稳定性逐渐减弱
(7)为验证VIIA族部分元素非金属性的递变规律,设计如图装置进行实验,请回答:

①棉花中浸有
 溶液的作用是
溶液的作用是②验证溴与碘的非金属性强弱:通入少量氯气,充分反应后,将A中液体滴入试管内,取下试管,充分振荡、静置,可观察到
您最近一年使用:0次



