目前,世界上多采用电解熔融氯化钠的方法来生产金属钠: 。已知A、B、C、D、E、F有如下转化关系:
。已知A、B、C、D、E、F有如下转化关系:
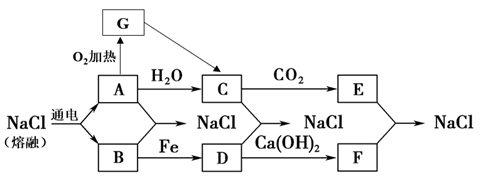
(1)写出化学式:A________ E_________ ,G________ 。
(2)写出A→C的化学方程式:________ 反应类型为:____ 。
写出B→D化学反应方程式:___________ 。
(3)G为_______ (颜色)固体,G→C的化学方程式__________________ 。
(4)若把A投入盛有D的溶液中,溶液中出现____________ 颜色沉淀。
 。已知A、B、C、D、E、F有如下转化关系:
。已知A、B、C、D、E、F有如下转化关系:
(1)写出化学式:A
(2)写出A→C的化学方程式:
写出B→D化学反应方程式:
(3)G为
(4)若把A投入盛有D的溶液中,溶液中出现
更新时间:2021-10-21 18:26:41
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】物质间的转化关系如图所示,其中圆圈“〇”内物质是化合物,方框“□”内的物质是单质,A为医学上治疗胃酸过多的一种药剂,G为淡黄色固体,C在通常状况下为无色液体。
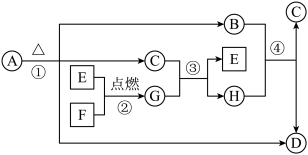
(1)C的化学式为_____ 。
(2)反应①②③④中_____ (填序号)属于氧化还原反应。
(3)检验H中阳离子的常用方法:_____ ,现象:_____ 。
(4)书写方程式:
①A与少量澄清石灰水反应的离子反应方程式:_____ 。
②由D转化为H的化学反应方程式:_____ 。
(5)若工业制得的D中混有少量A,用化学方程式表示提纯D的方法:_____ 。

(1)C的化学式为
(2)反应①②③④中
(3)检验H中阳离子的常用方法:
(4)书写方程式:
①A与少量澄清石灰水反应的离子反应方程式:
②由D转化为H的化学反应方程式:
(5)若工业制得的D中混有少量A,用化学方程式表示提纯D的方法:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】中学化学中有很多物质可以实现下图中物质之间的转化。其中反应条件和部分反应的产物已略去。液体B和C可能是单一溶质的溶液,也可能是纯净物。

(1)若A是一种红色金属,气体D能使品红溶液褪色,加热时又恢复原色。写出反应①的化学方程式_______________________________________________ 。
(2)若A是金属单质,D是一种无色气体,遇到空气变为红棕色,液体C呈浅绿色。
写出反应①的离子方程式________________________________________ ; 写出反应②的任意一个离子方程式____________________________________________ 。
(3)若A是一种金属单质,D是最轻的气体,B能否是NaOH溶液________ (填“能”或“否”),若能,写出相应的离子方程式 (若否,则不用填此空)__________________________ 。

(1)若A是一种红色金属,气体D能使品红溶液褪色,加热时又恢复原色。写出反应①的化学方程式
(2)若A是金属单质,D是一种无色气体,遇到空气变为红棕色,液体C呈浅绿色。
写出反应①的离子方程式
(3)若A是一种金属单质,D是最轻的气体,B能否是NaOH溶液
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】已知a、b、d、e、f、g、h为原子序数依次增大的七种短周期主族元素,非金属元素a最外层电子数与其周期数相同,b原子的最外层电子数是其所在周期数的2倍。d的一种单质可杀菌消毒,g的最高正价与最低负价代数和为4,f的最高价氧化物可分别与e和h的最高价氧化物的水化物反应,a单质在h单质中燃烧,产物溶于水得到一种强酸甲。请用化学用语回答下列问题:
(1)f在元素周期表中的位置_______ ,画出与h同族的第四周期元素的原子结构示意图_______ 。
(2)d、e、f、h的简单离子的半径由大到小的顺序_______ 。
(3)下列说法正确的是_______。
(4)为降低水源中 对人体的危害,可在强碱性条件下用f的单质将溶液中的
对人体的危害,可在强碱性条件下用f的单质将溶液中的 还原为
还原为 ,该反应的离子方程式为
,该反应的离子方程式为_______ 。
(5)将e和f单质各1mol投入足量水中,充分反应后,所得溶液体积为500mL,则该过程可得标况下气体体积_______ L。
(1)f在元素周期表中的位置
(2)d、e、f、h的简单离子的半径由大到小的顺序
(3)下列说法正确的是_______。
| A.简单氢化物的稳定性d>b |
| B.含氧酸的酸性h>g>b>f |
C.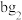 中b为 中b为 价;g为 价;g为 价可说明g的非金属性强于b 价可说明g的非金属性强于b |
D.g阴离子能与 反应而h的阴离子不能,可说明g的非金属性弱于h 反应而h的阴离子不能,可说明g的非金属性弱于h |
 对人体的危害,可在强碱性条件下用f的单质将溶液中的
对人体的危害,可在强碱性条件下用f的单质将溶液中的 还原为
还原为 ,该反应的离子方程式为
,该反应的离子方程式为(5)将e和f单质各1mol投入足量水中,充分反应后,所得溶液体积为500mL,则该过程可得标况下气体体积
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】下列图示中,A为一种常见的金属单质,B、C、D、E是含该元素的常见化合物,它们的焰色反应均为黄色。
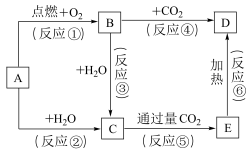
请填写下列空白:
(1)少量的A应保存在_______ 中;A着火时应采取的灭火措施是用_______ 盖灭。
A.煤油 B.水 C.二氧化碳 D.细沙 E.干粉灭火器
(2)以上反应中,属于氧化还原反应的有_______ 。(填写编号)
(3)反应②的离子方程式是_______ ,反应④的化学方程式是_____ ,反应⑥化学方程式是_________ 。

请填写下列空白:
(1)少量的A应保存在
A.煤油 B.水 C.二氧化碳 D.细沙 E.干粉灭火器
(2)以上反应中,属于氧化还原反应的有
(3)反应②的离子方程式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】A、B、C是由周期表中短周期元素组成的三种常见化合物,甲、乙、丙是三种单质,这些单质和化合物之间存在如图所示的关系,完成下列空白:
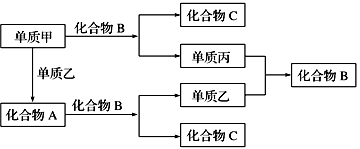
(1)向酚酞试液中加入化合物A的粉末,现象为________ 。
(2)单质甲与化合物B反应的离子方程式为__________ 。5.05g单质甲—钾合金溶于200mL水生成0.075mol氢气,确定该合金的化学式为______ 。
(3)向一定体积某浓度的化合物C的溶液中通入CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同。若向M中逐滴加入0.1mol/L盐酸,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系有下列图示两种情况。
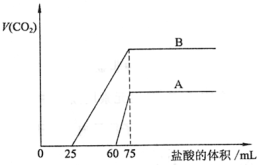
①由A确定滴加前60mL的盐酸时,发生反应的离子方程式为_____________________
②B对应的溶液M低温蒸干后得到固体a克,将a克固体充分加热至恒重后,固体质量减少_____ 克。
③由A、B可知,两次实验通入的CO2的体积比为___________

(1)向酚酞试液中加入化合物A的粉末,现象为
(2)单质甲与化合物B反应的离子方程式为
(3)向一定体积某浓度的化合物C的溶液中通入CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同。若向M中逐滴加入0.1mol/L盐酸,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系有下列图示两种情况。

①由A确定滴加前60mL的盐酸时,发生反应的离子方程式为
②B对应的溶液M低温蒸干后得到固体a克,将a克固体充分加热至恒重后,固体质量减少
③由A、B可知,两次实验通入的CO2的体积比为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】钠及它们的化合物在生产、生活中有着重要的用途。
(1)高压钠灯发光效率高、穿透力强、耗电少,寿命长。这种灯发出的光为___________ 色。
(2)碳酸氢钠可做复合膨松剂中的成分,其受热分解的化学方程式是___________ 。
过氧化钠是重要的工业漂白剂。实验小组研究Na2O2与水的反应。
(3)Na2O2与水反应的化学方程式是___________ 。
(4)甲同学向褪色的溶液中滴入两滴酚酞,观察到的现象与实验二相同,甲同学这样做的目的是___________ 。
(5)查阅资料得知,实验二中溶液褪色可能是溶液a中存在较多的H2O2,H2O2将酚酞氧化导致。乙同学通过实验三证实了H2O2的存在:取少量溶液a。加入试剂___________ (填化学式),有无色使带火星木条复燃的气体产生。
(6)为探究现象ii产生的原因,同学们在相同温度下继续进行了如下实验:
实验四:向H2O2溶液中滴入两滴酚酞,振荡。加入5滴0.4%的NaOH溶液,溶液变红又迅速变无色且产生气体,10分钟后溶液变无色。
实验五:向0.4%的NaOH溶液中滴入两滴酚酞,振荡,溶液变红,10分钟后溶液颜色无明显变化:向该溶液中通入氧气。溶液颜色无明显变化。
①实验五通入氧气的目的是___________ 。
②从实验四和实验五中,可得出的结论是___________ 。
(1)高压钠灯发光效率高、穿透力强、耗电少,寿命长。这种灯发出的光为
(2)碳酸氢钠可做复合膨松剂中的成分,其受热分解的化学方程式是
过氧化钠是重要的工业漂白剂。实验小组研究Na2O2与水的反应。
| 操作 | 现象 |
| 实验一:向盛有0.2gNa2O2的烧杯中加入5OmL蒸馏水 | 剧烈反应,产生能使带火星木条复燃的气体,得到溶液a |
| 实验二:恢复室温后向溶液a中滴入两滴酚酞 | i.溶液变红 ii.10分钟后溶液颜色明显变浅。稍后,溶液变为无色 |
(4)甲同学向褪色的溶液中滴入两滴酚酞,观察到的现象与实验二相同,甲同学这样做的目的是
(5)查阅资料得知,实验二中溶液褪色可能是溶液a中存在较多的H2O2,H2O2将酚酞氧化导致。乙同学通过实验三证实了H2O2的存在:取少量溶液a。加入试剂
(6)为探究现象ii产生的原因,同学们在相同温度下继续进行了如下实验:
实验四:向H2O2溶液中滴入两滴酚酞,振荡。加入5滴0.4%的NaOH溶液,溶液变红又迅速变无色且产生气体,10分钟后溶液变无色。
实验五:向0.4%的NaOH溶液中滴入两滴酚酞,振荡,溶液变红,10分钟后溶液颜色无明显变化:向该溶液中通入氧气。溶液颜色无明显变化。
①实验五通入氧气的目的是
②从实验四和实验五中,可得出的结论是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】某实验小组用如图实验装置来模仿防毒面具中的供氧原理。
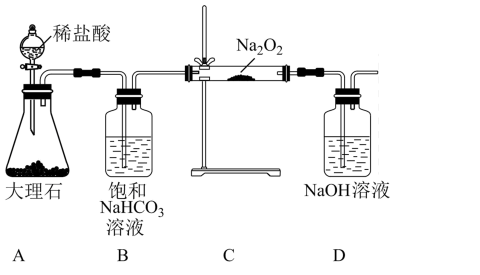
请回答下列问题:
(1)请用离子方程式表示B装置中饱和NaHCO3溶液的作用:_______ ,请写 出装置C中发生的两个化学反应方程式:_______ 、_______ 。
(2)装置C中发生反应的还原剂为_______ (写化学式),每生成1mol O2,转移_______ 个电子。
(3)若反应后装置C中有Na2CO3粉末和少量的NaHCO3固体,除去NaHCO3固体的方法是_______ ,所涉及反应的化学方程式为_______ 。

请回答下列问题:
(1)请用离子方程式表示B装置中饱和NaHCO3溶液的作用:
(2)装置C中发生反应的还原剂为
(3)若反应后装置C中有Na2CO3粉末和少量的NaHCO3固体,除去NaHCO3固体的方法是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】实验室里常用Na2O2与H2O反应快速制取少量的O2,下面装置用来制取O2并演示Na在O2中的燃烧实验。
(1)关闭装置中的止水夹a后,开启活塞b,漏斗中液体不断地往下滴,直至全部流入试管。试判断装置是否漏气________ (填“漏气”、“不漏气” 或“无法确定”)
(2)写出C装置中反应的化学方程式:_________
(3)若装置是不漏气的,打开止水夹a后,用上述装置进行实验。写出A中发生反应的化学方程式,并用双线桥标出化合价变化情况、电子转移的方向和数目及被氧化还原情况_________
(4)B装置中盛放的试剂是__________ ,其作用是___________ D仪器名称是 _____
(5)Fe(OH)2 在潮湿空气中变成灰绿色、红褐色:_________

(1)关闭装置中的止水夹a后,开启活塞b,漏斗中液体不断地往下滴,直至全部流入试管。试判断装置是否漏气
(2)写出C装置中反应的化学方程式:
(3)若装置是不漏气的,打开止水夹a后,用上述装置进行实验。写出A中发生反应的化学方程式,并用双线桥标出化合价变化情况、电子转移的方向和数目及被氧化还原情况
(4)B装置中盛放的试剂是
(5)Fe(OH)2 在潮湿空气中变成灰绿色、红褐色:

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】如图所示,此装置可用来制取和观察Fe(OH)2在空气中被氧化的颜色变化。实验时必须使用铁屑和6 mol·L-1的硫酸,其他试剂任选。填写下列空白:

(1)B中盛有一定量的NaOH溶液,A中应预先加入的药品是_______ ,A中反应的离子方程式是_______
(2)实验开始时先将止水夹a_______ (填“打开”或“关闭”),其目的是_______

(1)B中盛有一定量的NaOH溶液,A中应预先加入的药品是
(2)实验开始时先将止水夹a
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】铁及其化合物在生产、生活中有重要作用。回答下列问题:
I.硫酸亚铁晶体 在医药上常用作补血剂。某课外小组的同学通过实验测定补血剂中硫酸亚铁晶体的质量分数,实验步骤如图所示:
在医药上常用作补血剂。某课外小组的同学通过实验测定补血剂中硫酸亚铁晶体的质量分数,实验步骤如图所示:
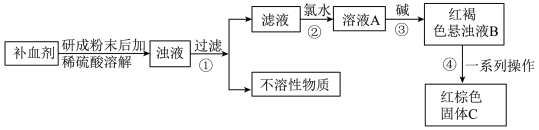
(1)检验经步骤①得到的滤液中是否含有 的方法为
的方法为______ 。
(2)步骤②加入氯水发生反应的离子方程式是______ 。
(3)步骤③产生的红褐色物质成分是______ (写化学式)。
(4)步骤④中一系列操作为______ 、洗涤、干燥、灼烧。
(5)若所取补血剂质量为 ,最终得到红棕色固体
,最终得到红棕色固体 的质量为
的质量为 ,则补血剂中硫酸亚铁晶体的质量分数为
,则补血剂中硫酸亚铁晶体的质量分数为______ (用含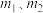 的代数式表示,不考虑实验中铁元素的损失)。
的代数式表示,不考虑实验中铁元素的损失)。
II.高铁酸钾 是一种新型、高效、多功能绿色水处理剂。工业上制备高铁酸钾以及高铁酸钾处理污水的部分流程如下:
是一种新型、高效、多功能绿色水处理剂。工业上制备高铁酸钾以及高铁酸钾处理污水的部分流程如下:

(6)过程①制取 ,理论上需要
,理论上需要 的物质的量为
的物质的量为______ 。步骤②中反应能够发生的原因是______ 。实验室用 饱和溶液制备
饱和溶液制备 胶体的方法是:取
胶体的方法是:取 小烧杯,加入
小烧杯,加入 蒸馏水,将蒸馏水加热至沸腾
蒸馏水,将蒸馏水加热至沸腾______ (将操作补充完整)。
I.硫酸亚铁晶体
 在医药上常用作补血剂。某课外小组的同学通过实验测定补血剂中硫酸亚铁晶体的质量分数,实验步骤如图所示:
在医药上常用作补血剂。某课外小组的同学通过实验测定补血剂中硫酸亚铁晶体的质量分数,实验步骤如图所示:
(1)检验经步骤①得到的滤液中是否含有
 的方法为
的方法为(2)步骤②加入氯水发生反应的离子方程式是
(3)步骤③产生的红褐色物质成分是
(4)步骤④中一系列操作为
(5)若所取补血剂质量为
 ,最终得到红棕色固体
,最终得到红棕色固体 的质量为
的质量为 ,则补血剂中硫酸亚铁晶体的质量分数为
,则补血剂中硫酸亚铁晶体的质量分数为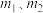 的代数式表示,不考虑实验中铁元素的损失)。
的代数式表示,不考虑实验中铁元素的损失)。II.高铁酸钾
 是一种新型、高效、多功能绿色水处理剂。工业上制备高铁酸钾以及高铁酸钾处理污水的部分流程如下:
是一种新型、高效、多功能绿色水处理剂。工业上制备高铁酸钾以及高铁酸钾处理污水的部分流程如下:
(6)过程①制取
 ,理论上需要
,理论上需要 的物质的量为
的物质的量为 饱和溶液制备
饱和溶液制备 胶体的方法是:取
胶体的方法是:取 小烧杯,加入
小烧杯,加入 蒸馏水,将蒸馏水加热至沸腾
蒸馏水,将蒸馏水加热至沸腾
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】小曹同学计划制备白色的Fe(OH)2沉淀,请帮助他完善实验过程:
I.小曹同学准备用NaOH固体配制240mL 的NaOH溶液。
的NaOH溶液。
(1)本实验必须用到的玻璃仪器有:量筒、胶头滴管、烧杯、___________ 。
(2)要配制出此溶液,小曹同学应称出___________ gNaOH。
(3)在配制过程中,小曹同学的其他操作都是正确的,但下列操作中会引起所配制溶液浓度偏高的一项是___________(填字母)。
Ⅱ.配制完成NaOH溶液后,小曹同学准备利用下述装置和配制好的NaOH溶液、铁屑、稀硫酸等试剂制取Fe(OH)2沉淀
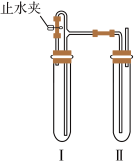
(4)试管I中加入的试剂是___________ 。
(5)小曹同学分别在试管I和Ⅱ中加入试剂,然后迅速打开止水夹,塞紧塞子后检验试管Ⅱ出口处排出的氢气的纯度。当排出的H2纯净时,再夹紧止水夹,此后试管Ⅱ中可以较长时间看到Fe(OH)2白色沉淀,其原因是___________ ,下列操作中也可以实现相同效果的是___________ (填字母)。
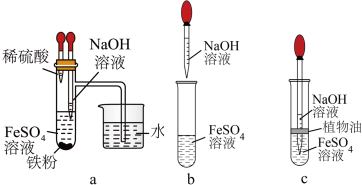
(6)如果Ⅱ中空气未排净,则Fe(OH)2白色沉淀将被氧化为Fe(OH)3,请写出该过程化学方程式_______ 。
I.小曹同学准备用NaOH固体配制240mL
 的NaOH溶液。
的NaOH溶液。(1)本实验必须用到的玻璃仪器有:量筒、胶头滴管、烧杯、
(2)要配制出此溶液,小曹同学应称出
(3)在配制过程中,小曹同学的其他操作都是正确的,但下列操作中会引起所配制溶液浓度偏高的一项是___________(填字母)。
| A.NaOH固体在称量前已部分变质 |
| B.有少量NaOH溶液残留在烧杯里 |
| C.定容时,俯视容量瓶的刻度线 |
| D.定容摇匀后,发现溶液凹液面最低处时低于刻度线,用胶头滴管补水至刻度线 |
Ⅱ.配制完成NaOH溶液后,小曹同学准备利用下述装置和配制好的NaOH溶液、铁屑、稀硫酸等试剂制取Fe(OH)2沉淀

(4)试管I中加入的试剂是
(5)小曹同学分别在试管I和Ⅱ中加入试剂,然后迅速打开止水夹,塞紧塞子后检验试管Ⅱ出口处排出的氢气的纯度。当排出的H2纯净时,再夹紧止水夹,此后试管Ⅱ中可以较长时间看到Fe(OH)2白色沉淀,其原因是

(6)如果Ⅱ中空气未排净,则Fe(OH)2白色沉淀将被氧化为Fe(OH)3,请写出该过程化学方程式
您最近一年使用:0次