已知反应:
①Cl2+2KBr=2KCl+Br2
②KClO3+6HCl=3Cl2↑+KCl+3H2O
③2KBrO3+Cl2=Br2+2KClO3
下列说法错误的是
①Cl2+2KBr=2KCl+Br2
②KClO3+6HCl=3Cl2↑+KCl+3H2O
③2KBrO3+Cl2=Br2+2KClO3
下列说法错误的是
| A.氧化性由弱到强的顺序:Br2<Cl2<KClO3<KBrO3 |
| B.①中KCI是还原产物,KBr发生氧化反应 |
| C.③中1mol氧化剂参加反应得到电子的物质的量为5mol |
| D.反应②中氧化产物与还原产物的物质的量之比为1:1 |
更新时间:2021-10-26 22:19:56
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】已知还原性:SO32->Br-,向含有2molNaBr和2molNa2SO3的混合液中通入 a mol Cl2充分反应,下列说法错误的是
| A.当 a=2 时, 发生的离子反应为 SO32-+Cl2+H2O=SO42-+2H++2Cl- |
| B.当 a≥3 时,发生的离子反应为2SO3+2Br-+3Cl2+2H2O=2SO42-+Br2+4H++6Cl- |
| C.当 2≤a≤3 时,溶液中SO42-、Br-与Cl-的物质的量之比为1:(3-a):a |
| D.当 2≤a≤3 时,溶液中 H+的物质的量为 2mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在常温下,发生下列几种反应:
①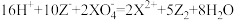
②
③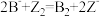
根据上述反应,下列结论判断错误的是
①
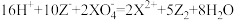
②

③
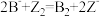
根据上述反应,下列结论判断错误的是
A.溶液中可发生反应: | B. 在③反应中发生氧化反应 在③反应中发生氧化反应 |
C.氧化性强弱的顺序为: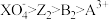 | D. 是 是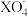 的还原产物 的还原产物 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】锌与很稀的硝酸反应生成硝酸锌、硝酸铵和水。当生成2 mol硝酸锌时,被还原的硝酸的物质的量为
| A.2 mol | B.1 mol | C.0.5 mol | D.0.25 mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】某同学在疫情期间通过KClO3+H2C2O4→CO2↑+ClO2↑+K2CO3+H2O(未配平)的方程自制高效消毒剂ClO2,下列说法正确的是
| A.该反应方程式配平后各物质前的系数分别为2,1,1,2,1,1 |
| B.若有18g H2C2O4参与反应,则会生成8.96L的ClO2气体 |
| C.氧化剂和还原剂的物质的量之比为1:2 |
| D.每生成1mol ClO2转移2NA电子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】世界卫生组织(WHO)和中国卫健委公认二氧化氯(ClO2)为新时代绿色消毒剂。常温下,ClO2气体与Cl2具有相似的颜色与气味,易溶于水,在水中的溶解度是Cl2的5~8倍。ClO2对热、震动、撞击和摩擦相当敏感,极易分解发生爆炸。ClO2几乎不与冷水反应,遇热水则会分解。经研究表明,ClO2反应释放出的原子氧可以氧化色素,所以ClO2也是优良的漂白剂。工业上可采用SO2与氯酸钠在酸性条件下反应制取ClO2,并生成NaHSO4。相信在不久的将来,ClO2将广泛应用到杀菌消毒领域。某兴趣小组取NaClO3样品质量6.0g,通过反应吸收得250mLClO2溶液,取出25.00mL,加入42.00mL0.500mol•L﹣1Fe2+充分反应,过量Fe2+再用0.0500mol•L﹣1K2Cr2O7标准溶液发生反应,恰好反应时消耗K2Cr2O7溶液20.00mL。反应原理如下:
4H++ClO2+5Fe2+═Cl﹣+5Fe3++2H2O
14H++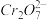 +6Fe2+═2Cr3++6Fe3++7H2O
+6Fe2+═2Cr3++6Fe3++7H2O
若以“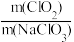 ”作为衡量ClO2产率,则ClO2的“产率”为
”作为衡量ClO2产率,则ClO2的“产率”为
4H++ClO2+5Fe2+═Cl﹣+5Fe3++2H2O
14H++
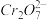 +6Fe2+═2Cr3++6Fe3++7H2O
+6Fe2+═2Cr3++6Fe3++7H2O若以“
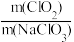 ”作为衡量ClO2产率,则ClO2的“产率”为
”作为衡量ClO2产率,则ClO2的“产率”为| A.33.75% | B.47.25% | C.50.75% | D.67.50% |
您最近一年使用:0次
【推荐2】常温下,将一定量的铁粉加入到50 mL 10 mol·L-1硝酸中,待其充分反应后,收集到的气体换算成标准状况下的体积为4.2 L,所得溶液能够使淀粉碘化钾溶液变蓝,该溶液也能使酸性高锰酸钾褪色。下列说法正确的是
| A.铁与硝酸的反应是吸热反应 | B.生成的气体一定为NO |
| C.反应后硝酸可能有剩余 | D.所得溶液中一定含有Fe2+ |
您最近一年使用:0次

 。关于该反应的叙述不正确的是
。关于该反应的叙述不正确的是 是氧化剂
是氧化剂 还原
还原

