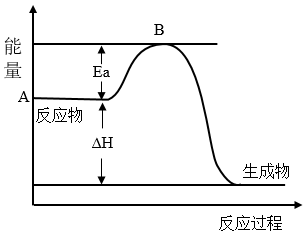
Ⅰ.2SO2(g)+O2(g) 2SO3(g) ΔH=akJ•mol-1,反应过程的能量变化如图所示。已知1molSO2(g)完全转化为1molSO3(g)放热99kJ。请回答:
2SO3(g) ΔH=akJ•mol-1,反应过程的能量变化如图所示。已知1molSO2(g)完全转化为1molSO3(g)放热99kJ。请回答:
(1)a=___ kJ•mol-1。
(2)该反应常用V2O5作催化剂,加入V2O5会使图中B点___ (填“升高”“降低”或“不变”),使图中ΔH___ (填“升高”“降低”或“不变”)。
(3)已知单质硫的燃烧热为296kJ•mol-1,写出反应的热化学方程式:__ 。
(4)工业上用H2和Cl2反应制HCl,各键能数据为:H—H:436kJ/mol,Cl—Cl:243kJ/mol,H—Cl:431kJ/mol。该反应的热化学方程式是__ 。
(5)已知:
①C(s)+O2(g)=CO2(g) ΔH=ΔH1;
②2CO(g)+O2(g)=2CO2(g) ΔH=ΔH2;
③TiO2(g)+2Cl2(g)=TiCl4(s)+O2(g) ΔH=ΔH3;
则TiO2(g)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)的ΔH=___ 。(列出关于ΔH1、ΔH2、ΔH3的表达式)
 2SO3(g) ΔH=akJ•mol-1,反应过程的能量变化如图所示。已知1molSO2(g)完全转化为1molSO3(g)放热99kJ。请回答:
2SO3(g) ΔH=akJ•mol-1,反应过程的能量变化如图所示。已知1molSO2(g)完全转化为1molSO3(g)放热99kJ。请回答:(1)a=
(2)该反应常用V2O5作催化剂,加入V2O5会使图中B点

(3)已知单质硫的燃烧热为296kJ•mol-1,写出反应的热化学方程式:
(4)工业上用H2和Cl2反应制HCl,各键能数据为:H—H:436kJ/mol,Cl—Cl:243kJ/mol,H—Cl:431kJ/mol。该反应的热化学方程式是
(5)已知:
①C(s)+O2(g)=CO2(g) ΔH=ΔH1;
②2CO(g)+O2(g)=2CO2(g) ΔH=ΔH2;
③TiO2(g)+2Cl2(g)=TiCl4(s)+O2(g) ΔH=ΔH3;
则TiO2(g)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)的ΔH=
更新时间:2021-11-04 19:44:23
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】回答下列问题:
(1)能表示反应 的示意图是
的示意图是_______ 。
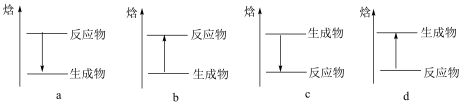
(2)已知:常温常压下,8 g甲烷气体在足量氧气中充分燃烧生成液态水和二氧化碳气体时放出445 kJ热量,写出甲烷气体的燃烧热的热化学方程式:_______ 。
(1)能表示反应
 的示意图是
的示意图是
(2)已知:常温常压下,8 g甲烷气体在足量氧气中充分燃烧生成液态水和二氧化碳气体时放出445 kJ热量,写出甲烷气体的燃烧热的热化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】氨在国民经济中占有重要地位。
(1)合成氨工业中,合成塔中每产生 ,放出
,放出 热量。
热量。
①工业合成氨的热化学方程式是_______ 。
②若起始时向容器内放入 和
和 ,达平衡后放出的热量为Q,则Q(填“>”、“<”或“=”)
,达平衡后放出的热量为Q,则Q(填“>”、“<”或“=”)_______  。
。
③已知:

 键断裂吸收的能量约等于
键断裂吸收的能量约等于_______  。
。
(2)工业生产尿素的原理是以 和
和 为原料合成尿素
为原料合成尿素 ,反应的化学方程式为
,反应的化学方程式为 ,该反应的平衡常数和温度关系如下:
,该反应的平衡常数和温度关系如下:
焓变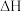 (填“>”、“<”或“=”)
(填“>”、“<”或“=”)_______ 0。
(1)合成氨工业中,合成塔中每产生
 ,放出
,放出 热量。
热量。①工业合成氨的热化学方程式是
②若起始时向容器内放入
 和
和 ,达平衡后放出的热量为Q,则Q(填“>”、“<”或“=”)
,达平衡后放出的热量为Q,则Q(填“>”、“<”或“=”) 。
。③已知:

 键断裂吸收的能量约等于
键断裂吸收的能量约等于 。
。(2)工业生产尿素的原理是以
 和
和 为原料合成尿素
为原料合成尿素 ,反应的化学方程式为
,反应的化学方程式为 ,该反应的平衡常数和温度关系如下:
,该反应的平衡常数和温度关系如下: | 165 | 175 | 185 | 195 |
| K | 111.9 | 74.1 | 50.6 | 34.8 |
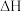 (填“>”、“<”或“=”)
(填“>”、“<”或“=”)
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】(1)在一定条件下N2与H2反应生成NH3,已知拆开1 mol H—H键、1 mol N—H键、1 mol N≡N键分别需要的能量是436 kJ、391 kJ、945.7 kJ,则N2与H2反应生成NH3的热化学方程式为:_____ 。
(2)N2H4和H2O2混合可作火箭推进剂,已知:16 g液态N2H4和足量氧气反应生成N2(g)和H2O(l),放出310.6 kJ 的热量,反应N2H4(l)+O2(g)=N2(g)+2H2O(l)的△H=_____ kJ•mol-1。
已知:2H2O2(l)=O2(g)+2H2O(l) △H=-196.4 kJ•mol-1.N2H4和H2O2反应生成N2(g)和H2O(l)的热化学方程式为_____ 。
(3)实验室用50 mL 0.50 mol•L-1盐酸与50 mL某浓度的NaOH溶液在如下图所示装置中反应,通过测定反应过程中所放出的热量可计算中和热。该装置有一处明显的错误,该处错误是缺少一种玻璃仪器,该仪器的名称为_____ ;实验室提供了0.50 mol•L-1和0.55 mol•L-1两种浓度的NaOH溶液,应选择_____ mol•L-1的溶液进行实验。

(2)N2H4和H2O2混合可作火箭推进剂,已知:16 g液态N2H4和足量氧气反应生成N2(g)和H2O(l),放出310.6 kJ 的热量,反应N2H4(l)+O2(g)=N2(g)+2H2O(l)的△H=
已知:2H2O2(l)=O2(g)+2H2O(l) △H=-196.4 kJ•mol-1.N2H4和H2O2反应生成N2(g)和H2O(l)的热化学方程式为
(3)实验室用50 mL 0.50 mol•L-1盐酸与50 mL某浓度的NaOH溶液在如下图所示装置中反应,通过测定反应过程中所放出的热量可计算中和热。该装置有一处明显的错误,该处错误是缺少一种玻璃仪器,该仪器的名称为

您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】根据实验数据写出下列反应能表现燃烧热的热化学方程式:
(1)沼气是一种能源,它的主要成分是CH4。0.5 mol CH4完全燃烧生成CO2和液态H2O时,放出445 kJ热量__________________________________ 。
(2)18 g葡萄糖固体(C6H12O6)与适量O2反应,生成CO2和液态水,放出280.4 kJ热量__________________________________ 。
(3)SiH4是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2和H2O(l)。已知室温下2 g SiH4自燃放出热量89.2 kJ__________________________________ 。
(1)沼气是一种能源,它的主要成分是CH4。0.5 mol CH4完全燃烧生成CO2和液态H2O时,放出445 kJ热量
(2)18 g葡萄糖固体(C6H12O6)与适量O2反应,生成CO2和液态水,放出280.4 kJ热量
(3)SiH4是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2和H2O(l)。已知室温下2 g SiH4自燃放出热量89.2 kJ
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】写出下列热化学反应方程式:
(1)1molN2(g)与适量H2(g)起反应生成NH3(g),放出92.2kJ热量:_________________________
(2)1molN2(g)与适量O2(g)起反应生成NO2(g),吸收68kJ热量:____________________________
(3)1molCu(s)能与一定量的O2(g)起反应生成CuO(s),放出157kJ热量:____________
(4)1molC8H18(l)在O2(g)中燃烧,生成CO2(g)和H2O(l),放出5518kJ热量:_______________
(1)1molN2(g)与适量H2(g)起反应生成NH3(g),放出92.2kJ热量:
(2)1molN2(g)与适量O2(g)起反应生成NO2(g),吸收68kJ热量:
(3)1molCu(s)能与一定量的O2(g)起反应生成CuO(s),放出157kJ热量:
(4)1molC8H18(l)在O2(g)中燃烧,生成CO2(g)和H2O(l),放出5518kJ热量:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】实验室可用 分解制取
分解制取 ,
, 受热分解的反应分两步进行:
受热分解的反应分两步进行:
①
②
已知:


则反应 的
的
__________  。
。
 分解制取
分解制取 ,
, 受热分解的反应分两步进行:
受热分解的反应分两步进行:①

②

已知:



则反应
 的
的
 。
。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】碳是形成化合物种类最多的元素,其单质及其化合物是人类生产生活的主要能源物质。已知:
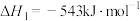 。
。
(1)该反应的熵变
___________ 0(填“>”“<”“=”),该反应自发进行的条件是___________ (填“低温”“高温”或“任意温度”)。
(2)反应
 ,则
,则
___________  (填“>”“<”“=”)。
(填“>”“<”“=”)。
(3)已知:①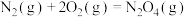
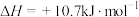
②
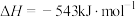
写出气态肼和 反应的热化学方程式:
反应的热化学方程式:___________ 。

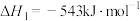 。
。(1)该反应的熵变

(2)反应

 ,则
,则
 (填“>”“<”“=”)。
(填“>”“<”“=”)。(3)已知:①
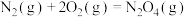
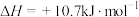
②

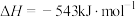
写出气态肼和
 反应的热化学方程式:
反应的热化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】已知:①

②
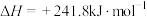
③
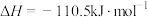
④
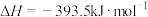
回答下列问题:
(1)上述变化中属于吸热反应的是___________ (填序号)。
(2)写出 燃烧的热化学方程式:
燃烧的热化学方程式:___________ 。
(3)反应 的
的
___________  。
。
(4)相同压强下,质量相等且起始温度相同的两份 与足量的
与足量的 充分反应,分别生成液态水(反应I)和水蒸气(反应Ⅱ),反应I放出的热量
充分反应,分别生成液态水(反应I)和水蒸气(反应Ⅱ),反应I放出的热量___________ (填“>”“<”或“=”)反应Ⅱ放出的热量。
(5)在一定条件下,将 和
和 充入
充入 密闭容器中发生反应生成氨气:
密闭容器中发生反应生成氨气: ,达到平衡时
,达到平衡时 的转化率为
的转化率为 ,放出
,放出 的热量,该反应的平衡常数
的热量,该反应的平衡常数
___________  。写出
。写出 与
与 反应的热化学方程式:
反应的热化学方程式:___________ 。
(6)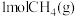 完全燃烧生成气态水的能量变化和
完全燃烧生成气态水的能量变化和 燃烧的能量变化如图所示。在催化剂作用下,
燃烧的能量变化如图所示。在催化剂作用下, 可以还原
可以还原 生成单质
生成单质 、
、 和
和 ,写出该反应的热化学方程式:
,写出该反应的热化学方程式:________ 。



②

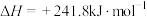
③

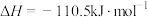
④

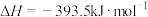
回答下列问题:
(1)上述变化中属于吸热反应的是
(2)写出
 燃烧的热化学方程式:
燃烧的热化学方程式:(3)反应
 的
的
 。
。(4)相同压强下,质量相等且起始温度相同的两份
 与足量的
与足量的 充分反应,分别生成液态水(反应I)和水蒸气(反应Ⅱ),反应I放出的热量
充分反应,分别生成液态水(反应I)和水蒸气(反应Ⅱ),反应I放出的热量(5)在一定条件下,将
 和
和 充入
充入 密闭容器中发生反应生成氨气:
密闭容器中发生反应生成氨气: ,达到平衡时
,达到平衡时 的转化率为
的转化率为 ,放出
,放出 的热量,该反应的平衡常数
的热量,该反应的平衡常数
 。写出
。写出 与
与 反应的热化学方程式:
反应的热化学方程式:(6)
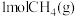 完全燃烧生成气态水的能量变化和
完全燃烧生成气态水的能量变化和 燃烧的能量变化如图所示。在催化剂作用下,
燃烧的能量变化如图所示。在催化剂作用下, 可以还原
可以还原 生成单质
生成单质 、
、 和
和 ,写出该反应的热化学方程式:
,写出该反应的热化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】I.氮是地球上含量丰富的元素,氮及其化合物的研究在生产、生活中有着重要意义。
(1)如图是1molNO2和1molCO反应生成CO2和NO过程中能量变化示意图,写出NO2和CO反应的热化学方程式____ 。

(2)已知:H−H键能为436 kJ∙mol−1,N≡N键能为946 kJ∙mol−1,N−H键能为391 kJ∙mol−1。根据键能计算,消耗1molN2合成氨反应的△H=____ 。
(3)在一固定容积为2L的密闭容器内加入1.5mol的N2和5mol的H2,在一定条件下发生如下反应:N2+3H2 2NH3,若第5分钟时达到平衡,此时测得NH3的物质的量为2mol,请回答下列问题:
2NH3,若第5分钟时达到平衡,此时测得NH3的物质的量为2mol,请回答下列问题:
①前5分钟的平均反应速率υ(NH3)为____ ,平衡时H2的转化率为____ 。
②能说明该合成氨反应一定达到平衡状态的是____ 。
a.容器内N2、H2、NH3的浓度之比为1:3:2
b.NH3的浓度保持不变
c.容器内压强保持不变
d.混合气体的密度保持不变
II.2020年一月一场突如其来的新冠肺炎席卷全球,该病最明显的症状就是出现发热,市售体温枪能快速的检测人体体温,该体温枪所用的电池具有使用寿命长、容量大等特点,应用十分广泛。该种电池由氧化银作为正极,金属锌粉作为负极,电解液为氢氧化钾或氢氧化钠,电池的总反应方程式为Zn+Ag2O+H2O=Zn(OH)2+2Ag,根据信息回答下列问题:
(4)放电时,负极电极反应:____ ;正极电极反应:____ 。
(5)试计算在放电过程中转移3NA个电子时,正极____ (填“增大”或“减小”)的质量的为____ 。
(1)如图是1molNO2和1molCO反应生成CO2和NO过程中能量变化示意图,写出NO2和CO反应的热化学方程式

(2)已知:H−H键能为436 kJ∙mol−1,N≡N键能为946 kJ∙mol−1,N−H键能为391 kJ∙mol−1。根据键能计算,消耗1molN2合成氨反应的△H=
(3)在一固定容积为2L的密闭容器内加入1.5mol的N2和5mol的H2,在一定条件下发生如下反应:N2+3H2
 2NH3,若第5分钟时达到平衡,此时测得NH3的物质的量为2mol,请回答下列问题:
2NH3,若第5分钟时达到平衡,此时测得NH3的物质的量为2mol,请回答下列问题:①前5分钟的平均反应速率υ(NH3)为
②能说明该合成氨反应一定达到平衡状态的是
a.容器内N2、H2、NH3的浓度之比为1:3:2
b.NH3的浓度保持不变
c.容器内压强保持不变
d.混合气体的密度保持不变
II.2020年一月一场突如其来的新冠肺炎席卷全球,该病最明显的症状就是出现发热,市售体温枪能快速的检测人体体温,该体温枪所用的电池具有使用寿命长、容量大等特点,应用十分广泛。该种电池由氧化银作为正极,金属锌粉作为负极,电解液为氢氧化钾或氢氧化钠,电池的总反应方程式为Zn+Ag2O+H2O=Zn(OH)2+2Ag,根据信息回答下列问题:
(4)放电时,负极电极反应:
(5)试计算在放电过程中转移3NA个电子时,正极
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】用Cl2生产某些含氯有机物时会产生副产物HCl。利用反应A,可实现氯的循环利用。
反应A:4HCl+O2 2Cl2+2H2O
2Cl2+2H2O
已知:反应A中,4 mol HCl被氧化,放出115.6 kJ的热量。

(1)H2O的电子式是________ 。
(2)断开1 mol H—O键与断开1 mol H—Cl键所需能量相差约为________ kJ;H2O中H—O键比HCl中H—Cl键________ (填“强”或“弱”)。
反应A:4HCl+O2
 2Cl2+2H2O
2Cl2+2H2O已知:反应A中,4 mol HCl被氧化,放出115.6 kJ的热量。

(1)H2O的电子式是
(2)断开1 mol H—O键与断开1 mol H—Cl键所需能量相差约为
您最近一年使用:0次



