已知下列热化学方程式:
①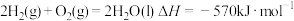
②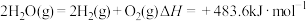
③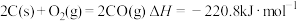
④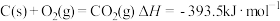
回答下列问题:
(1)上述反应中属于放热反应的是___________ (填写序号)。
(2) 的燃烧热为
的燃烧热为___________ 。
(3)燃烧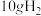 生成液态水,放出的热量为
生成液态水,放出的热量为___________ 。
(4) 的燃烧热的热化学方程式为
的燃烧热的热化学方程式为___________ 。
(5)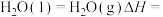
___________ 。
①
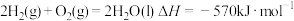
②
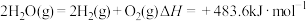
③
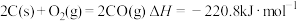
④
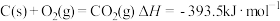
回答下列问题:
(1)上述反应中属于放热反应的是
(2)
 的燃烧热为
的燃烧热为(3)燃烧
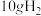 生成液态水,放出的热量为
生成液态水,放出的热量为(4)
 的燃烧热的热化学方程式为
的燃烧热的热化学方程式为(5)
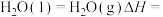
更新时间:2021-11-09 16:41:26
|
相似题推荐
【推荐1】氨气是一种重要的化学物质,可用于制取化肥和硝酸等。
(1)工业合成氨的热化学方程式为:N2(g)+3H2(g) 2NH3(g) △H=-92 kJ/mol
2NH3(g) △H=-92 kJ/mol
表中a为___________ 。
(2)合成氨原料气由天然气在高温下与水和空气反应而得。涉及的主要反应如下:
I.CH4(g)+H2O(g)→CO(g)+3H2(g)
II.2CH4(g)+O2(g)→2CO(g)+4H2(g)
III.CO(g)+H2O(g)→H2(g)+CO2(g)
假设反应产生的CO全部转化为CO2,CO2被碱液完全吸收,剩余的H2O通过冷凝干燥除去。进入合成氨反应塔的原料气为纯净的N2和H2。
①为使原料气中N2和H2的体积比为1:3,推出起始气体中CH4和空气的比例___________ (设空气中O2和N2的体积比为1:4,所有气体均按理想气体处理)。
②已知:IV.C(s)+2H2(g)→CH4(g) ∆H4=-74.8kJ∙mol-1
V.C(s)+ O2(g)→CO(g) ∆H5=-110.5kJ∙mol-1
O2(g)→CO(g) ∆H5=-110.5kJ∙mol-1
计算反应II的反应热___________ 。
(3)合成氨原料中的H2可用CO在高温下与水蒸气反应制得。已知在25℃、101 kPa 下:
I. 2C(石墨,s)+O2(g)=2CO(g) △H1=- 222 kJ/mol
II.2H2(g)+O2(g)=2H2O(g) △H2=- 242 kJ/mol
III.C(石墨,s)+ O2(g)=CO2(g) △H3=- 394kJ/mol
①25℃、101 kPa 下CO与水蒸气反应转化为H2的热化学方程式为___________ 。
②根据反应I、II、III,下列说法正确的是___________ (填选项字母)。
a.由反应II可以推知:2H2(g)+O2(g)=2H2O(l) △H4,则△H4小于△H2
b.反应III的反应热等于O2分子中化学键断裂时所吸收的总能量与CO2分子中化学键形成时所释放的总能量的差
c.下图可表示反应I的反应过程和能量的关系
 。
。
(1)工业合成氨的热化学方程式为:N2(g)+3H2(g)
 2NH3(g) △H=-92 kJ/mol
2NH3(g) △H=-92 kJ/mol| N-H | H-H | N≡N | |
| 断开1 mol化学键需要吸收的能量/kJ | a | 436 | 946 |
表中a为
(2)合成氨原料气由天然气在高温下与水和空气反应而得。涉及的主要反应如下:
I.CH4(g)+H2O(g)→CO(g)+3H2(g)
II.2CH4(g)+O2(g)→2CO(g)+4H2(g)
III.CO(g)+H2O(g)→H2(g)+CO2(g)
假设反应产生的CO全部转化为CO2,CO2被碱液完全吸收,剩余的H2O通过冷凝干燥除去。进入合成氨反应塔的原料气为纯净的N2和H2。
①为使原料气中N2和H2的体积比为1:3,推出起始气体中CH4和空气的比例
②已知:IV.C(s)+2H2(g)→CH4(g) ∆H4=-74.8kJ∙mol-1
V.C(s)+
 O2(g)→CO(g) ∆H5=-110.5kJ∙mol-1
O2(g)→CO(g) ∆H5=-110.5kJ∙mol-1计算反应II的反应热
(3)合成氨原料中的H2可用CO在高温下与水蒸气反应制得。已知在25℃、101 kPa 下:
I. 2C(石墨,s)+O2(g)=2CO(g) △H1=- 222 kJ/mol
II.2H2(g)+O2(g)=2H2O(g) △H2=- 242 kJ/mol
III.C(石墨,s)+ O2(g)=CO2(g) △H3=- 394kJ/mol
①25℃、101 kPa 下CO与水蒸气反应转化为H2的热化学方程式为
②根据反应I、II、III,下列说法正确的是
a.由反应II可以推知:2H2(g)+O2(g)=2H2O(l) △H4,则△H4小于△H2
b.反应III的反应热等于O2分子中化学键断裂时所吸收的总能量与CO2分子中化学键形成时所释放的总能量的差
c.下图可表示反应I的反应过程和能量的关系
 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】天然气中伴随有H2S等合硫化合物,脱硫方法有多种:
(1)一种湿法脱硫是用碳酸钾溶液吸收其中的H2S,同时生成两种酸式盐,该反应的化学方程为___________ 。
(2)一种于法脱硫,其涉及反应:H2(g)+CO(g)+SO2(g) H2O(g)+CO2(g)+S(s)
H2O(g)+CO2(g)+S(s) ,高脱硫率可采取的措施是
,高脱硫率可采取的措施是_____________ 。
a.高压 b.加入催化剂 c.减少CO2的浓度 d.增加CO的浓度 e.分离出硫
(3)用脱硫剂ZDE—01的海绵铁法脱硫,可实现常温脱硫
①脱硫:Fe2O3·H2O(s)+3H2S(g)=Fe2S3·H2O(s)+3H2O(g)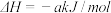
②再生:2Fe2S3·H2O(s)+3O2(g)=2Fe2O3·H2O(s)+6S(s)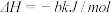
则2H2S(g)+O2(g)=2H2O(g)+2S(s) =
=_______ (用a、b表示)
(4)一种改进的克劳斯法脱硫的工艺,化学反应如下:
H3S+1.5O2=H2O+SO2 SO2+0.5O2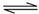 SO3
SO3
SO3(g)+H2O(g)=H2SO4(g) H2SO4(g)+0.17H2O(g) H2SO4(aq)
H2SO4(aq)
该法最终得到的硫酸溶液的质量分数为________ 。
(1)一种湿法脱硫是用碳酸钾溶液吸收其中的H2S,同时生成两种酸式盐,该反应的化学方程为
(2)一种于法脱硫,其涉及反应:H2(g)+CO(g)+SO2(g)
 H2O(g)+CO2(g)+S(s)
H2O(g)+CO2(g)+S(s) ,高脱硫率可采取的措施是
,高脱硫率可采取的措施是a.高压 b.加入催化剂 c.减少CO2的浓度 d.增加CO的浓度 e.分离出硫
(3)用脱硫剂ZDE—01的海绵铁法脱硫,可实现常温脱硫
①脱硫:Fe2O3·H2O(s)+3H2S(g)=Fe2S3·H2O(s)+3H2O(g)
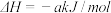
②再生:2Fe2S3·H2O(s)+3O2(g)=2Fe2O3·H2O(s)+6S(s)
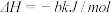
则2H2S(g)+O2(g)=2H2O(g)+2S(s)
 =
=(4)一种改进的克劳斯法脱硫的工艺,化学反应如下:
H3S+1.5O2=H2O+SO2 SO2+0.5O2
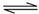 SO3
SO3SO3(g)+H2O(g)=H2SO4(g) H2SO4(g)+0.17H2O(g)
 H2SO4(aq)
H2SO4(aq)该法最终得到的硫酸溶液的质量分数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】2SO2(g)+O2(g)⇌2SO3(g),反应过程的能量变化如图所示.

已知1mol SO2(g)氧化为1mol SO3(g)的△H=-99kJ/mol.
请回答下列问题:
(1)E的大小对该反应的反应热______ 影响?(填“有”或“无”).该反应通常用V2O5作催化剂,加V2O5会使图中B点 ______ (填“升高”或“降低”);
(2)图中△H=______ kJ/mol;
(3)如果反应速率υ(SO2)为0.05mol/(L•min),则υ(O2)=______ mol/(L•min);
(4)1molSO2(g)氧化为1mol SO3(g)的反应热△H1______ 1mol SO3(g)还原为1mol SO2(g)的反应热△H2(填“>、<或=”) 。
(5)已知单质硫的燃烧热为296kJ/mol,计算由S(s)生成3mol SO3(l)的△H=_________________

已知1mol SO2(g)氧化为1mol SO3(g)的△H=-99kJ/mol.
请回答下列问题:
(1)E的大小对该反应的反应热
(2)图中△H=
(3)如果反应速率υ(SO2)为0.05mol/(L•min),则υ(O2)=
(4)1molSO2(g)氧化为1mol SO3(g)的反应热△H1
(5)已知单质硫的燃烧热为296kJ/mol,计算由S(s)生成3mol SO3(l)的△H=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】Ⅰ.现有如下两个反应:
A.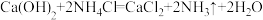
B.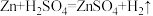
(1)上述反应属于放热反应的是_______ (填“A”或“B”)。
(2)将纯锌片和纯铜片按图方式插入 相同浓度的稀硫酸中一段时间,回答下列问题:
相同浓度的稀硫酸中一段时间,回答下列问题:
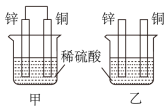
①在甲乙两个烧杯中,甲铜极上发生_______ 反应(填“氧化”或“还原”),乙在_______ 表面产生气泡(填“ ”或“
”或“ ”)。
”)。
②能构成原电池的是_______ 装置(填“甲”或“乙”),其中负极为_______ 电极(填“ ”或“
”或“ ”)。
”)。
③两个装置中 均被腐蚀,若转移
均被腐蚀,若转移 电子,理论上
电子,理论上 片质量减轻
片质量减轻_______ g。
(3)在进行上述实验时发现甲放出气泡的速率较快,为了加快乙的反应速率,可采用的措施有_______ (写出一种即可)。
II.一定条件下,在密闭容器中充入一定量的 和
和 发生反应:
发生反应: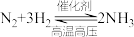 ,各物质的浓度变化如图所示。
,各物质的浓度变化如图所示。
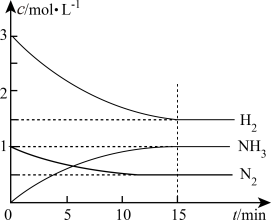
(4)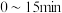 内,平均反应速率
内,平均反应速率 为
为_______ 。
(5)下列叙述能说明该反应已达到平衡状态的是_______。
A.
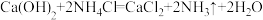
B.
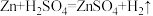
(1)上述反应属于放热反应的是
(2)将纯锌片和纯铜片按图方式插入
 相同浓度的稀硫酸中一段时间,回答下列问题:
相同浓度的稀硫酸中一段时间,回答下列问题:
①在甲乙两个烧杯中,甲铜极上发生
 ”或“
”或“ ”)。
”)。②能构成原电池的是
 ”或“
”或“ ”)。
”)。③两个装置中
 均被腐蚀,若转移
均被腐蚀,若转移 电子,理论上
电子,理论上 片质量减轻
片质量减轻(3)在进行上述实验时发现甲放出气泡的速率较快,为了加快乙的反应速率,可采用的措施有
II.一定条件下,在密闭容器中充入一定量的
 和
和 发生反应:
发生反应: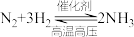 ,各物质的浓度变化如图所示。
,各物质的浓度变化如图所示。
(4)
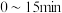 内,平均反应速率
内,平均反应速率 为
为(5)下列叙述能说明该反应已达到平衡状态的是_______。
A. | B.密闭容器内气体总质量保持不变 |
| C.各物质的浓度保持不变 | D.消耗 的同时生成 的同时生成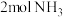 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】镁是很活泼的金属,常用作脱硫剂、脱氧剂。在电子工业中用镁制取硅的反应为:2Mg+SiO2 2MgO+Si,同时有副反应发生:2Mg+Si
2MgO+Si,同时有副反应发生:2Mg+Si Mg2Si,Mg2Si遇盐酸迅速反应生成SiH4,SiH4在常温下是一种不稳定、易分解的气体(燃烧热约为1430
Mg2Si,Mg2Si遇盐酸迅速反应生成SiH4,SiH4在常温下是一种不稳定、易分解的气体(燃烧热约为1430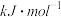 )。如图是进行Mg与SiO2反应的实验装置,试回答下列问题:
)。如图是进行Mg与SiO2反应的实验装置,试回答下列问题:
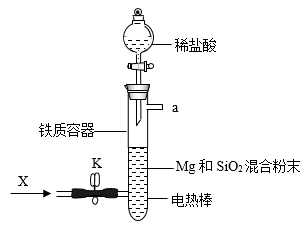
(1)由于O2的存在对该实验有较大影响,实验中应通入X气体作为保护气。X气体应选用①CO2、②N2、③H2中的____________ 。
(2)当接通电源引发反应后,切断电源,反应能继续进行,其原因是____________ 。证明了反应物Mg与SiO2具有的总能量_________ (填“大于”、“小于”或“等于”)生成物MgO和Si具有的总能量。
(3)反应结束时,待冷却至常温后,关闭K,从分液漏斗中加入稀盐酸,可观察到导管口a处有闪亮的火星。据此现象可推知_______ 在空气中能自燃。燃烧的热化学方程式为______ ,当产生等量的热量时,燃烧CH4和SiH4的物质的量之比为_______ (CH4的燃烧热是890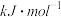 )
)
 2MgO+Si,同时有副反应发生:2Mg+Si
2MgO+Si,同时有副反应发生:2Mg+Si Mg2Si,Mg2Si遇盐酸迅速反应生成SiH4,SiH4在常温下是一种不稳定、易分解的气体(燃烧热约为1430
Mg2Si,Mg2Si遇盐酸迅速反应生成SiH4,SiH4在常温下是一种不稳定、易分解的气体(燃烧热约为1430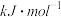 )。如图是进行Mg与SiO2反应的实验装置,试回答下列问题:
)。如图是进行Mg与SiO2反应的实验装置,试回答下列问题:
(1)由于O2的存在对该实验有较大影响,实验中应通入X气体作为保护气。X气体应选用①CO2、②N2、③H2中的
(2)当接通电源引发反应后,切断电源,反应能继续进行,其原因是
(3)反应结束时,待冷却至常温后,关闭K,从分液漏斗中加入稀盐酸,可观察到导管口a处有闪亮的火星。据此现象可推知
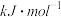 )
)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】某化学反应中,设反应物的总能量为E1,生成物的总能量为E2,

(1)若E1>E2,则该反应为_____________ (填“放热”或“吸热”)反应。该反应可用图_____________ (填“A”或“B”)表示。
(2)若E1<E2,则该反应为_____________ (填“放热”或“吸热”)反应。该反应可用图___________ (填“A”或“B”)表示
(3)太阳能的开发和利用是21世纪的一个重要课题。
①利用储能介质储存太阳能的原理是白天在太阳照射下,某种盐熔化,吸收热量;晚间熔盐释放出相应能量,从而使室温得以调节。已知下列数据:
其中最适宜作储能介质的一种盐是_____________ (填字母)。
A CaCl2·6H2O
B Na2SO4·l0H2O
C Na2HPO4·12H2O
D Na2S2O3·5H2O

②图是一种太阳能热水器的示意图,图中A是集热器,B是储水容器,C是供阴天时加热的辅助电热器。根据对水的密度的认识,你估计在阳光照射下水将沿_________ (填“顺”或“逆”)时针方向流动。

(1)若E1>E2,则该反应为
(2)若E1<E2,则该反应为
(3)太阳能的开发和利用是21世纪的一个重要课题。
①利用储能介质储存太阳能的原理是白天在太阳照射下,某种盐熔化,吸收热量;晚间熔盐释放出相应能量,从而使室温得以调节。已知下列数据:
| 盐 | 熔点/℃ | 熔化吸热KJ·mol-1 | 参考价格/元 |
| CaCl2·6H2O | 29.0 | 37.3 | 780〜850 |
| Na2SO4·l0H2O | 32.4 | 77.0 | 800〜900 |
| Na2HPO4·12H2O | 36.1 | 100.1 | 1600-2000 |
| Na2S2O3·5H2O | 48.5 | 49.7 | 1400-1800 |
其中最适宜作储能介质的一种盐是
A CaCl2·6H2O
B Na2SO4·l0H2O
C Na2HPO4·12H2O
D Na2S2O3·5H2O

②图是一种太阳能热水器的示意图,图中A是集热器,B是储水容器,C是供阴天时加热的辅助电热器。根据对水的密度的认识,你估计在阳光照射下水将沿
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】我国利用焦炉煤气制取甲醇及二甲醚技术已日臻成熟。回答下列问题:
(1)已知下列反应的热化学方程式:
①
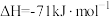
②
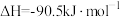
③
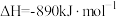
则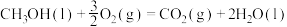 的
的
_______  。
。
(2)二甲醚(DME)被誉为“21世纪的清洁燃料”。由合成气制备二甲醚的主要原理如下:
Ⅰ.
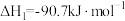 ,
, ;
;
Ⅱ.
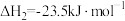 ,
, ;
;
Ⅲ.
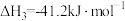 ,
, 。
。
①下列措施中,能提高平衡时 产量的有
产量的有_______ (填字母)。
A.使用过量的 B.升高温度 C.增大压强
B.升高温度 C.增大压强
②一定温度下,将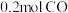 和
和 通入
通入 恒容密闭容器中,发生反应Ⅲ,
恒容密闭容器中,发生反应Ⅲ, 后达到平衡状态,平衡后测得
后达到平衡状态,平衡后测得 的体积分数为20%。则
的体积分数为20%。则 内
内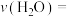
_______ , 的转化率
的转化率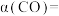
_______ ,
_______ (用最简分数表示)。再往该平衡体系中充入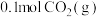 和
和 ,则平衡向
,则平衡向_______ (填“正向”“逆向”或“不”)移动, 的转化率
的转化率_______ (填“增大”“减小”或“不变”)。
(1)已知下列反应的热化学方程式:
①

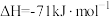
②

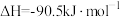
③

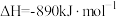
则
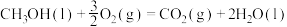 的
的
 。
。(2)二甲醚(DME)被誉为“21世纪的清洁燃料”。由合成气制备二甲醚的主要原理如下:
Ⅰ.

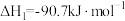 ,
, ;
;Ⅱ.

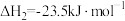 ,
, ;
;Ⅲ.

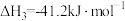 ,
, 。
。①下列措施中,能提高平衡时
 产量的有
产量的有A.使用过量的
 B.升高温度 C.增大压强
B.升高温度 C.增大压强②一定温度下,将
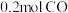 和
和 通入
通入 恒容密闭容器中,发生反应Ⅲ,
恒容密闭容器中,发生反应Ⅲ, 后达到平衡状态,平衡后测得
后达到平衡状态,平衡后测得 的体积分数为20%。则
的体积分数为20%。则 内
内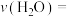
 的转化率
的转化率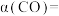

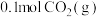 和
和 ,则平衡向
,则平衡向 的转化率
的转化率
您最近一年使用:0次
【推荐2】回答下列问题
(1)甲醇是人们开发和利用的一种新能源。已知:
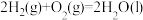
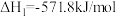
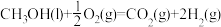
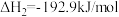
①表示甲醇燃烧热的热化学方程式为___________ ;
②上述第二个反应的能量变化如图所示,则 =
=___________ kJmol。(用E1、E2的相关式子表示);

(2)已知反应
 ,试根据表中所列键能数据估算a=
,试根据表中所列键能数据估算a=___________ 。
(3) 和
和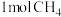 完全燃烧放出的热量分别为:286kJ、890kJ,等质量的H2和CH4完全燃烧放出的热量,
完全燃烧放出的热量分别为:286kJ、890kJ,等质量的H2和CH4完全燃烧放出的热量,___________ (填化学式)放出的热量多。
(4)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水,当它们混合反应时,即产生大量氮气和水蒸气,并放出大量热。已知0.4mol液态肼与足量液态双氧水反应,生成氮气和水蒸气,放出256kJ的热量。
①写出该反应的热化学方程式:___________ 。
②此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是___________ 。
(1)甲醇是人们开发和利用的一种新能源。已知:
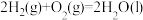
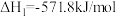
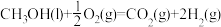
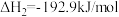
①表示甲醇燃烧热的热化学方程式为
②上述第二个反应的能量变化如图所示,则
 =
=
(2)已知反应

 ,试根据表中所列键能数据估算a=
,试根据表中所列键能数据估算a=| 化学键 | H-H | N-H | N≡N |
| 键能/kJ/mol | 436 | 391 | 945 |
 和
和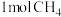 完全燃烧放出的热量分别为:286kJ、890kJ,等质量的H2和CH4完全燃烧放出的热量,
完全燃烧放出的热量分别为:286kJ、890kJ,等质量的H2和CH4完全燃烧放出的热量,(4)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水,当它们混合反应时,即产生大量氮气和水蒸气,并放出大量热。已知0.4mol液态肼与足量液态双氧水反应,生成氮气和水蒸气,放出256kJ的热量。
①写出该反应的热化学方程式:
②此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】氢能是发展中的新能源,它的利用包括氢的制备、储存和应用三个环节。回答下列问题:
(1)通过以下反应均可获取H2。下列有关说法正确的是(_____ )
①太阳光催化分解水制氢:2H2O(l)=2H2(g)+ O2(g) ΔH1=571.6kJ·mol–1
②焦炭与水反应制氢:C(s)+ H2O(g) =CO(g)+ H2(g)ΔH2=131.3kJ·mol–1
③甲烷与水反应制氢:CH4(g)+ H2O(g)=CO(g)+3H2(g)ΔH3=206.1kJ·mol–1
A.反应①中电能转化为化学能
B.反应②为放热反应
C.反应③使用催化剂,ΔH3减小
D.反应CH4(g)=C(s)+2H2(g)的ΔH=74.8kJ·mol–1
(2)俄罗斯用“质子﹣M”号运载火箭成功将“光线”号卫星送入预定轨道。发射用的运载火箭使用的是以液氢为燃烧剂,液氧为氧化剂的高能低温推进剂,已知:
①H2(g)=H2(l)△H1=﹣0.92kJ·mol﹣1
②O2(g)=O2(l)△H2=﹣6.84kJ·mol﹣1
③有关过程如图:
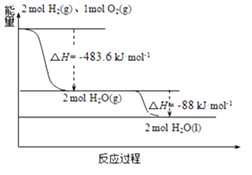
下列说法正确的是(_____ )
A.2mol H2(g)与1mol O2(g)所具有的总能量比2molH2O(g)所具有的总能量低
B.氢气的燃烧热为△H=﹣241.8 kJ·mol﹣1
C.火箭液氢燃烧的热化学方程式2H2(l)+O2(l)═2H2O(g)△H=﹣474.92kJ·mol﹣1
D.H2O(g)变成H2O(l)的过程中,断键吸收的能量小于成键放出的能量
(3)氢气可用于制备H2O2。已知:
H2(g)+A(l)=B(l) ΔH1
O2(g)+B(l)=A(l)+H2O2(l) ΔH2
其中A、B为有机物,两反应均为自发反应,则H2(g)+ O2(g)= H2O2(l)的ΔH____ 0(填“>”、“<”或“=”)。
(4)①合金贮氢材料具有优异的吸收氢性能,在配合氢能的开发中起到重要作用。贮氢合金ThNi5可催化由CO、H2合成CH4的反应,已知温度为T时:
CH4(g)+2H2O=CO2(g)+4H2(g) △H=+165kJ•mol
CO(g)+H2O(g)=CO2(g)+H2(g) △H=-41kJ•mol
则温度为T时,该反应的热化学方程式为_________ 。
②研究表明过渡金属型氢化物(又称间充氢化物),在这类氢化物中,氢原子填充在金属的晶格间隙之间,其组成不固定,通常是非化学计量的,如:LaH2.76、TiH1.73、CeH2.69、ZrH1.98、PrH2.85、TaH0.78。已知标准状况下,1体积的钯粉大约可吸附896体积的氢气(钯粉的密度为10.64 g/cm3,相对原子质量为106.4),试写出钯(Pd)的氢化物的化学式____________ 。
(5)甲醇是重要的化工原料,又可称为燃料。利用合成气(主要成分为CO、CO2和H2 ,其中CO分子为C≡O)在催化剂的作用下合成甲醇,发生的主反应如下:
①CO(g)+2H2(g) CH3OH(g) △H1
CH3OH(g) △H1
②CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H2
CH3OH(g)+H2O(g) △H2
③CO2(g)+H2(g) CO(g)+H2O(g) △H3
CO(g)+H2O(g) △H3
回答下列问题:
(1)已知反应①中的相关的化学键键能数据如下:
由此计算△H1=___ kJ·mol-1,已知△H2=-58kJ·mol-1,则△H3=___ kJ·mol-1。
(1)通过以下反应均可获取H2。下列有关说法正确的是(
①太阳光催化分解水制氢:2H2O(l)=2H2(g)+ O2(g) ΔH1=571.6kJ·mol–1
②焦炭与水反应制氢:C(s)+ H2O(g) =CO(g)+ H2(g)ΔH2=131.3kJ·mol–1
③甲烷与水反应制氢:CH4(g)+ H2O(g)=CO(g)+3H2(g)ΔH3=206.1kJ·mol–1
A.反应①中电能转化为化学能
B.反应②为放热反应
C.反应③使用催化剂,ΔH3减小
D.反应CH4(g)=C(s)+2H2(g)的ΔH=74.8kJ·mol–1
(2)俄罗斯用“质子﹣M”号运载火箭成功将“光线”号卫星送入预定轨道。发射用的运载火箭使用的是以液氢为燃烧剂,液氧为氧化剂的高能低温推进剂,已知:
①H2(g)=H2(l)△H1=﹣0.92kJ·mol﹣1
②O2(g)=O2(l)△H2=﹣6.84kJ·mol﹣1
③有关过程如图:

下列说法正确的是(
A.2mol H2(g)与1mol O2(g)所具有的总能量比2molH2O(g)所具有的总能量低
B.氢气的燃烧热为△H=﹣241.8 kJ·mol﹣1
C.火箭液氢燃烧的热化学方程式2H2(l)+O2(l)═2H2O(g)△H=﹣474.92kJ·mol﹣1
D.H2O(g)变成H2O(l)的过程中,断键吸收的能量小于成键放出的能量
(3)氢气可用于制备H2O2。已知:
H2(g)+A(l)=B(l) ΔH1
O2(g)+B(l)=A(l)+H2O2(l) ΔH2
其中A、B为有机物,两反应均为自发反应,则H2(g)+ O2(g)= H2O2(l)的ΔH
(4)①合金贮氢材料具有优异的吸收氢性能,在配合氢能的开发中起到重要作用。贮氢合金ThNi5可催化由CO、H2合成CH4的反应,已知温度为T时:
CH4(g)+2H2O=CO2(g)+4H2(g) △H=+165kJ•mol
CO(g)+H2O(g)=CO2(g)+H2(g) △H=-41kJ•mol
则温度为T时,该反应的热化学方程式为
②研究表明过渡金属型氢化物(又称间充氢化物),在这类氢化物中,氢原子填充在金属的晶格间隙之间,其组成不固定,通常是非化学计量的,如:LaH2.76、TiH1.73、CeH2.69、ZrH1.98、PrH2.85、TaH0.78。已知标准状况下,1体积的钯粉大约可吸附896体积的氢气(钯粉的密度为10.64 g/cm3,相对原子质量为106.4),试写出钯(Pd)的氢化物的化学式
(5)甲醇是重要的化工原料,又可称为燃料。利用合成气(主要成分为CO、CO2和H2 ,其中CO分子为C≡O)在催化剂的作用下合成甲醇,发生的主反应如下:
①CO(g)+2H2(g)
 CH3OH(g) △H1
CH3OH(g) △H1②CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H2
CH3OH(g)+H2O(g) △H2③CO2(g)+H2(g)
 CO(g)+H2O(g) △H3
CO(g)+H2O(g) △H3回答下列问题:
(1)已知反应①中的相关的化学键键能数据如下:
| 化学键 | H—H | C—O | C≡O | H—O | C—H |
| E/(kJ.mol-1) | 436 | 343 | 1076 | 465 | 413 |
由此计算△H1=
您最近一年使用:0次
【推荐1】葡萄糖是人体所需能量的重要来源之一。葡萄糖燃烧的热化学方程式为:C6H12O6(s)+6O2(g)=6CO2(g)+6H2O(l) ΔH=-2 800 kJ/mol,葡萄糖在人体组织中氧化的热化学方程式与它燃烧的热化学方程式相同。
计算:
(1)100 g葡萄糖在人体中完全氧化时所产生的热量_______ 。
(2)生成18 g水时放出的热量_______ 。
计算:
(1)100 g葡萄糖在人体中完全氧化时所产生的热量
(2)生成18 g水时放出的热量
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】根据要求回答下列问题:
(1)机动车尾气已成为城市大气的主要污染源,机动车尾气中的主要有害物质为氮的氧化物。目前科技工作者正在探索用甲烷等燃料气体将氮氧化物还原为N2和H2O,涉及的反应有:
CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(g) ΔH1=-574 kJ·mol-1
CH4(g)+2NO2(g)===CO2(g)+2H2O(g)+N2(g) ΔH2=-867 kJ·mol-1
写出CH4还原NO生成N2的热化学方程式:______________________________ 。
(2)一定条件下,不同量的CO2与不同量的NaOH充分反应放出的热量如下表所示:
写出该条件下,CO2与NaOH反应生成NaHCO3的热化学方程式:
______________________________________________ 。
(3)我国煤炭资源相对石油和天然气资源丰富,煤的综合利用主要是指煤的气化和液化。煤的主要成分为碳氢化合物,用CH代表煤的“分子式”。已知:
煤炭在氧气氛围中气化 2CH(s)+O2(g)===2CO(g)+H2(g) ΔH1
气化后的气体合成甲醇 CO(g)+2H2(g)===CH3OH(g) ΔH2
甲醇制备丙烯的反应 3CH3OH(g)===C3H6(g)+3H2O(g) ΔH3
写出在一定条件下,煤炭在氧气氛围中反应直接生成丙烯、水蒸气和CO的热化学方程式:
______________________________________ 。
(1)机动车尾气已成为城市大气的主要污染源,机动车尾气中的主要有害物质为氮的氧化物。目前科技工作者正在探索用甲烷等燃料气体将氮氧化物还原为N2和H2O,涉及的反应有:
CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(g) ΔH1=-574 kJ·mol-1
CH4(g)+2NO2(g)===CO2(g)+2H2O(g)+N2(g) ΔH2=-867 kJ·mol-1
写出CH4还原NO生成N2的热化学方程式:
(2)一定条件下,不同量的CO2与不同量的NaOH充分反应放出的热量如下表所示:
| CO2的量 | NaOH的量 | 放出的热量 |
| 22.0 g | 750 mL 1.0 mol·L-1 | x kJ |
| 1.0 mol | 2.0 L 1.0 mol·L-1 | y kJ |
写出该条件下,CO2与NaOH反应生成NaHCO3的热化学方程式:
(3)我国煤炭资源相对石油和天然气资源丰富,煤的综合利用主要是指煤的气化和液化。煤的主要成分为碳氢化合物,用CH代表煤的“分子式”。已知:
煤炭在氧气氛围中气化 2CH(s)+O2(g)===2CO(g)+H2(g) ΔH1
气化后的气体合成甲醇 CO(g)+2H2(g)===CH3OH(g) ΔH2
甲醇制备丙烯的反应 3CH3OH(g)===C3H6(g)+3H2O(g) ΔH3
写出在一定条件下,煤炭在氧气氛围中反应直接生成丙烯、水蒸气和CO的热化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】红磷在氯气中燃烧的能量变化关系如图所示。
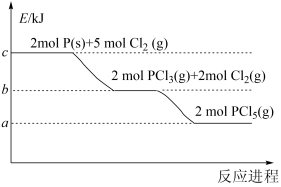
(1)反应PCl3(g)+Cl2(g)=PCl5(g)是___________ (填“吸热”或“放热”)反应。
(2)写出固态红磷在足量的氯气中完全燃烧生成气态物质的热化学方程式:___________ 。
(3)6.2 g红磷在8.96 L(标准状况)氯气中完全燃烧生成气态物质时,放出的热量为___________ kJ(用含a、b、c的代数式表示)。
(4)白磷在氧气中燃烧有如下转化关系。
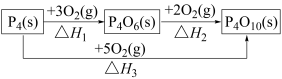
其中ΔH2=___________ (用含ΔH1和ΔH3的代数式表示)。
(5)用烧碱溶液吸收五氯化磷尾气生成两种正盐,写出该反应的离子方程式:___________ 。

(1)反应PCl3(g)+Cl2(g)=PCl5(g)是
(2)写出固态红磷在足量的氯气中完全燃烧生成气态物质的热化学方程式:
(3)6.2 g红磷在8.96 L(标准状况)氯气中完全燃烧生成气态物质时,放出的热量为
(4)白磷在氧气中燃烧有如下转化关系。
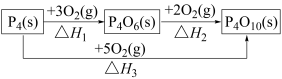
其中ΔH2=
(5)用烧碱溶液吸收五氯化磷尾气生成两种正盐,写出该反应的离子方程式:
您最近一年使用:0次



