某学习小组为认识铁及其化合物的性质、分散系的性质做了如下一组综合实验,根据实验流程回答相关问题:

(1)请写出Fe2O3与①反应的离子方程式:___________ 。
(2)物质②为___________ 。
(3)请写出FeCl3溶液与铁粉反应的化学方程式:___________ 。
(4)向FeCl2溶液中滴加NaOH溶液最终生成Fe(OH)3浊液,该过程的现象为___________ ,此过程中发生的氧化还原反应为___________ (用化学方程式表达)。
(5)将FeCl3饱和溶液滴入沸水中,并继续煮沸至红褐色,制得胶体,它与FeCl3溶液、Fe(OH)3浊液的本质区别是___________ 。

(1)请写出Fe2O3与①反应的离子方程式:
(2)物质②为
(3)请写出FeCl3溶液与铁粉反应的化学方程式:
(4)向FeCl2溶液中滴加NaOH溶液最终生成Fe(OH)3浊液,该过程的现象为
(5)将FeCl3饱和溶液滴入沸水中,并继续煮沸至红褐色,制得胶体,它与FeCl3溶液、Fe(OH)3浊液的本质区别是
更新时间:2021-03-19 20:24:39
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】Fe(OH)3胶体的制备实验原理及操作如下:

(1)方法:在小烧杯中加入40 mL蒸馏水,加热至沸腾,向沸水中___________ 。继续煮沸至液体___________ ,停止加热,即可得到Fe(OH)3胶体。
(2)原理:FeCl3 + 3H2O
________ + 3HCl
(3)利用___________ 可以鉴别Fe(OH)3胶体和FeCl3溶液。

(1)方法:在小烧杯中加入40 mL蒸馏水,加热至沸腾,向沸水中
(2)原理:FeCl3 + 3H2O

(3)利用
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)向Fe(OH)3胶体中逐滴滴入过量的盐酸,会出现一系列变化:先出现________ ,随后_________________ ,原因(用离子方程式和适当的文字表示) ____________
(2)实验室用饱和溶液制取Fe(OH)3 胶体的实验操作过程是_________ 。现有NaCl溶液和Fe(OH)3 胶体的混合体系,若要除去 Fe(OH)3 胶体,可以采用的操作是______ ,若要除去体系中的Na+ 和Cl-,可以采用_____ 的方法。
(2)实验室用饱和溶液制取Fe(OH)3 胶体的实验操作过程是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】现有以下物质:①NaOH溶液;②液氨;③BaCO3固体;④熔融KHSO4;⑤Fe(OH)3胶体;⑥铜;⑦CO2;⑧CH3COOH;⑨蔗糖;⑩冰水混合物
(1)以上物质中属于混合物的是________ (填序号),以上物质中属于电解质的是_______ (填序号);以上纯净物中能导电的是_______ (填序号)。
(2)写出制备物质⑤的化学方程式________ ,在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮沸至溶液呈红褐色,即制得Fe(OH)3胶体。鉴别胶体成功制备最简单的方法是_________ 。
(3)在含40g溶质的①溶液中缓缓通入标准状况下66gCO2,则反应后溶液的溶质有______ (填化学式),该过程的离子反应方程式为___________ 。
(1)以上物质中属于混合物的是
(2)写出制备物质⑤的化学方程式
(3)在含40g溶质的①溶液中缓缓通入标准状况下66gCO2,则反应后溶液的溶质有
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】将下列有关铁及其化合物的性质或用途的字母序号与所对应的物质对应起来:
A.具有磁性的黑色固体;B.用于治疗缺铁性贫血;C.涂料中的红色颜料;D.用于保存亚铁盐溶液;E.在空气中很不稳定;F.遇KSCN溶液变色
(1)铁单质
(2)三氧化二铁
(3)四氧化三铁
(4)氢氧化亚铁
(5)亚铁盐
(6)铁盐
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】电子工业常用30%的 溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。
溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。
(1)检验溶液中 存在的试剂是
存在的试剂是_______ ,证明 存在的现象是
存在的现象是_______ 。
(2)写出 溶液与金属铜发生反应的离子方程式
溶液与金属铜发生反应的离子方程式_______ 。
(3)某工程师为了从使用过的腐蚀废液(主要含 、
、 、
、 、
、 )中回收铜,并重新获得纯净的
)中回收铜,并重新获得纯净的 溶液,准备采用图示步骤。
溶液,准备采用图示步骤。
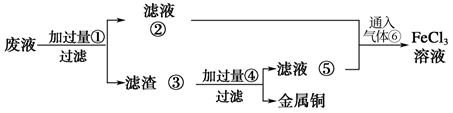
请写出上述实验中加入或生成的有关物质的化学式:①_______ ,④_______ 。
(4)将铜片放入
 溶液中,反应一段时间后取出铜片,溶液中
溶液中,反应一段时间后取出铜片,溶液中 ,则此时溶液中的
,则此时溶液中的 与
与 的物质的量之比为
的物质的量之比为_______ 。
 溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。
溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。(1)检验溶液中
 存在的试剂是
存在的试剂是 存在的现象是
存在的现象是(2)写出
 溶液与金属铜发生反应的离子方程式
溶液与金属铜发生反应的离子方程式(3)某工程师为了从使用过的腐蚀废液(主要含
 、
、 、
、 、
、 )中回收铜,并重新获得纯净的
)中回收铜,并重新获得纯净的 溶液,准备采用图示步骤。
溶液,准备采用图示步骤。
请写出上述实验中加入或生成的有关物质的化学式:①
(4)将铜片放入

 溶液中,反应一段时间后取出铜片,溶液中
溶液中,反应一段时间后取出铜片,溶液中 ,则此时溶液中的
,则此时溶液中的 与
与 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】硫酸亚铁铵[(NH4)2Fe(SO4)2•6H2O,相对分子质量392]晶体又称莫尔盐,易溶易电离但却比一般的亚铁盐稳定,因此广泛应用于制药、电镀以及定量分析。回答下列与之有关的问题:
(1)在莫尔盐所涉及的五种元素中:
①S元素在门捷列夫元素周期表中的位置是______________ ;
②其中处于同主族的两种元素非金属性更强的是:_____________ 。
(2)为检验莫尔盐是否变质,可用的试剂为_______________ 。
碘是合成人体甲状腺激素的重要原料,食盐中加KIO3是我国为解决普遍性碘缺乏问题的国家规定,下图是自动电位滴定法测定食盐中碘含量的实验过程:
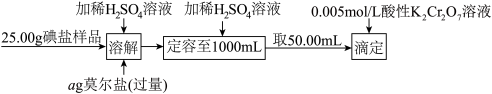
(3)已知“溶解”过程中IO3-的还原产物为碘单质,写出该反应的离子反应方程式:______________________________ 。
(4)取50. 00 mL样品,用0.005 mol/L酸性K2Cr2O7溶液滴定剩余Fe2+,滴定操作时使用的锥形瓶未干燥,导致结果_____________ (填“偏大”“偏小”或“无影响”)
(1)在莫尔盐所涉及的五种元素中:
①S元素在门捷列夫元素周期表中的位置是
②其中处于同主族的两种元素非金属性更强的是:
(2)为检验莫尔盐是否变质,可用的试剂为
碘是合成人体甲状腺激素的重要原料,食盐中加KIO3是我国为解决普遍性碘缺乏问题的国家规定,下图是自动电位滴定法测定食盐中碘含量的实验过程:

(3)已知“溶解”过程中IO3-的还原产物为碘单质,写出该反应的离子反应方程式:
(4)取50. 00 mL样品,用0.005 mol/L酸性K2Cr2O7溶液滴定剩余Fe2+,滴定操作时使用的锥形瓶未干燥,导致结果
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】铁及其化合物与生产、生活关系密切
(1)生铁(以赤铁矿为例)是通过高炉冶炼而得,用化学方程式表示其原理为__________
(2)在钢铁厂的生产中,炽热的铁水注入模具之前,必须对模具进行充分的干燥处理,不得留有水,原因是__________ (用化学方程式表示)
(3)用废铁皮制取铁红(Fe2O3)的部分流程示意图如下:
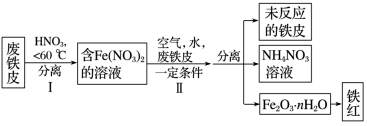
①步骤Ⅰ若要检验是否有Fe3+生成,方法是__________
②步骤Ⅱ中发生反应: ,反应产生的HNO3又将废铁皮中的铁转化为Fe(NO3)2,能体现“绿色化学”思想的是
,反应产生的HNO3又将废铁皮中的铁转化为Fe(NO3)2,能体现“绿色化学”思想的是__________ (任写一项)。
(4) Fe2O3可制取新型、高效水处理剂高铁酸钾K2FeO4
______ Fe2O3+______NaClO+______KOH ______ K2FeO4(高铁酸钾)+ _____NaCl+_____H2O
______ K2FeO4(高铁酸钾)+ _____NaCl+_____H2O
①K2FeO4中铁元素的化合价__________ ;配平上述反应__________ 。此过程中氧化剂是__________ (填化学式)。
②高铁酸钾(K2FeO4)是一种新型、高效的绿色水处理剂,在水中反应生成氢氧化铁胶体。高铁酸钾作为水处理剂的作用是__________ 、__________ 。
(1)生铁(以赤铁矿为例)是通过高炉冶炼而得,用化学方程式表示其原理为
(2)在钢铁厂的生产中,炽热的铁水注入模具之前,必须对模具进行充分的干燥处理,不得留有水,原因是
(3)用废铁皮制取铁红(Fe2O3)的部分流程示意图如下:

①步骤Ⅰ若要检验是否有Fe3+生成,方法是
②步骤Ⅱ中发生反应:
 ,反应产生的HNO3又将废铁皮中的铁转化为Fe(NO3)2,能体现“绿色化学”思想的是
,反应产生的HNO3又将废铁皮中的铁转化为Fe(NO3)2,能体现“绿色化学”思想的是(4) Fe2O3可制取新型、高效水处理剂高铁酸钾K2FeO4
______ Fe2O3+______NaClO+______KOH
 ______ K2FeO4(高铁酸钾)+ _____NaCl+_____H2O
______ K2FeO4(高铁酸钾)+ _____NaCl+_____H2O①K2FeO4中铁元素的化合价
②高铁酸钾(K2FeO4)是一种新型、高效的绿色水处理剂,在水中反应生成氢氧化铁胶体。高铁酸钾作为水处理剂的作用是
您最近一年使用:0次
填空题
|
适中
(0.65)
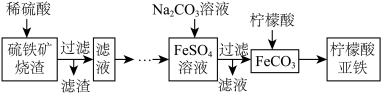
【推荐2】某研究性学习小组从硫铁矿烧渣(主要成分为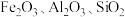 )出发,设计了如下流程,制得硫酸亚铁溶液,最终获得柠檬酸亚铁:
)出发,设计了如下流程,制得硫酸亚铁溶液,最终获得柠檬酸亚铁:
下表列出了有关金属离子生成氢氧化物沉淀的 (开始沉淀的
(开始沉淀的 按金属离子浓度为
按金属离子浓度为 计算)
计算)
(1)由硫铁矿烧渣制备柠檬酸亚铁溶液的过程中过量硫酸的作用是_______________ 。
(2)请结合所学知识补全流程中缺少的操作步骤。_________________
 )出发,设计了如下流程,制得硫酸亚铁溶液,最终获得柠檬酸亚铁:
)出发,设计了如下流程,制得硫酸亚铁溶液,最终获得柠檬酸亚铁:
下表列出了有关金属离子生成氢氧化物沉淀的
 (开始沉淀的
(开始沉淀的 按金属离子浓度为
按金属离子浓度为 计算)
计算)| 金属离子 | 开始沉淀的 | 完全沉淀的 |
 | 1.1 | 3.2 |
 | 3.0 | 5.0 |
 | 5.8 | 8.8 |
(1)由硫铁矿烧渣制备柠檬酸亚铁溶液的过程中过量硫酸的作用是
(2)请结合所学知识补全流程中缺少的操作步骤。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】铁是人类较早使用的金属之一、运用铁及其化合物的知识,完成下列问题。
(1)所含铁元素既有氧化性又有还原性的物质是____ (填字母代号)。
(2)向沸水中逐滴滴加lmol/LFeCl3溶液,至____ ,该分散系中粒子直径的范围是____ nm。
(3)电子工业需要用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出FeCl3溶液与铜反应的离子方程式:____ 。某校同学为测定FeCl3腐蚀铜后所得溶液的组成,进行了如下实验:首先取少量待测溶液﹐滴入KSCN溶液呈红色,则溶液中含有的金属阳离子是____ ,在此基础上,又进行了定量组成的测定:取50.0mL待测溶液,向其中加入足量的AgNO3溶液,得白色沉淀,____ (填实验操作,下同)、洗涤、干燥,称量沉淀质量为43.05g。则待测溶液中,FeCl3的物质的量浓度为____ 。
(4)若要验证该溶液中含有Fe2+,正确的实验方法是____ (填字母代号)。
A.向试管中加入试液,滴入KSCN溶液,若显红色,证明含有Fe2+
B.向试管中加入试液,滴入酸性高锰酸钾溶液,若褪色,证明含有Fe2+
C.向试管中加入试液,滴入氯水,再滴入KSCN溶液,若显红色,证明原溶液中含有Fe2+
(5)欲从废水中回收铜,并重新获得FeCl3溶液,设计实验方案如图:

A.请写出上述实验中加入或生成的有关物质的化学式:①____ ;②____ ;③____ ;④____ 。
B.请写出通入⑥的化学方程式:_____ 。
(1)所含铁元素既有氧化性又有还原性的物质是
| A.Fe | B.FeCl2 | C.FeSO4 | D.Fe2O3 |
(3)电子工业需要用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出FeCl3溶液与铜反应的离子方程式:
(4)若要验证该溶液中含有Fe2+,正确的实验方法是
A.向试管中加入试液,滴入KSCN溶液,若显红色,证明含有Fe2+
B.向试管中加入试液,滴入酸性高锰酸钾溶液,若褪色,证明含有Fe2+
C.向试管中加入试液,滴入氯水,再滴入KSCN溶液,若显红色,证明原溶液中含有Fe2+
(5)欲从废水中回收铜,并重新获得FeCl3溶液,设计实验方案如图:

A.请写出上述实验中加入或生成的有关物质的化学式:①
B.请写出通入⑥的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】按要求完成下列填空
(1)写出下列物质在水溶液中的电离方程式:
①
___________
②
___________
(2)写出下列反应的化学方程式:
①除去 粉末中混有的少量
粉末中混有的少量 所涉及的反应:
所涉及的反应:___________ ;
②在消防员的呼吸面具中, 与
与 发生的反应:
发生的反应:___________ ;
③将 通入冷的石灰乳中制漂白粉:
通入冷的石灰乳中制漂白粉:___________ ;
④ 在空气中久置变成红褐色:
在空气中久置变成红褐色:___________ 。
(3)写出下列反应的离子方程式:
①钠与水的反应:___________ ;
② 与水的反应:
与水的反应:___________ ;
③除去 溶液中混有的少量
溶液中混有的少量 :
:___________ 。
(1)写出下列物质在水溶液中的电离方程式:
①

②

(2)写出下列反应的化学方程式:
①除去
 粉末中混有的少量
粉末中混有的少量 所涉及的反应:
所涉及的反应:②在消防员的呼吸面具中,
 与
与 发生的反应:
发生的反应:③将
 通入冷的石灰乳中制漂白粉:
通入冷的石灰乳中制漂白粉:④
 在空气中久置变成红褐色:
在空气中久置变成红褐色:(3)写出下列反应的离子方程式:
①钠与水的反应:
②
 与水的反应:
与水的反应:③除去
 溶液中混有的少量
溶液中混有的少量 :
:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】下图是某儿童微量元素体检报告单的部分数据:
大连市医疗机构临床检验结果报告单
根据上表的数据,回答下列问题。
(1)该儿童缺乏___________ 元素。
(2)报告单中“μmol·L-1”是___________ (填“质量”“体积”或“浓度”)的单位。
(3)服用维生素C可使食物中的Fe3+转化为Fe2+,在这个过程中体现维生素C的___________ (填“氧化性”或“还原性”)。
(4)缺铁性贫血患者应补充Fe2+,一些补铁剂以硫酸亚铁为主要成分,将硫酸亚铁制成药片时外表包有一层特殊的糖衣,推测糖衣的主要作用是___________ 。
(5)关于铁的氢氧化物有两种,请写出氢氧化亚铁在空气中被氧化成氢氧化铁的实验现象___________ ,对应化学反应方程式为___________
大连市医疗机构临床检验结果报告单
| 分析项目 | 检测结果 | 单位 | 参考范围 | |
| 1 | 锌(Zn) | 115.92 | μmol·L-1 | 66~120 |
| 2 | 铁(Fe) | 6.95↓ | mmol·L-1 | 7.52~11.82 |
| 4 | 钙(Ca) | 1.68 | mmol·L-1 | 1.55~2.10 |
| … | … | … | … | … |
根据上表的数据,回答下列问题。
(1)该儿童缺乏
(2)报告单中“μmol·L-1”是
(3)服用维生素C可使食物中的Fe3+转化为Fe2+,在这个过程中体现维生素C的
(4)缺铁性贫血患者应补充Fe2+,一些补铁剂以硫酸亚铁为主要成分,将硫酸亚铁制成药片时外表包有一层特殊的糖衣,推测糖衣的主要作用是
(5)关于铁的氢氧化物有两种,请写出氢氧化亚铁在空气中被氧化成氢氧化铁的实验现象
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】“价类”二维图是学习元素及其化合物的重要工具,如图所示是铁及其化合物的“价类”二维图。
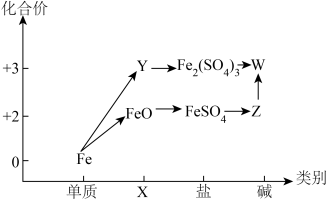
(1)X、Y分别代表_______ 、_______ ;Z在空气中转化为W的化学方程式为_______ 。
(2)某小组研究 性质,预测
性质,预测 能与
能与_______ 发生氧化还原反应(填序号)。
①NaOH溶液②氯水③稀盐酸④酸性 溶液⑤镁⑥碳酸钠
溶液⑤镁⑥碳酸钠
(3)往FeBr2溶液中通入一定量氯气,已知n(FeBr2)∶n(Cl2)=1,写出该反应的离子方程式_______ 。
(4)为检验食品中的铁元素,可将菠菜剪碎、研磨、溶解、_______ ,然后将少许滤液加入试管中,加入少量稀硝酸(稀硝酸具有氧化性),再滴加几滴KSCN溶液,振荡,若观察到_______ 现象,说明试验样品中含有铁元素。
(5)高铁酸钠是一种能杀菌、脱色、除臭的新型高效水处理剂。工业上可用 氧化
氧化 的方法制备
的方法制备 ,其原理为
,其原理为 ,用双线桥法表示该反应的电子转移方向和数目
,用双线桥法表示该反应的电子转移方向和数目_______ 。

(1)X、Y分别代表
(2)某小组研究
 性质,预测
性质,预测 能与
能与①NaOH溶液②氯水③稀盐酸④酸性
 溶液⑤镁⑥碳酸钠
溶液⑤镁⑥碳酸钠(3)往FeBr2溶液中通入一定量氯气,已知n(FeBr2)∶n(Cl2)=1,写出该反应的离子方程式
(4)为检验食品中的铁元素,可将菠菜剪碎、研磨、溶解、
(5)高铁酸钠是一种能杀菌、脱色、除臭的新型高效水处理剂。工业上可用
 氧化
氧化 的方法制备
的方法制备 ,其原理为
,其原理为 ,用双线桥法表示该反应的电子转移方向和数目
,用双线桥法表示该反应的电子转移方向和数目
您最近一年使用:0次



