完成下列问题。
Ⅰ.电负性的概念是由美国化学家鲍林提出的,用来描述不同元素的原子对键合电子吸引力的大小,可用一定数值x来表示。下面是某些短周期元素的x值:
(1)通过分析x值变化规律,确定Mg的x值范围:___________<x(Mg)<___________。___________
(2)指出下列两种化合物中氧元素的化合价:HClO___________ ,HFO___________ 。有机物结构式为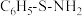 ,其中S-N中,共用电子对偏向
,其中S-N中,共用电子对偏向___________ 。
(3)成键的两原子相应元素x数值的差值为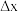 ,当
,当 时,一般为离子键,
时,一般为离子键, 时,一般为共价键,则
时,一般为共价键,则 中化学键类型是
中化学键类型是___________ 。
(4)预测元素周期表中,x值最小的元素位于___________ 周期___________ 族(放射性元素除外)。
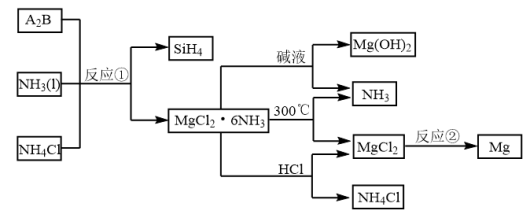
Ⅱ.下图中反应①是制备 的一种方法,其副产物是优质的镁资源。
的一种方法,其副产物是优质的镁资源。
(5)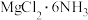 中所含元素的简单离子半径由小到大的顺序(氢元素的简单离子只考虑H+):
中所含元素的简单离子半径由小到大的顺序(氢元素的简单离子只考虑H+):___________ 。
(6)A2B的化学式为___________ 。上图中可以循环使用的物质有___________ (化学式)。
(7)一定条件下,由SiH4和CH4反应生成H2和一种固体耐磨材料___________ 。
(8)为实现燃煤脱硫,煤中加入浆状 ,使燃烧产生的
,使燃烧产生的 转化为稳定的镁化合物。该反应的化学方程式:
转化为稳定的镁化合物。该反应的化学方程式:___________ 。
Ⅰ.电负性的概念是由美国化学家鲍林提出的,用来描述不同元素的原子对键合电子吸引力的大小,可用一定数值x来表示。下面是某些短周期元素的x值:
| 元素 | Li | Be | B | C | N | O | F | Na | Al | Si | P | S | Cl |
| x值 | 0.98 | 1.57 | 2.04 | 2.55 | 3.0 | 3.44 | 3.98 | 0.93 | 1.61 | 1.90 | 2.19 | 2.58 | 3.16 |
(2)指出下列两种化合物中氧元素的化合价:HClO
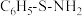 ,其中S-N中,共用电子对偏向
,其中S-N中,共用电子对偏向(3)成键的两原子相应元素x数值的差值为
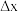 ,当
,当 时,一般为离子键,
时,一般为离子键, 时,一般为共价键,则
时,一般为共价键,则 中化学键类型是
中化学键类型是(4)预测元素周期表中,x值最小的元素位于
Ⅱ.下图中反应①是制备
 的一种方法,其副产物是优质的镁资源。
的一种方法,其副产物是优质的镁资源。
(5)
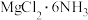 中所含元素的简单离子半径由小到大的顺序(氢元素的简单离子只考虑H+):
中所含元素的简单离子半径由小到大的顺序(氢元素的简单离子只考虑H+):(6)A2B的化学式为
(7)一定条件下,由SiH4和CH4反应生成H2和一种固体耐磨材料
(8)为实现燃煤脱硫,煤中加入浆状
 ,使燃烧产生的
,使燃烧产生的 转化为稳定的镁化合物。该反应的化学方程式:
转化为稳定的镁化合物。该反应的化学方程式:
更新时间:2021-11-20 08:55:03
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】如图中的每一方框内表示一种反应物或生成物,其中A、C、D、E、F 在通常情况下均为气体,且A 与 C 物质的量之比为 1:1,B 为常见液体,F 为红棕色气体。
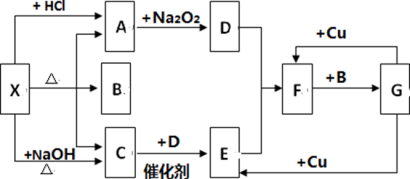
试回答下列问题:
(1)X 是_____ ;F 是_____ 。(写化学式)
(2)写出 G→E 反应的化学方程式并用双线桥标出电子转移的方向和数目_________ 。
(3)G 与 Cu 的反应中,G 表现__________ 性质。
(4)写出X→A 的离子方程式:__________ 。
(5)以 C、B、D 为原料可生产 G,若使 amolC 的中心原子完全转化到 G 中,理论上至少需要 D______ mol。

试回答下列问题:
(1)X 是
(2)写出 G→E 反应的化学方程式并用双线桥标出电子转移的方向和数目
(3)G 与 Cu 的反应中,G 表现
(4)写出X→A 的离子方程式:
(5)以 C、B、D 为原料可生产 G,若使 amolC 的中心原子完全转化到 G 中,理论上至少需要 D
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】常温下,A是可用来对自来水进行消毒的黄绿色单质气体,A、B、C、D、E 都含X元素,其转化关系如下图所示。
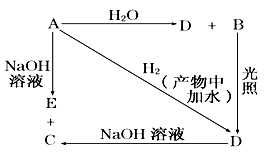
(1)请分别写出A、B、C、D、E的化学式(如为溶液请填溶质的化学式):
A_____ ,B _____ ,C ______ ,D_____ ,E___________ 。
(2)写出下列反应的化学方程式:
A+H2O:______________ ;
A+NaOH:______________________ 。

(1)请分别写出A、B、C、D、E的化学式(如为溶液请填溶质的化学式):
A
(2)写出下列反应的化学方程式:
A+H2O:
A+NaOH:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】化学学习和研究离不开元素周期表。下图为元素周期表的一部分,根据表中给出的7种元素,回答下列问题:

(1) 元素的原子结构示意图是
元素的原子结构示意图是______ , 元素在元素周期表中的位置是
元素在元素周期表中的位置是______ 。
(2) 、
、 、
、 三种元素的原子半径从大到小的顺序是
三种元素的原子半径从大到小的顺序是______ (填元素符号)。
(3) 、
、 的简单氢化物中,稳定性较强的是
的简单氢化物中,稳定性较强的是______ (填化学式)。
(4) 的最高价氧化物对应的水化物与
的最高价氧化物对应的水化物与 溶液反应的离子方程式是
溶液反应的离子方程式是______ 。
(5) 的简单氢化物属于
的简单氢化物属于______ (填“离子化合物”或“共价化合物”),其所含的化学键是______ (填“离子键”或“共价键”)。
(6)下列事实不能 用来判断 和
和 非金属性强弱的是
非金属性强弱的是______ (填序号)。
a. 、
、 的单质与铁反应分别生成
的单质与铁反应分别生成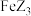 、
、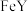
b. 能从
能从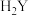 中置换出
中置换出 单质
单质
c.相同温度下,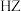 的溶解度比
的溶解度比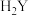 的大
的大

(1)
 元素的原子结构示意图是
元素的原子结构示意图是 元素在元素周期表中的位置是
元素在元素周期表中的位置是(2)
 、
、 、
、 三种元素的原子半径从大到小的顺序是
三种元素的原子半径从大到小的顺序是(3)
 、
、 的简单氢化物中,稳定性较强的是
的简单氢化物中,稳定性较强的是(4)
 的最高价氧化物对应的水化物与
的最高价氧化物对应的水化物与 溶液反应的离子方程式是
溶液反应的离子方程式是(5)
 的简单氢化物属于
的简单氢化物属于(6)下列事实
 和
和 非金属性强弱的是
非金属性强弱的是a.
 、
、 的单质与铁反应分别生成
的单质与铁反应分别生成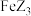 、
、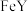
b.
 能从
能从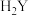 中置换出
中置换出 单质
单质c.相同温度下,
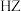 的溶解度比
的溶解度比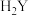 的大
的大
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】如图是元素周期表的一部分,填写下列空格:
(1)比较④⑤⑧的原子半径由大到小依次___________ 。(填元素符号,下同)
(2)元素②与④形成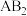 型化合物的电子式为
型化合物的电子式为___________ ,属于___________ 晶体。
(3)③的气态氢化物与⑨的气态氢化物反应的化学反应方程式:___________ ,所得产物中含有的化学键类型有___________ 。
(4)⑥、⑦最高价氧化物对应的水化物碱性较强的是___________ 。(填化学式)
| ① | |||||||||||||||||
| ② | ③ | ④ | ⑤ | ||||||||||||||
| ⑥ | ⑦ | ⑧ | ⑨ | ||||||||||||||
(2)元素②与④形成
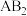 型化合物的电子式为
型化合物的电子式为(3)③的气态氢化物与⑨的气态氢化物反应的化学反应方程式:
(4)⑥、⑦最高价氧化物对应的水化物碱性较强的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题:

(1)在此元素周期表的一部分中,金属性最强的元素是___________ (填元素符号)。
(2)⑤、⑥的原子半径由大到小的顺序为___________ (填元素符号)。
(3)⑦、⑧两种元素的氢化物稳定性较强的是___________ (用化学式表示)。
(4)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的化学式:___________ 。

(1)在此元素周期表的一部分中,金属性最强的元素是
(2)⑤、⑥的原子半径由大到小的顺序为
(3)⑦、⑧两种元素的氢化物稳定性较强的是
(4)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的化学式:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】硅和卤素单质反应可以得到SiX4。
SX4的熔沸点
①0℃时,SiF4、SiCl4、SiBr4、SiI4呈液态的是___________ (填化学式),沸点依次升高的原因是___________ ,气态SiX4分子的空间构型是___________ ;
②SiCl4与N﹣甲基咪唑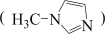 反应可以得到M2+,其结构如图所示:
反应可以得到M2+,其结构如图所示:
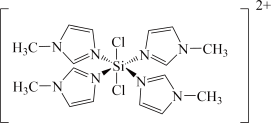
N-甲基咪唑分子中碳原子的杂化轨道类型为___________ ,H、C、N的电负性由大到小的顺序为___________ ,1个M2+中含有___________ 个σ键;
SX4的熔沸点
| SiF4 | SiCl4 | SiBr4 | SiI4 | |
| 熔点/K | 183.0 | 203.2 | 278.6 | 393.7 |
| 沸点/K | 187.2 | 330.8 | 427.2 | 560.7 |
②SiCl4与N﹣甲基咪唑
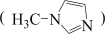 反应可以得到M2+,其结构如图所示:
反应可以得到M2+,其结构如图所示:
N-甲基咪唑分子中碳原子的杂化轨道类型为
您最近一年使用:0次
【推荐2】元素的性质在元素周期表中按其排列呈现一定的规律。下表为元素周期表中部分元素,根据要求回答下列问题:
(1)在以上元素的基态原子的电子排布中4s轨道上只有1个电子的元素有_________ (填元素名称)。
(2)根据元素原子的外围电子排布的特征,可将元素周期表分成五个区域:s区、p区、d区、ds区和f区,以上12种元素分别属于s区、d区、ds区和p区,则属于s区的元素有________ 种,属于d区的元素有______ 种。
(3)CaO晶胞如图所示,CaO晶体中Ca2+的配位数为______ ;与每一个钙离子距离最近并且距离相等的钙离子有____ 个;CaO晶体和NaCl晶体的晶格能分别为:CaO:3 401 kJ/mol、NaCl:786 kJ/mol。导致两者晶格能差异的主要原因_______________ 。

(4)由叠氮酸钠(NaN3)热分解可得光谱纯N2:2NaN3(s)===2Na(l)+3N2(g),下列有关说法正确的是____ (选填序号)。
A.NaN3与KN3结构类似,前者晶格能较小
B.金属钠的晶胞结构如图所示,每个晶胞平均分摊2个钠原子

C.氮的第一电离能大于氧
D.氮气常温下很稳定,是因为氮的电负性小
| K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge |
(1)在以上元素的基态原子的电子排布中4s轨道上只有1个电子的元素有
(2)根据元素原子的外围电子排布的特征,可将元素周期表分成五个区域:s区、p区、d区、ds区和f区,以上12种元素分别属于s区、d区、ds区和p区,则属于s区的元素有
(3)CaO晶胞如图所示,CaO晶体中Ca2+的配位数为

(4)由叠氮酸钠(NaN3)热分解可得光谱纯N2:2NaN3(s)===2Na(l)+3N2(g),下列有关说法正确的是
A.NaN3与KN3结构类似,前者晶格能较小
B.金属钠的晶胞结构如图所示,每个晶胞平均分摊2个钠原子

C.氮的第一电离能大于氧
D.氮气常温下很稳定,是因为氮的电负性小
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】化合物M由两种短周期主族元素组成,在一定条件下可以发生下列转化:
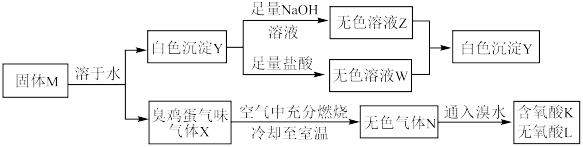
请回答下列问题:
(1)固体M的化学式为___________ 。
(2)无氧酸L中阴离子对应元素在元素周期表中的位置为___________ ,其基态原子中电子的空间运动状态有___________ 种。
(3)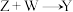 的化学方程式为
的化学方程式为___________ 。
(4)上述流程的反应中涉及的短周期非金属元素的电负性由大到小的顺序为___________ 。
(5)如图所示,在室温下向甲、乙两相同密闭容器中,分别充入等物质的量气体X和气体N。
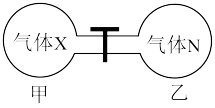
①反应前两容器中的气体密度: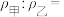
___________ 。
②打开活塞,使气体充分反应,则反应前后的压强: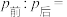
___________ 。
(6)将无色气体N通入到浓硝酸中,有红棕色气体冒出,在反应中n(氧化剂):n(还原剂)=___________ 。

请回答下列问题:
(1)固体M的化学式为
(2)无氧酸L中阴离子对应元素在元素周期表中的位置为
(3)
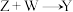 的化学方程式为
的化学方程式为(4)上述流程的反应中涉及的短周期非金属元素的电负性由大到小的顺序为
(5)如图所示,在室温下向甲、乙两相同密闭容器中,分别充入等物质的量气体X和气体N。

①反应前两容器中的气体密度:
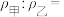
②打开活塞,使气体充分反应,则反应前后的压强:
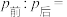
(6)将无色气体N通入到浓硝酸中,有红棕色气体冒出,在反应中n(氧化剂):n(还原剂)=
您最近一年使用:0次

 B
B D。
D。

