研究电解质在水溶液中的平衡能了解它的存在形式。
(1)已知部分弱酸的电离常数如下表:
①写出 的
的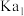 的表达式
的表达式_______ 。
② 、
、 、
、 三种酸的酸性由强到弱的顺序是
三种酸的酸性由强到弱的顺序是_______ 。
③将过量 通入
通入 溶液,反应的离子方程式是
溶液,反应的离子方程式是_______ 。
(2)二元弱酸 溶液中
溶液中 的物质的量分数
的物质的量分数 随
随 的变化如图所示。则
的变化如图所示。则 第二级电离平衡常数
第二级电离平衡常数
_______ 。
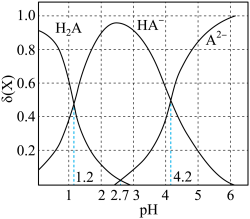
(3)已知25℃,NH3·H2O的Kb=1.8×10-5,H2SO3的Ka1=1.3×10-2,Ka2=6.2×10-8,若氨水的浓度为2.0 mol·L-1,溶液中的c(OH−)=_______ mol·L−1。将SO2通入该氨水中,当c(OH−)降至1.0×10−7mol·L−1时,溶液中的 =
=_______ 。
(1)已知部分弱酸的电离常数如下表:
| 化学式 |  |  |  |
电离平衡常数Ka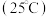 | 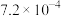 |  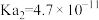 | 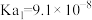  |
 的
的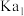 的表达式
的表达式②
 、
、 、
、 三种酸的酸性由强到弱的顺序是
三种酸的酸性由强到弱的顺序是③将过量
 通入
通入 溶液,反应的离子方程式是
溶液,反应的离子方程式是(2)二元弱酸
 溶液中
溶液中 的物质的量分数
的物质的量分数 随
随 的变化如图所示。则
的变化如图所示。则 第二级电离平衡常数
第二级电离平衡常数

(3)已知25℃,NH3·H2O的Kb=1.8×10-5,H2SO3的Ka1=1.3×10-2,Ka2=6.2×10-8,若氨水的浓度为2.0 mol·L-1,溶液中的c(OH−)=
 =
=
更新时间:2021-11-20 11:21:33
|
【知识点】 弱电解质的电离平衡
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】I、电解质在水溶液中的行为影响了电解质溶液的性质(以下讨论均在常温时)。
(1)0.1
 溶液的pH=3
溶液的pH=3
① 的电离度
的电离度___________ (用百分比表示)。
②该溶液中由水电离出的 浓度是
浓度是___________  。
。
③计算 的电离平衡常数
的电离平衡常数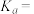
___________ 。
Ⅱ、某铬盐厂净化含Cr(VI)废水并提取Cr2O3的一种工艺流程如图所示。

已知:Ksp[Cr(OH)3]=6.0×10-29
(2)步骤I中,发生的反应为2H++2

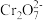 +H2O,随着酸的浓度增大B中
+H2O,随着酸的浓度增大B中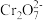 的浓度会
的浓度会___________ (“增大”或“减小”)。
(3)当清液中Cr3+的浓度6×10-5mol·L-1时,可认为已达铬的排放标准。此时清液的pH=___________ 。
(4)已知NaHSO3溶液显酸性,则溶液中c(H2SO3)___________ c( )浓度大小关系为(填“>”“<”)
)浓度大小关系为(填“>”“<”)
(1)0.1

 溶液的pH=3
溶液的pH=3①
 的电离度
的电离度②该溶液中由水电离出的
 浓度是
浓度是 。
。③计算
 的电离平衡常数
的电离平衡常数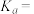
Ⅱ、某铬盐厂净化含Cr(VI)废水并提取Cr2O3的一种工艺流程如图所示。

已知:Ksp[Cr(OH)3]=6.0×10-29
(2)步骤I中,发生的反应为2H++2


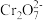 +H2O,随着酸的浓度增大B中
+H2O,随着酸的浓度增大B中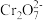 的浓度会
的浓度会(3)当清液中Cr3+的浓度6×10-5mol·L-1时,可认为已达铬的排放标准。此时清液的pH=
(4)已知NaHSO3溶液显酸性,则溶液中c(H2SO3)
 )浓度大小关系为(填“>”“<”)
)浓度大小关系为(填“>”“<”)
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】已知:草酸H2C2O4的Ka1=5.0×10-2, Ka2=5.4×10-5; Ksp(CaC2O4)=4.8×10-8
(1)在此溶液中逐滴滴加0.2mol/L的NaOH溶液,n( )的变化趋势是
)的变化趋势是_________________ 。
(2)用Ka1 、 Ka2、Kw 表示对应的K
① +2H+ =H2C2O4 K=
+2H+ =H2C2O4 K=____________ ② +OH- =
+OH- = +H2O K=
+H2O K=____________
③H2C2O4+ =2
=2 K=
K=____________
(3)0.1mol/L的Na2C2O4溶液100mL,该溶液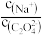
______ 2(填“>”、“<”或“=”,下同),向此溶液中加入草酸(H2C2O4)固体至pH=7,溶液中c( )
)_______ c( )。
)。
(4)在某温度下向含有草酸钙(CaC2O4)固体的CaC2O4饱和溶液中加入少量草酸(H2C2O4)固体,则CaC2O4的溶解量________ (填“增大”、“减小”或“不变”,下同),Ksp(CaC2O4)__________ ,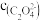
__________ 。
(5)将0.2mol/L的H2C2O4溶液与0.2mol/L的CaCl2溶液等体积混合,通过计算说明溶液中是否有沉淀生成_______ 。
(1)在此溶液中逐滴滴加0.2mol/L的NaOH溶液,n(
 )的变化趋势是
)的变化趋势是(2)用Ka1 、 Ka2、Kw 表示对应的K
①
 +2H+ =H2C2O4 K=
+2H+ =H2C2O4 K= +OH- =
+OH- = +H2O K=
+H2O K=③H2C2O4+
 =2
=2 K=
K=(3)0.1mol/L的Na2C2O4溶液100mL,该溶液
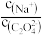
 )
) )。
)。(4)在某温度下向含有草酸钙(CaC2O4)固体的CaC2O4饱和溶液中加入少量草酸(H2C2O4)固体,则CaC2O4的溶解量
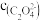
(5)将0.2mol/L的H2C2O4溶液与0.2mol/L的CaCl2溶液等体积混合,通过计算说明溶液中是否有沉淀生成
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】运用化学反应原理,研究硫、磷化合物的反应具有重要意义。
(1)已知H3PO2(次磷酸)的水溶液中存在 H3PO2分子。H3PO2与足量 NaOH溶液充分反应,消耗的酸和碱的物质的量相等,则生成盐的化学式为___________ ,该盐属于___________ (填"正盐"或"酸式盐")。H3PO2易被氧化为 H3PO4,已知常温下H3PO4的电离常数为 ,请利用以上数据计算推测 Na2HPO4溶液的酸碱性
,请利用以上数据计算推测 Na2HPO4溶液的酸碱性___________ 。(填“酸性”、“碱性”或“中性”)
(2)常温下,用NaOH溶液吸收 SO2得到 pH=9的Na2SO3溶液,吸收过程中水的电离衡___________ (填"向左"、"向右"或"不")移动。试计算该溶液中
___________ 。(常温下 H2SO3的电离平衡常数 )
)
(3)NaHSO3溶液的pH<7,NaHCO3溶液的pH>7,则NaHSO3溶液中c(H2SO3)___________ (填“>”“<”或“=”,下同)c( ),NaHCO3溶液中c(H2CO3)
),NaHCO3溶液中c(H2CO3)___________ c( )。
)。
(4)化工生产中常用 FeS作沉淀剂除去工业废水中的Cu2+,其反应原理为Cu2+(aq)+FeS(s)⇌CuS(s)+Fe2+(aq)。下列有关叙述正确的是___________ 。
a.
b.达到平衡时c(Fe2+)=c(Cu2+)
c.溶液中加入少量 Na2S固体后,溶液中c(Fe2+)、c(Cu2+)都减小
d. 该反应平衡常数
(1)已知H3PO2(次磷酸)的水溶液中存在 H3PO2分子。H3PO2与足量 NaOH溶液充分反应,消耗的酸和碱的物质的量相等,则生成盐的化学式为
 ,请利用以上数据计算推测 Na2HPO4溶液的酸碱性
,请利用以上数据计算推测 Na2HPO4溶液的酸碱性(2)常温下,用NaOH溶液吸收 SO2得到 pH=9的Na2SO3溶液,吸收过程中水的电离衡

 )
)(3)NaHSO3溶液的pH<7,NaHCO3溶液的pH>7,则NaHSO3溶液中c(H2SO3)
 ),NaHCO3溶液中c(H2CO3)
),NaHCO3溶液中c(H2CO3) )。
)。(4)化工生产中常用 FeS作沉淀剂除去工业废水中的Cu2+,其反应原理为Cu2+(aq)+FeS(s)⇌CuS(s)+Fe2+(aq)。下列有关叙述正确的是
a.

b.达到平衡时c(Fe2+)=c(Cu2+)
c.溶液中加入少量 Na2S固体后,溶液中c(Fe2+)、c(Cu2+)都减小
d. 该反应平衡常数

您最近一年使用:0次



