向稀氨水中分别加入下列物质,请判断电离平衡移动的方向。
加入的物质 |
| NH3 | NaOH |
电离平衡移动的方向 |
更新时间:2021-12-01 23:57:53
|
相似题推荐
填空题
|
容易
(0.94)
【推荐1】电离平衡常数的影响因素
电离平衡常数K 值只与电解质____________ 和______ 有关,与浓度______ 。
由于电离是______ 的,所以电离平衡常数随着温度的升高而______ 。
电离平衡常数K 值只与电解质
由于电离是
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐2】在滴有酚酞的氨水中加入NH4Cl溶液后红色变浅,解释:______ 。
您最近一年使用:0次
填空题
|
容易
(0.94)
名校
【推荐3】电解质溶液中存在多种平衡。请回答下列问题:
(1)已知:
物质的量浓度均为0.1mol/L的下列溶液:a. CH3COOH b. HClO ,比较二者C(H+)的大小:a______ b(填“>”、“<”或“=”)。
(2)常温下,将 0.1mol/L 的 CH3COOH 溶液加水稀释,在稀释过程中,下列表达式的数值变大的__________ (填字母)。
A. c(H+) B. C. c(H+)·c(OH-)
C. c(H+)·c(OH-)
(3)25℃时,体积均为 10mL,pH 均为 2 的醋酸溶液与一元酸 HX 溶液分别加水稀释至 1000mL,稀释过程中 pH 的变化如图所示。已知:pH= -lgC(H+),则:
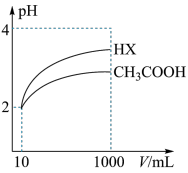
①25℃时,醋酸的电离常数________ HX的电离常数。(填“>”、“<”或“=”)
②稀释100倍后, 醋酸溶液中由水电离出的 c(H+)________ HX溶液中由水电离出的c(H+)。(填“>”、“<”或“=”)
(1)已知:
| 化学式 | CH3COOH | HClO |
| 电离常数(25℃) | 1.8×10-5 | 3.0×10-8 |
物质的量浓度均为0.1mol/L的下列溶液:a. CH3COOH b. HClO ,比较二者C(H+)的大小:a
(2)常温下,将 0.1mol/L 的 CH3COOH 溶液加水稀释,在稀释过程中,下列表达式的数值变大的
A. c(H+) B.
 C. c(H+)·c(OH-)
C. c(H+)·c(OH-) (3)25℃时,体积均为 10mL,pH 均为 2 的醋酸溶液与一元酸 HX 溶液分别加水稀释至 1000mL,稀释过程中 pH 的变化如图所示。已知:pH= -lgC(H+),则:

①25℃时,醋酸的电离常数
②稀释100倍后, 醋酸溶液中由水电离出的 c(H+)
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐1】用 醋酸溶液进行导电性实验,发现灯泡亮度很低;用
醋酸溶液进行导电性实验,发现灯泡亮度很低;用 氨水进行导电性实验,发现灯泡亮度同样很低。但若将两种溶液等体积混合再进行导电性实验,灯泡亮度却显著增加。请分析其中的原因。
氨水进行导电性实验,发现灯泡亮度同样很低。但若将两种溶液等体积混合再进行导电性实验,灯泡亮度却显著增加。请分析其中的原因。_________
 醋酸溶液进行导电性实验,发现灯泡亮度很低;用
醋酸溶液进行导电性实验,发现灯泡亮度很低;用 氨水进行导电性实验,发现灯泡亮度同样很低。但若将两种溶液等体积混合再进行导电性实验,灯泡亮度却显著增加。请分析其中的原因。
氨水进行导电性实验,发现灯泡亮度同样很低。但若将两种溶液等体积混合再进行导电性实验,灯泡亮度却显著增加。请分析其中的原因。
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐2】电离平衡常数的意义
电离平衡常数越大,表示该弱电解质电离程度______ ,弱酸的酸性______ ,弱碱的碱性______ 。
电离平衡常数越大,表示该弱电解质电离程度
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐1】在一定温度下,冰醋酸加水稀释过程中溶液的导电能力如下图所示,请回答:
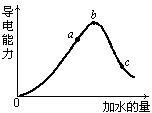
(1)写出醋酸的电离方程式_______________________________________ 。
(2)a、b、c三点溶液中氢离子浓度由小到大的顺序为________________ 。
(3)a、b、c三点中醋酸的电离程度最大的是________ 。
(4)取甲、乙两份等体积c点的溶液,甲用蒸馏水稀释10倍,,乙用蒸馏水稀释100倍,则稀释后甲、乙两溶液中的H+浓度:C(H+)甲__ 10C(H+)乙(填“大于”、“小于”或 “等于”)甲,其原因是:_______________________ 。

(1)写出醋酸的电离方程式
(2)a、b、c三点溶液中氢离子浓度由小到大的顺序为
(3)a、b、c三点中醋酸的电离程度最大的是
(4)取甲、乙两份等体积c点的溶液,甲用蒸馏水稀释10倍,,乙用蒸馏水稀释100倍,则稀释后甲、乙两溶液中的H+浓度:C(H+)甲
您最近一年使用:0次
填空题
|
容易
(0.94)
解题方法
【推荐2】某学生在实验室测某稀硫酸溶液的pH时,他先用蒸馏水润湿pH试纸,然后用洁净干燥的玻璃棒蘸取试样进行检测。
(1)该学生的操作是__________ (填“正确的”或“错误的”),理由是__________ 。
(2)若用此方法分别测定c(H+)相等的盐酸和醋酸溶液的pH,误差较大的是__________ 。
(3)该学生用此方法测定下列溶液的pH,其中测定结果无误差的是________ (填序号)
(1)该学生的操作是
(2)若用此方法分别测定c(H+)相等的盐酸和醋酸溶液的pH,误差较大的是
(3)该学生用此方法测定下列溶液的pH,其中测定结果无误差的是
A.NaOH溶液 B.CH3COONa溶液 C.NaCl溶液 D.NaHSO4溶液
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐3】判断下列叙述的正误(用正确或错误表示)。
1.电负性的大小可以作为判断元素非金属性强弱的依据。(_______)
2.催化剂可以加快化学反应的速率,也可以提高反应物的转化率。(_______)
3.比较电离常数的大小可以判断弱电解质的相对强弱。(_______)
4.常温下,加水稀释醋酸溶液的过程中,醋酸的电离程度增大。(_______)
5.在一定条件下,化学反应的△H只与反应体系的始态和终态有关,而与反应的途径无关。(_______)
1.电负性的大小可以作为判断元素非金属性强弱的依据。(_______)
2.催化剂可以加快化学反应的速率,也可以提高反应物的转化率。(_______)
3.比较电离常数的大小可以判断弱电解质的相对强弱。(_______)
4.常温下,加水稀释醋酸溶液的过程中,醋酸的电离程度增大。(_______)
5.在一定条件下,化学反应的△H只与反应体系的始态和终态有关,而与反应的途径无关。(_______)
您最近一年使用:0次




