Zn与S形成某种化合物的晶胞如图所示。
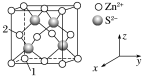
(1)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。例如图中原子1的坐标为(0,0,0),则原子2的坐标为__ 。
(2)已知晶体密度为dg·cm-3,S2-半径为apm,若要使S2-、Zn2+相切,则Zn2+半径为__ pm(写计算表达式)。

(1)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。例如图中原子1的坐标为(0,0,0),则原子2的坐标为
(2)已知晶体密度为dg·cm-3,S2-半径为apm,若要使S2-、Zn2+相切,则Zn2+半径为
2021高三·全国·专题练习 查看更多[1]
(已下线)专题讲座(十一)晶胞参数、坐标参数的分析与应用(练) — 2022年高考化学一轮复习讲练测(新教材新高考)
更新时间:2021-12-07 08:38:06
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】完成下列问题
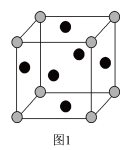
(1)铜银合金是优质的金属材料,其晶胞与铜晶胞类似,其中Ag位于顶角,Cu位于面心,如图1所示。
①该铜银合金的化学式是___________
②已知该铜银晶胞的参数为a cm、晶体密度为ρ g·cm-3,则阿伏加德罗常数(NA)为___________ mol-1(用代数式表示,下同)
③若Ag、Cu的原子半径分别为bcm、ccm,则该晶胞中原子空间利用率φ=___________
(2)ZnF2具有金红石型四方结构,KZnF3具有钙钛矿型立方结构,两种晶体的晶胞结构如图2所示:

①ZnF2和KZnF3晶体(晶胞顶角为K+)中,Zn2+的配位数之比为___________ 。
②若NA表示阿伏加德罗常数的值,则ZnF2晶体的密度为___________ g·cm-3(用含a、c、NA的代数式表示)。
③KZnF3晶胞中A离子的坐标参数为(0,0,0),B离子的坐标参数为(1,0,0),C离子的坐标参数为(0,1,0),则D离子的坐标参数为___________
(1)铜银合金是优质的金属材料,其晶胞与铜晶胞类似,其中Ag位于顶角,Cu位于面心,如图1所示。

①该铜银合金的化学式是
②已知该铜银晶胞的参数为a cm、晶体密度为ρ g·cm-3,则阿伏加德罗常数(NA)为
③若Ag、Cu的原子半径分别为bcm、ccm,则该晶胞中原子空间利用率φ=
(2)ZnF2具有金红石型四方结构,KZnF3具有钙钛矿型立方结构,两种晶体的晶胞结构如图2所示:

①ZnF2和KZnF3晶体(晶胞顶角为K+)中,Zn2+的配位数之比为
②若NA表示阿伏加德罗常数的值,则ZnF2晶体的密度为
③KZnF3晶胞中A离子的坐标参数为(0,0,0),B离子的坐标参数为(1,0,0),C离子的坐标参数为(0,1,0),则D离子的坐标参数为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】碳化钨是耐高温耐磨材料。下图为碳化钨晶体的部分结构,碳原子嵌入金属的晶格间隙,并不破坏原有金属的晶格,形成填隙化合物。
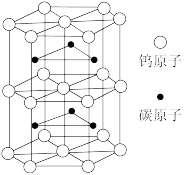
(1)在该结构中,每个钨原子周围距离钨原子最近且等距离的碳原子有___________ 个。
(2)假设该部分晶体的体积为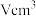 ,碳化钨的摩尔质量为
,碳化钨的摩尔质量为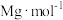 ,密度为
,密度为 ,则阿伏加德罗常数
,则阿伏加德罗常数 用上述数据表示为
用上述数据表示为___________ 。

(1)在该结构中,每个钨原子周围距离钨原子最近且等距离的碳原子有
(2)假设该部分晶体的体积为
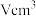 ,碳化钨的摩尔质量为
,碳化钨的摩尔质量为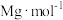 ,密度为
,密度为 ,则阿伏加德罗常数
,则阿伏加德罗常数 用上述数据表示为
用上述数据表示为
您最近一年使用:0次
【推荐1】某硅酸盐研究所在硅酸盐材料和闪烁晶体等领域研究上取得了重大的成就。
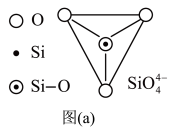
(1)[SiO4]4-是构成硅酸盐的基本结构单元,通过共用氧相连可形成硅氧组群。
①基态硅原子价电子的轨道表示式是_____________ 。
②与[SiO4]4-互为等电子体的微粒符号是_____________ 任写一种)。
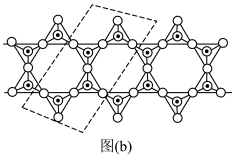
③下图为一种硅氧组群的结构示意图,其离子符号为_____________ ,其中Si原子的杂化方式为_____________ 。
④电负性:Si______ O(填“>”、 “=”或“<” )。
(2)钨酸铅(PWO)是一种闪烁晶体,晶胞结构如图所示。
PWO中钨酸根结构式为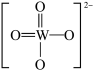 ,该离子中,σ键和π键的个数比是
,该离子中,σ键和π键的个数比是_____________ 。
②PWO晶体中含有的微粒间作用力是___________________
A.范德华力 B.离子键 C.共价键 D.金属键
③已知PWO的摩尔质量为Mg·mol-1,则该晶体的密度d=_____________ g·cm-3。
(1)[SiO4]4-是构成硅酸盐的基本结构单元,通过共用氧相连可形成硅氧组群。
①基态硅原子价电子的轨道表示式是
②与[SiO4]4-互为等电子体的微粒符号是
③下图为一种硅氧组群的结构示意图,其离子符号为

④电负性:Si
(2)钨酸铅(PWO)是一种闪烁晶体,晶胞结构如图所示。
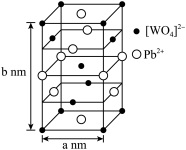
PWO中钨酸根结构式为
 ,该离子中,σ键和π键的个数比是
,该离子中,σ键和π键的个数比是②PWO晶体中含有的微粒间作用力是
A.范德华力 B.离子键 C.共价键 D.金属键
③已知PWO的摩尔质量为Mg·mol-1,则该晶体的密度d=
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】硼及其化合物在工农业生产中应用广泛。
(1)基态硼原子的核外电子排布式为__________ ,有_______ 种不同能量的电子。
(2)BF3溶于水后.在一定条件下可转化为H3O+·[B(OH)F3]-,该物质中阳离子的空间构型为_____________ ,阴离子的中心原子轨道采用________ 杂化。
(3)与BH 互为等电子体的分子是
互为等电子体的分子是_______________ (写化学式)。
(4)EminBF4的熔点为12 ℃,在常温下为液体,由有机物阳离子[Emin]+和[BF4]-构成。该物质的晶体属于_________ 晶体。
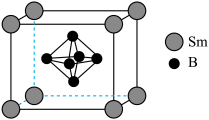
(5)一种由硼和钐(Sm)形成的晶体的晶胞结构如图所示,已知晶胞常数a=n pm,则晶体的密度为_____________ g·cm-3(设NA为阿伏伽德罗常数的值)。
(1)基态硼原子的核外电子排布式为
(2)BF3溶于水后.在一定条件下可转化为H3O+·[B(OH)F3]-,该物质中阳离子的空间构型为
(3)与BH
 互为等电子体的分子是
互为等电子体的分子是(4)EminBF4的熔点为12 ℃,在常温下为液体,由有机物阳离子[Emin]+和[BF4]-构成。该物质的晶体属于
(5)一种由硼和钐(Sm)形成的晶体的晶胞结构如图所示,已知晶胞常数a=n pm,则晶体的密度为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】晶胞中粒子数目的计算
(1)铜晶胞
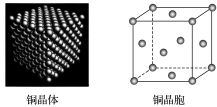
①位于顶角上的铜原子为_____________ 个晶胞共有。
②位于面心上的铜原子为_____________ 个晶胞共有。
因此晶体铜中属于某一晶胞的铜原子数是8× +6×
+6× =
=_____________ 。
(2)NaCl晶胞
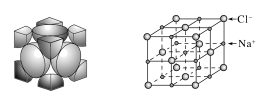
①Cl-位于_____________ 和_____________ ,共有_____________ 个。
②Na+位于_____________ 和_____________ ,共有_____________ 个。
(1)铜晶胞

①位于顶角上的铜原子为
②位于面心上的铜原子为
因此晶体铜中属于某一晶胞的铜原子数是8×
 +6×
+6× =
=(2)NaCl晶胞

①Cl-位于
②Na+位于
您最近一年使用:0次

 受热分解生成
受热分解生成 和
和 ,
, 四面体(如下图(a))中Si原子的杂化形式为
四面体(如下图(a))中Si原子的杂化形式为