运用分类的方法研究物质及变化的规律是化学学习的有效途径。
Ⅰ.物质的组成和性质都是对物质进行分类常用的依据,运用分类的方法可以发现物质及其变化的规律,预测物质的性质及可能发生的变化。
(1)①现有下列四种物质: 、
、 、
、 、
、 ,按类别将上述四种物质填入下表:
,按类别将上述四种物质填入下表:
②为了保护环境,应减少 在大气中的排放。
在大气中的排放。 属于酸性氧化物,可与NaOH、
属于酸性氧化物,可与NaOH、___________ (填与NaOH不同类别的一种具体物质,写化学式)等反应。写出 与足量NaOH溶液反应的化学方程式
与足量NaOH溶液反应的化学方程式___________ 。
Ⅱ.现有下列物质:① 、②稀硫酸、③熔化的
、②稀硫酸、③熔化的 、④无水酒精、⑤
、④无水酒精、⑤ 、⑥
、⑥ 、⑦镁铝合金,请回答下列问题:
、⑦镁铝合金,请回答下列问题:
(2)其中属于混合物的有___________ (填序号);属于电解质的有___________ (填序号)。
(3)写出②和⑤反应的离子方程式___________ 。
(4)请写出 在①中燃烧的实验现象:
在①中燃烧的实验现象:___________ 。
Ⅰ.物质的组成和性质都是对物质进行分类常用的依据,运用分类的方法可以发现物质及其变化的规律,预测物质的性质及可能发生的变化。
(1)①现有下列四种物质:
 、
、 、
、 、
、 ,按类别将上述四种物质填入下表:
,按类别将上述四种物质填入下表: | 类别 | 酸 | 碱 | 盐 | 酸性氧化物 |
| 物质 | a | b | c | d |
②为了保护环境,应减少
 在大气中的排放。
在大气中的排放。 属于酸性氧化物,可与NaOH、
属于酸性氧化物,可与NaOH、 与足量NaOH溶液反应的化学方程式
与足量NaOH溶液反应的化学方程式Ⅱ.现有下列物质:①
 、②稀硫酸、③熔化的
、②稀硫酸、③熔化的 、④无水酒精、⑤
、④无水酒精、⑤ 、⑥
、⑥ 、⑦镁铝合金,请回答下列问题:
、⑦镁铝合金,请回答下列问题:(2)其中属于混合物的有
(3)写出②和⑤反应的离子方程式
(4)请写出
 在①中燃烧的实验现象:
在①中燃烧的实验现象:
更新时间:2021-12-11 15:38:48
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】含氯消毒剂、医用酒精、过氧乙酸(CH3COOOH)、氯仿(CHCl3)等均能有效灭活病毒。回答下列问题:
(1)下列属于电解质的是_______ (填字母,下同);属于有机化合物的是_______ 。
A.漂白粉 B.医用酒精 C.过氧乙酸 D.氯仿
(2)工业上制备漂白粉的化学方程式为_______ 。
(3)“84消毒液”的有效成分为NaClO,不可与酸性清洁剂(主要含稀盐酸)混合使用的原因是______ (用离子方程式说明)。
(4)实验室可用下列装置制取氯仿(难溶于水。易溶于乙醇等有机溶剂,密度为1.48g·cm-3,沸点61.3℃)。

①仪器a的名称为_______ 。
②收集时锥形瓶中放适量水的目的是_______ 。
③从锥形瓶的收集液中获得氯仿的操作方法是_______ 。
(1)下列属于电解质的是
A.漂白粉 B.医用酒精 C.过氧乙酸 D.氯仿
(2)工业上制备漂白粉的化学方程式为
(3)“84消毒液”的有效成分为NaClO,不可与酸性清洁剂(主要含稀盐酸)混合使用的原因是
(4)实验室可用下列装置制取氯仿(难溶于水。易溶于乙醇等有机溶剂,密度为1.48g·cm-3,沸点61.3℃)。

①仪器a的名称为
②收集时锥形瓶中放适量水的目的是
③从锥形瓶的收集液中获得氯仿的操作方法是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】有以下9种物质,请回答下列问题:
①干冰②氯化钠③蔗糖④稀硫酸⑤NaHSO4溶液⑥碳酸氢钠⑦氢氧化钡溶液⑧氯化氢⑨NH3
(1)其中能导电的是__ (填写序号,下同);属于电解质的是__ ;属于非电解质的是__ 。
(2)分别写出物质⑤在水中的电离方程式:__ 。
(3)写出物质④和⑦反应的离子方程式:__ 。
(4)写出物质⑤和⑥在水中发生反应的离子方程式:__ 。
①干冰②氯化钠③蔗糖④稀硫酸⑤NaHSO4溶液⑥碳酸氢钠⑦氢氧化钡溶液⑧氯化氢⑨NH3
(1)其中能导电的是
(2)分别写出物质⑤在水中的电离方程式:
(3)写出物质④和⑦反应的离子方程式:
(4)写出物质⑤和⑥在水中发生反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】离子反应是中学化学中重要的反应类型,回答下列问题:
I.下列物质:①铜②纯碱③Ba(OH)2固体④Cu2(OH)2CO3⑤盐酸溶液⑥酒精⑦熔融的NaCl⑧二氧化碳。
(1)属于盐类的是____ 。
(2)属于非电解质是____ 。
(3)属于电解质的是____ 。
(4)能导电的是____ 。
II.将两种化合物一起溶于水得到一种无色透明溶液,溶液中含有下列离子中的某些离子:K+、Mg2+、Fe3+、Ba2+、 、OH-、
、OH-、 和Cl-,取该溶液进行如下实验:
和Cl-,取该溶液进行如下实验:
I.取少量溶液滴入紫色石蕊试液,溶液呈蓝色。
II.取少许溶液滴入BaCl2溶液,无白色沉淀产生。
III.取少许溶液先滴加硝酸再加AgNO3溶液,产生白色沉淀。
IV.再取少许原溶液滴入少量H2SO4溶液,有白色沉淀产生。
(5)根据以上现象判断,原溶液中肯定不存在的离子是____ 。
(6)写出实验Ⅲ中可能发生反应的离子方程式____ ,____ 。
(7)如溶液中各种离子数相等,确定溶液中____ (填有或无)K+。判断依据是____ 。
I.下列物质:①铜②纯碱③Ba(OH)2固体④Cu2(OH)2CO3⑤盐酸溶液⑥酒精⑦熔融的NaCl⑧二氧化碳。
(1)属于盐类的是
(2)属于非电解质是
(3)属于电解质的是
(4)能导电的是
II.将两种化合物一起溶于水得到一种无色透明溶液,溶液中含有下列离子中的某些离子:K+、Mg2+、Fe3+、Ba2+、
 、OH-、
、OH-、 和Cl-,取该溶液进行如下实验:
和Cl-,取该溶液进行如下实验:I.取少量溶液滴入紫色石蕊试液,溶液呈蓝色。
II.取少许溶液滴入BaCl2溶液,无白色沉淀产生。
III.取少许溶液先滴加硝酸再加AgNO3溶液,产生白色沉淀。
IV.再取少许原溶液滴入少量H2SO4溶液,有白色沉淀产生。
(5)根据以上现象判断,原溶液中肯定不存在的离子是
(6)写出实验Ⅲ中可能发生反应的离子方程式
(7)如溶液中各种离子数相等,确定溶液中
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】物质在水中可能存在电离平衡、盐的水解平衡和沉淀溶解平衡,请回答:
(1)泡沫灭火剂包括 溶液(约1
溶液(约1 ),
), 溶液(约1
溶液(约1 )及起泡剂,使用时发生反应的离子方程式为
)及起泡剂,使用时发生反应的离子方程式为___________ 。
(2)含等物质的量的 和
和 的溶液物料守恒式为
的溶液物料守恒式为___________ 。
(3)向2 0.1
0.1
 溶液中加入1
溶液中加入1 0.1
0.1 氨水,有白色沉淀产生,继续加入4滴0.1
氨水,有白色沉淀产生,继续加入4滴0.1
 溶液,观察到白色沉淀变为红褐色。试用离子方程式解释白色沉淀变为红褐色的原因:
溶液,观察到白色沉淀变为红褐色。试用离子方程式解释白色沉淀变为红褐色的原因:___________ 。
(4)向 溶液中滴加氨水产生蓝色沉淀,若所得溶液
溶液中滴加氨水产生蓝色沉淀,若所得溶液 ,已知
,已知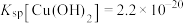 ,则溶液中
,则溶液中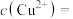
______  。
。
(5)某溶液只含 、
、 、
、 三种金属离子,且三种离子沉淀时的
三种金属离子,且三种离子沉淀时的 如下表所示:为制备
如下表所示:为制备 ,除去
,除去 、
、 离子应该先加入
离子应该先加入_________ ,然后再加入________ ,调节pH范围为_______ 。
(1)泡沫灭火剂包括
 溶液(约1
溶液(约1 ),
), 溶液(约1
溶液(约1 )及起泡剂,使用时发生反应的离子方程式为
)及起泡剂,使用时发生反应的离子方程式为(2)含等物质的量的
 和
和 的溶液物料守恒式为
的溶液物料守恒式为(3)向2
 0.1
0.1
 溶液中加入1
溶液中加入1 0.1
0.1 氨水,有白色沉淀产生,继续加入4滴0.1
氨水,有白色沉淀产生,继续加入4滴0.1
 溶液,观察到白色沉淀变为红褐色。试用离子方程式解释白色沉淀变为红褐色的原因:
溶液,观察到白色沉淀变为红褐色。试用离子方程式解释白色沉淀变为红褐色的原因:(4)向
 溶液中滴加氨水产生蓝色沉淀,若所得溶液
溶液中滴加氨水产生蓝色沉淀,若所得溶液 ,已知
,已知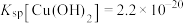 ,则溶液中
,则溶液中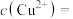
 。
。(5)某溶液只含
 、
、 、
、 三种金属离子,且三种离子沉淀时的
三种金属离子,且三种离子沉淀时的 如下表所示:为制备
如下表所示:为制备 ,除去
,除去 、
、 离子应该先加入
离子应该先加入| 金属离子 |  |  |  | |
 | 氢氧化物开始沉淀 | 1.9 | 7.0 | 4.7 |
| 氢氧化物完全沉淀 | 3.2 | 9.0 | 6.7 | |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】回答下列问题
(1)按要求写出方程式:
①HNO3(电离方程式)___________
②硫酸钠和氯化钡溶液反应(离子方程式)___________
③钠与水反应(离子方程式)___________
(2)以下为中学化学中常见的几种物质:①二氧化碳②熔融KC1③NaHSO4固体④铜⑤稀硫酸⑥蔗糖⑦澄清石灰水,其中属于电解质的有___________ ,属于非电解质的有___________ (填编号)。
(3)高铁酸钠(Na2FeO4)(铁为+6价)是一种新型的净水剂,可以通过下述反应制取:2Fe(OH)3+4NaOH+3NaClO=2Na2FeO4+3NaCl+5H2O
①该反应中氧化剂是___________ (用化学式表示,后同),___________ 元素被氧化,还原产物为___________
②用单线桥在方程式中标出电子转移的情况:___________ 。
2Fe(OH)3+4NaOH+3NaC1O=2Na2FeO4+3NaCl+5H2O
(1)按要求写出方程式:
①HNO3(电离方程式)
②硫酸钠和氯化钡溶液反应(离子方程式)
③钠与水反应(离子方程式)
(2)以下为中学化学中常见的几种物质:①二氧化碳②熔融KC1③NaHSO4固体④铜⑤稀硫酸⑥蔗糖⑦澄清石灰水,其中属于电解质的有
(3)高铁酸钠(Na2FeO4)(铁为+6价)是一种新型的净水剂,可以通过下述反应制取:2Fe(OH)3+4NaOH+3NaClO=2Na2FeO4+3NaCl+5H2O
①该反应中氧化剂是
②用单线桥在方程式中标出电子转移的情况:
2Fe(OH)3+4NaOH+3NaC1O=2Na2FeO4+3NaCl+5H2O
您最近一年使用:0次
填空题
|
适中
(0.64)
【推荐3】写出下列反应的离子方程式:
(1)氢氧化钡溶液与硫酸铜溶液反应:_____________________________________ 。
(2)碳酸钙固体中加入足量醋酸:_________________________________________ 。
(3)氧化铁和稀硫酸溶液反应:___________________________________________ 。
(4)向NaHSO4溶液中逐滴加入Ba(OH)2溶液至中性:________________________ 。
(1)氢氧化钡溶液与硫酸铜溶液反应:
(2)碳酸钙固体中加入足量醋酸:
(3)氧化铁和稀硫酸溶液反应:
(4)向NaHSO4溶液中逐滴加入Ba(OH)2溶液至中性:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】实验室所用的氯水为什么是新制的?_______________ 

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】有以下7种生活中常见的物质:① ;②氧化钠;③漂白粉;④
;②氧化钠;③漂白粉;④ ;⑤食盐水;⑥NaOH。回答下列问题:
;⑤食盐水;⑥NaOH。回答下列问题:
(1)以上物质中属于电解质的是_______ (填序号,下同);属于碱的是_______ ;属于盐的是_______ 。
(2)①在水中电离的方程为_______ 。
(3)②与稀盐酸反应的离子方程式为_______ 。
(4)写出④转化成①的化学方程式_______ 。
(5)现设计实验由大理石( )、水、氯气来制取③:大理石(
)、水、氯气来制取③:大理石( )
) ③溶液
③溶液 ③,请写出在制取③的实验过程中发生的化学方程式:
③,请写出在制取③的实验过程中发生的化学方程式:_______ 。
 ;②氧化钠;③漂白粉;④
;②氧化钠;③漂白粉;④ ;⑤食盐水;⑥NaOH。回答下列问题:
;⑤食盐水;⑥NaOH。回答下列问题:(1)以上物质中属于电解质的是
(2)①在水中电离的方程为
(3)②与稀盐酸反应的离子方程式为
(4)写出④转化成①的化学方程式
(5)现设计实验由大理石(
 )、水、氯气来制取③:大理石(
)、水、氯气来制取③:大理石( )
) ③溶液
③溶液 ③,请写出在制取③的实验过程中发生的化学方程式:
③,请写出在制取③的实验过程中发生的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】从物质类别和元素化合价两个维度研究物质的性质及转化是重要的化学学习方法。氯及其化合物有重要用途,如图为氯元素的“价类二维图”的部分信息。请回答下列问题:
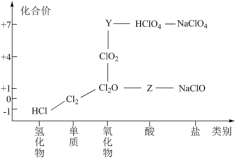
(1)根据图中信息写出Y、Z的化学式______ 、______ 。
(2)漂白液的有效成分是______ ,氯气既有氧化性又有还原性,结合图示说明理由______ 。
(3)实验室可用二氧化锰与浓盐酸在加热条件下制得氯气。写出该反应的化学方程式______ ,该反应中盐酸表现______ (填字母)。
A.酸性 B.氧化性 C.还原性
(4)84消毒液使用说明中特别提醒不可与洁厕灵混合使用,否则会产生氯气,有关反应方程式为NaClO+2HCl═NaCl+Cl2↑+H2O,下列有关该反应说法不正确 的是______ 。
(5)ClO2在杀菌消毒过程中会产生副产物亚氯酸盐(ClO ),需将其转化为Cl-除去,下列试剂中可将ClO
),需将其转化为Cl-除去,下列试剂中可将ClO 转化为Cl-的是
转化为Cl-的是______ (填字母)。

(1)根据图中信息写出Y、Z的化学式
(2)漂白液的有效成分是
(3)实验室可用二氧化锰与浓盐酸在加热条件下制得氯气。写出该反应的化学方程式
A.酸性 B.氧化性 C.还原性
(4)84消毒液使用说明中特别提醒不可与洁厕灵混合使用,否则会产生氯气,有关反应方程式为NaClO+2HCl═NaCl+Cl2↑+H2O,下列有关该反应说法
| A.n(氧化剂)∶n(还原剂)=1∶1 | B.n(氧化剂)∶n(还原剂)=1∶2 |
| C.氧化性:NaClO>Cl2 | D.Cl2既是氧化产物又是还原产物 |
 ),需将其转化为Cl-除去,下列试剂中可将ClO
),需将其转化为Cl-除去,下列试剂中可将ClO 转化为Cl-的是
转化为Cl-的是| A.O3 | B.FeSO4 | C.KI | D.KMnO4 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】乙烯的产量可以用来衡量一个国家的石油化工发展水平。请回答下列问题:
(1)乙烯的结构式是_______ 。
(2)若将乙烯气体通入溴的四氯化碳溶液中,反应的化学方程式为_______ 。
(3)可以用来除去乙烷中混有的少量乙烯的试剂是_______ (填序号)。
①水 ②氢气 ③溴水 ④酸性 溶液
溶液
(4)在一定条件下,乙烯能与水反应生成有机物A,其反应类型是_______ 反应(填“取代”或“加成”)。
(5)下列化学反应原理相同的一组是_______ (填序号)。
①乙烯使溴的四氯化碳溶液和酸性KMnO4溶液褪色
② 使溴水和酸性KMnO4溶液褪色
使溴水和酸性KMnO4溶液褪色
③ 使品红溶液和滴有酚酞的NaOH溶液褪色
使品红溶液和滴有酚酞的NaOH溶液褪色
(1)乙烯的结构式是
(2)若将乙烯气体通入溴的四氯化碳溶液中,反应的化学方程式为
(3)可以用来除去乙烷中混有的少量乙烯的试剂是
①水 ②氢气 ③溴水 ④酸性
 溶液
溶液(4)在一定条件下,乙烯能与水反应生成有机物A,其反应类型是
(5)下列化学反应原理相同的一组是
①乙烯使溴的四氯化碳溶液和酸性KMnO4溶液褪色
②
 使溴水和酸性KMnO4溶液褪色
使溴水和酸性KMnO4溶液褪色③
 使品红溶液和滴有酚酞的NaOH溶液褪色
使品红溶液和滴有酚酞的NaOH溶液褪色
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】“飘尘”是物质燃烧时产生的粒子漂浮物,颗粒很小(直径小于10-7m),不易沉降(可漂浮数小时甚至数年),它与空气中SO2、O2接触时,SO2部分转化为SO3,使空气中酸度增加形成酸雨。
(1)下列关于SO2的叙述中,正确的是_____ ;
A.SO2既可以做氧化剂,也可以做还原剂 B.SO2不是大汽污染物 C.大气中SO2的主要来源是汽车排出的尾气 D.SO2具有漂白性,因而可以使石蕊溶液褪色
(2)下列反应中,SO2表现了还原性的是_______ ;
A.SO2+H2O⇌H2SO3 B.SO2+2NaOH=Na2CO3+H2O C.2SO2+O2 2SO3 D.SO2+CaO=CaSO3
2SO3 D.SO2+CaO=CaSO3
(3)不能鉴别二氧化碳和二氧化硫的试剂是________ ;
A.品红溶液 B.澄清石灰水 C.溴水 D.酸性高锰酸钾溶液
(4)下列哪种危害不是酸雨导致的_______ ;
A.造成洪涝灾害 B.腐蚀建筑物 C.恶化人类环境 D.导致树木枯萎
(5)根据SO2通入不同溶液中实验现象,所得结论不正确的是_______ ;
(6)减少酸雨产生的途径可采取下列的哪些措施___________ 。
①少用煤做燃料 ②把工厂烟囱造高 ③燃料脱硫 ④飞机、汽车等交通工具采用清洁燃料,如天然气等 ⑤开发新能源
(1)下列关于SO2的叙述中,正确的是
A.SO2既可以做氧化剂,也可以做还原剂 B.SO2不是大汽污染物 C.大气中SO2的主要来源是汽车排出的尾气 D.SO2具有漂白性,因而可以使石蕊溶液褪色
(2)下列反应中,SO2表现了还原性的是
A.SO2+H2O⇌H2SO3 B.SO2+2NaOH=Na2CO3+H2O C.2SO2+O2
 2SO3 D.SO2+CaO=CaSO3
2SO3 D.SO2+CaO=CaSO3(3)不能鉴别二氧化碳和二氧化硫的试剂是
A.品红溶液 B.澄清石灰水 C.溴水 D.酸性高锰酸钾溶液
(4)下列哪种危害不是酸雨导致的
A.造成洪涝灾害 B.腐蚀建筑物 C.恶化人类环境 D.导致树木枯萎
(5)根据SO2通入不同溶液中实验现象,所得结论不正确的是
| 溶液 | 现象 | 结论 | |
| A | 含HCl、BaCl2的FeCl3溶液 | 产生白色沉淀 | SO2有还原性 |
| B | H2S溶液 | 产生黄色沉淀 | SO2有氧化性 |
| C | 酸性KMnO4溶液 | 紫色溶液褪色 | SO2有漂白性 |
| D | Na2SiO3溶液 | 产生胶状沉淀 | 酸性:H2SO3>H2SiO3 |
(6)减少酸雨产生的途径可采取下列的哪些措施
①少用煤做燃料 ②把工厂烟囱造高 ③燃料脱硫 ④飞机、汽车等交通工具采用清洁燃料,如天然气等 ⑤开发新能源
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】硫和氮是两种重要的元素,它们的氧化物又是造成空气污染的主要物质。
(1)汽车尾气含有NO、CO等多种污染物,是城市的污染源。
①用化学方程式表示产生NO的原因___ 。
②治理尾气方法是加装催化转化装置,使NO和CO反应转化为无污染的两种气体,发生反应的化学方程式是___ 。
(2)工业上产生的NO2可用NH3在一定条件下消除污染。
①写出此反应的化学方程式___ 。
②在标准状况下,消耗NO233.6L,则此反应的氧化产物比还原产物多___ g。
(3)工业上为了减少燃煤过程中SO2的排放,向燃煤中加入生石灰,其产物可作建筑材料。写出有关反应的化学方程式___ 。
(1)汽车尾气含有NO、CO等多种污染物,是城市的污染源。
①用化学方程式表示产生NO的原因
②治理尾气方法是加装催化转化装置,使NO和CO反应转化为无污染的两种气体,发生反应的化学方程式是
(2)工业上产生的NO2可用NH3在一定条件下消除污染。
①写出此反应的化学方程式
②在标准状况下,消耗NO233.6L,则此反应的氧化产物比还原产物多
(3)工业上为了减少燃煤过程中SO2的排放,向燃煤中加入生石灰,其产物可作建筑材料。写出有关反应的化学方程式
您最近一年使用:0次



