设NA为阿伏加德罗常数的值,下列叙述正确的是
| A.密闭容器中,1molN2和3molH2充分催化反应后分子总数为2 NA |
| B.常温常压下,46g NO2和N2O4的混合气体中含有的氧原子数目为2 NA |
| C.58.5gNaCl固体中含有NA个分子 |
| D.12g 金刚石中含有4 NA σ键 |
更新时间:2021-12-10 21:55:22
|
相似题推荐
单选题
|
适中
(0.65)
真题
名校
【推荐1】NA为阿伏加德罗常数的数值,下列说法中正确的是( )
| A.在密闭容器中加入l.5mol H2和0.5molN2,充分反应后得到NH3分子数为NA |
| B.一定条件下,2.3g的Na完全与O2反应生成3.6g产物时失去的电子数为0.1NA |
| C.1.0L的0.1 mol·L-1Na2S溶液中含有的S2-离子数为0.1NA |
| D.标准状况下,22.4L的CCl4中含有的CCl4分子数为NA |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】阿伏加德罗常数的命名是为了纪念意大利科学家阿伏加德罗,用NA代表阿伏加德罗常数的值,下列说法正确的是
| A.1molFe粉与足量高温水蒸气反应,转移电子数为3mol |
| B.1mol2D216O含有的中子数为10NA |
| C.25℃,101kPa下,22.4 LO2含有的氧原子数为2NA |
| D.2 mol·L- 1KCl溶液中含有的离子数为4NA |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】设NA为阿伏加德罗常数的值,下列说法正确的是
| A.36 g由35Cl和37Cl组成的氯气中所含质子数一定为17NA |
| B.一定条件下,6.4 g铜与过量的硫粉反应,转移电子数目为0.2NA |
| C.常温常压下,水蒸气通过过氧化钠使其增重4 g时,反应中转移的电子数为2NA |
| D.0.4 mol NH3与0.6 mol O2在加热及催化剂条件下充分反应,得到NO的分子数为0.4NA |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】设NA为阿伏加 德罗常数的值,下列说法正确的是
| A.1LpH=6的纯水中含有OH-的数目为10-8NA |
| B.当氢氧酸性燃料电池中转移2mol电子时被氧化的分子数为NA |
C.0.5mol雄黄(As4S4,结构如图 ),含有NA个S—S键 ),含有NA个S—S键 |
| D.一定条件下向密闭容器中充入1molH2和2molH2(g)充分反应,生成HI分子数最多等于2NA |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】 工业合成氨,关乎到世界化工发展和粮食安全,对其研究意义重大。下列有关合成氨反应:
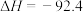 kJ⋅mol
kJ⋅mol 的说法
的说法不 正确的是

 kJ⋅mol
kJ⋅mol 的说法
的说法A.合成氨反应的 J⋅K J⋅K ⋅mol ⋅mol ,在较低温度下不能自发进行 ,在较低温度下不能自发进行 |
| B.氮气和氢气的反应活化能很大,需要外界提供能量才可能发生反应 |
C.恒温恒容密闭容器中充入1mol 和3mol 和3mol ,充分反应后放出热量小于92.4kJ ,充分反应后放出热量小于92.4kJ |
| D.温度升高,反应物的活化分子百分数增大,有效碰撞次数增多,反应速率增大 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】在标准状况下,将2.24L 与4.48LHCl气体充入密闭容器内混合。设
与4.48LHCl气体充入密闭容器内混合。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 与4.48LHCl气体充入密闭容器内混合。设
与4.48LHCl气体充入密闭容器内混合。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.反应中有 个H-Cl键断裂 个H-Cl键断裂 | B.反应中没有离子键的断裂和形成 |
| C.混合后,容器内物质含有非极性键 | D.混合后,容器内物质含有 个共价键 个共价键 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法不正确的是
| A.离子化合物含离子键,也可能含极性键或非极性键 |
| B.含金属元素的化合物一定是离子化合物 |
| C.强电解质不一定是离子化合物 |
| D.熔融状态能导电的化合物是离子化合物 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】观察下列模型并结合有关信息进行判断,下列说法错误的是
| HCN | S8 | SF6 | B12结构单元 | |
| 结构模型示意图 | 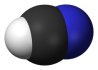 | 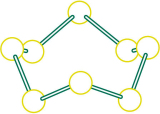 | 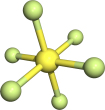 | 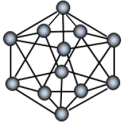 |
| 备注 | 易溶于CS2 | 熔点1873K |
| A.HCN的结构式为H-C三N,分子中“C三N”键含有1个σ键和2个π键 |
| B.固态硫S8属于原子晶体 |
| C.SF6是由极性键构成的非极性分子 |
| D.单质硼属于原子晶体 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列叙述中不正确 的是
A.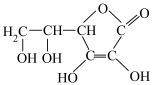 中含有2个手性碳原子 中含有2个手性碳原子 |
B.Cl2中两个氯原子形成共价键,轨道重叠示意图为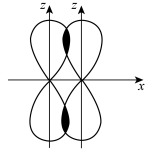 |
| C.对羟基苯甲醛形成分子间氢键,而邻羟基苯甲醛形成分子内氢键,所以对羟基苯甲醛的熔沸点比邻羟基苯甲醛的高 |
| D.CF3COOH的酸性大于CCl3COOH,是因为F的电负性大于Cl,最终导致CF3COOH的羧基中的羟基的极性更大 |
您最近半年使用:0次

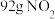 含有分子的数目为
含有分子的数目为
 的
的 溶液含有
溶液含有 的数目为
的数目为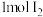 与
与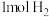 在密闭容器中充分反应,生成HI分子的数目为
在密闭容器中充分反应,生成HI分子的数目为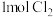 和足量铁粉反应,转移电子的数目为
和足量铁粉反应,转移电子的数目为 分子间作用力较小
分子间作用力较小 与
与 的不同状态可以说明
的不同状态可以说明

