下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题:
(1)④、⑤、⑥的离子半径由大到小的顺序为___________ (用对应的离子符号表示)。
(2)②、③、⑦的最高价氧化物对应水化物的酸性由强到弱的顺序是___________ (填相应的酸)。
(3)元素④、⑤可形成既含离子键又含共价键的化合物,写出符合要求的化合物的电子式:___________ 。
(4)写出表中①~⑧元素中最高价氧化物对应水化物碱性最强的物质和自然界中含量最高的金属元素对应的单质反应的离子方程式:___________ 。
族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ |
(2)②、③、⑦的最高价氧化物对应水化物的酸性由强到弱的顺序是
(3)元素④、⑤可形成既含离子键又含共价键的化合物,写出符合要求的化合物的电子式:
(4)写出表中①~⑧元素中最高价氧化物对应水化物碱性最强的物质和自然界中含量最高的金属元素对应的单质反应的离子方程式:
更新时间:2021-11-12 23:11:06
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用。表中列出了钙元素及a~f6种元素在周期表中的位置。
(1)a的元素符号是____ ;e的最高价氧化物是____ 。
(2)c、d的最高价氧化物对应的水化物中,碱性较弱的物质是____ (写化学式)。
(3)用电子式表示c与f组成的化合物的形成过程____ 。
(4)非金属性b强于e,用原子结构解释原因____ 。
(5)下列关于f及其化合物的推断中,正确的是____ (填字母)。
a.f的最高化合价均为+7价
b.f单质的氧化性在同主族中最强
c.f的最高价氧化物对应的水化物的溶液pH<7
(6)某种牛奶的营养成分表如表所示。
①营养成分表中,所含物质质量最大的是____ 。
②已知镁能与O2、H2O反应,对比钙与镁的原子结构和在元素周期表中的位置关系,你预测金属钙的性质是____ 。
③请结合钙的化学性质判断牛奶中钙的存在形式为____ (填“单质”或“化合物”)。
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | a | b | ||||||
| 3 | c | d | e | f | ||||
| 4 | Ca |
(2)c、d的最高价氧化物对应的水化物中,碱性较弱的物质是
(3)用电子式表示c与f组成的化合物的形成过程
(4)非金属性b强于e,用原子结构解释原因
(5)下列关于f及其化合物的推断中,正确的是
a.f的最高化合价均为+7价
b.f单质的氧化性在同主族中最强
c.f的最高价氧化物对应的水化物的溶液pH<7
(6)某种牛奶的营养成分表如表所示。
| 营养成分表 | ||
| 项目 | 每100g | NRV% |
| 能量 | 309kJ | 4% |
| 蛋白质 | 3.6g | 6% |
| 脂肪 | 4.4g | 7% |
| 碳水化合物 | 5.0g | 2% |
| 钠 | 65mg | 3% |
| 钙 | 120mg | 15% |
②已知镁能与O2、H2O反应,对比钙与镁的原子结构和在元素周期表中的位置关系,你预测金属钙的性质是
③请结合钙的化学性质判断牛奶中钙的存在形式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】下表是元素周期表的一部分,除标出的元素外,表中的每个编号代表一种元素。请根据要求回答问题:
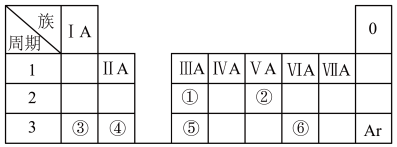
(1)②的元素符号是____ ;
(2)①和⑤的原子半径大小关系是①____ ⑤(填“>”“<”或“=”);
(3)③、④和⑤中,金属性最强的元素是____ (填元素符号);
(4)⑤、⑥的最高价氧化物对应的水化物相互反应的离子方程式为____ 。

(1)②的元素符号是
(2)①和⑤的原子半径大小关系是①
(3)③、④和⑤中,金属性最强的元素是
(4)⑤、⑥的最高价氧化物对应的水化物相互反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】重晶石( )作为原料制备金属钡及其他含钡化合物的方法如下图:
)作为原料制备金属钡及其他含钡化合物的方法如下图:
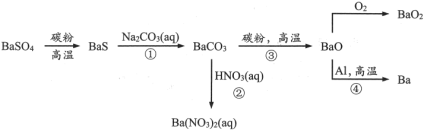
完成下列填空:
(1)Ba在元素周期表中位于第_______ 族,最外层电子的电子云形状是_______ 。图中涉及的第二周期元素原子半径由大到小的顺序是_______ ,可以判断其中两种元素非金属性强弱的反应是_______ (选填流程中的反应编号)。
(2)配平BaS与稀硝酸反应的化学方程式:_______ 。
_______ _______
_______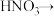 _______
_______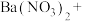 _______
_______ _______
_______ _______
_______
检验溶液中BaS是否完全反应的方法是:取少量反应液,加入_______ (填试剂),有黑色沉淀生成,则BaS未反应完全。
(3)工业上,利用反应①②而不用BaS直接与稀硝酸反应制 的原因是
的原因是_______ 。
(4)元素的金属性:Al_______ Ba(选填“>”或“<”);已知:沸点Al>Ba,反应④在真空容器中可以发生的理由是_______ 。
 )作为原料制备金属钡及其他含钡化合物的方法如下图:
)作为原料制备金属钡及其他含钡化合物的方法如下图:
完成下列填空:
(1)Ba在元素周期表中位于第
(2)配平BaS与稀硝酸反应的化学方程式:
_______
 _______
_______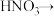 _______
_______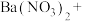 _______
_______ _______
_______ _______
_______
检验溶液中BaS是否完全反应的方法是:取少量反应液,加入
(3)工业上,利用反应①②而不用BaS直接与稀硝酸反应制
 的原因是
的原因是(4)元素的金属性:Al
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】现有部分短周期元素的性质或原子结构如下表:
(1)元素T的原子最外层共有___________ 种不同运动状态的电子;元素X的一种同位素可测定文物年代,这种同位素的符号是___________ 。
(2)元素Y与氢元素形成一种离子YH ,写出该微粒的结构式
,写出该微粒的结构式___________ (用元素符号表示且体现配位键)。
(3)下列表述中能证明非金属性较强的是Z这一事实的是___________ 。
a.常温下Z的单质和T的单质状态不同
b.Z的氢化物比T的氢化物稳定
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应
(4)探寻物质的性质差异性是学习的重要方法之一、T、X、Y、Z四种元素的最高价氧化物的水化物中化学性质明显不同于其他三种酸的是___________ (写化学式)。
| 元素编号 | 元素性质或原子结构 |
| T | M层上有2对成对电子 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 元素最高正价是+7价 |
(2)元素Y与氢元素形成一种离子YH
 ,写出该微粒的结构式
,写出该微粒的结构式(3)下列表述中能证明非金属性较强的是Z这一事实的是
a.常温下Z的单质和T的单质状态不同
b.Z的氢化物比T的氢化物稳定
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应
(4)探寻物质的性质差异性是学习的重要方法之一、T、X、Y、Z四种元素的最高价氧化物的水化物中化学性质明显不同于其他三种酸的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】W、X、Y、Z、M、G、H七种短周期元素,原子序数依次增大。W、Z同主族,可形成离子化合物ZW;Y、G同主族,可形成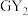 、
、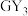 两种分子;X的气态氢化物与其最高价氧化物对应的水化物能反应;H不是稀有气体元素,W、X、Y、Z、M、G、H的最外层电子数之和等于29。请回答下列问题:
两种分子;X的气态氢化物与其最高价氧化物对应的水化物能反应;H不是稀有气体元素,W、X、Y、Z、M、G、H的最外层电子数之和等于29。请回答下列问题:
(1)Y在元素周期表中的位置为_______ 。
(2)X的气态氢化物的电子式为_____ ,工业合成X的气态氢化物的化学方程式为______ 。
(3)Y、Z、G三种元素原子半径由大到小的顺序是_______ (用元素符号表示)。
(4)Z、M最高价氧化物对应的水化物相互反应的离子方程式为_______ ,G的最高价氧化物对应的水化物的浓溶液与金属铜反应的化学方程式为_______ 。
(5)G的非金属性_______ (填“>”或“<”)H的非金属性,下列表述可以作为验证的证据的是_______ (填字母)。
A.比较这两种元素单质的沸点
B.比较这两种元素单质与氢气化合的难易程度
C.G和H单质分别与Fe反应生成FeG、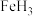
D.比较这两种元素单质与酸或碱反应的难易程度
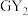 、
、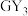 两种分子;X的气态氢化物与其最高价氧化物对应的水化物能反应;H不是稀有气体元素,W、X、Y、Z、M、G、H的最外层电子数之和等于29。请回答下列问题:
两种分子;X的气态氢化物与其最高价氧化物对应的水化物能反应;H不是稀有气体元素,W、X、Y、Z、M、G、H的最外层电子数之和等于29。请回答下列问题:(1)Y在元素周期表中的位置为
(2)X的气态氢化物的电子式为
(3)Y、Z、G三种元素原子半径由大到小的顺序是
(4)Z、M最高价氧化物对应的水化物相互反应的离子方程式为
(5)G的非金属性
A.比较这两种元素单质的沸点
B.比较这两种元素单质与氢气化合的难易程度
C.G和H单质分别与Fe反应生成FeG、
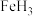
D.比较这两种元素单质与酸或碱反应的难易程度
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】短周期元素A、B、C、D、E在元素周期表中的位置如下图所示,其中B元素是碳元素。请回答下列问题:

(1)B元素在周期表中的位置:_________________ ;请写出该原子的电子式:___________ ;其原子核外电子能量最高的能级是:_______ 。
(2)比较A、C、D元素简单离子半径的大小:_______ >_______ >_______ (填微粒符号)。
(3)F与D同主族且相邻,请比较D的氢化物和F的氢化物稳定性大小:_______ (用化学式表示)。
(4)E单质常用湿润的淀粉碘化钾试纸检验。有学生对淀粉碘化钾进行了实验探究。在淀粉碘化钾溶液中,滴加少量次氯酸钠溶液,立刻会看到溶液变蓝色,这是因为_______ (请结合氧化还原反应知识解释相关现象,下同)。在所形成的蓝色溶液中,再滴加亚硫酸钠溶液,发现蓝色逐渐消失,这是因为_________________ 。据此分析,I2、ClO-、SO42-氧化性有弱到强的顺序排列为____________________ 。

(1)B元素在周期表中的位置:
(2)比较A、C、D元素简单离子半径的大小:
(3)F与D同主族且相邻,请比较D的氢化物和F的氢化物稳定性大小:
(4)E单质常用湿润的淀粉碘化钾试纸检验。有学生对淀粉碘化钾进行了实验探究。在淀粉碘化钾溶液中,滴加少量次氯酸钠溶液,立刻会看到溶液变蓝色,这是因为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】X、Y、Z、W、M为短周期主族元素,25℃时,其最高价氧化物对应的水化物(浓度均为0.01mol·L-1)溶液的pH和原子半径的关系如图所示。

(1)Y的最高价氧化物的电子式为:___________ 。
(2)最简单气态氢化物的热稳定性:Z___________ W(>或<)
(3)X、M两种元素形成的简单离子半径大小顺序:X___________ M(>或<)。
(4)X的氢化物与Z的氢化物反应后生成的化合物中的化学键类型是___________ 。

(1)Y的最高价氧化物的电子式为:
(2)最简单气态氢化物的热稳定性:Z
(3)X、M两种元素形成的简单离子半径大小顺序:X
(4)X的氢化物与Z的氢化物反应后生成的化合物中的化学键类型是
您最近一年使用:0次
【推荐2】回答下列问题:
(1)第二周期元素的第一电离能 随原子序数
随原子序数 的变化情况如图。
的变化情况如图。 随Z的递增而呈增大趋势的原因是
随Z的递增而呈增大趋势的原因是________ ,原子核对外层电子的引力增大。导致 在a点出现齿峰的原因是
在a点出现齿峰的原因是________ 。

(2)① 常用于制造火柴,P和S的第一电离能较大的是
常用于制造火柴,P和S的第一电离能较大的是________ 。
② 俗称雄黄,其中基态As原子的核外电子排布式为[Ar]
俗称雄黄,其中基态As原子的核外电子排布式为[Ar] ________ ,有________ 个未成对电子。
③P、S、As电负性由大到小的顺序是________ 。
(1)第二周期元素的第一电离能
 随原子序数
随原子序数 的变化情况如图。
的变化情况如图。 随Z的递增而呈增大趋势的原因是
随Z的递增而呈增大趋势的原因是 在a点出现齿峰的原因是
在a点出现齿峰的原因是
(2)①
 常用于制造火柴,P和S的第一电离能较大的是
常用于制造火柴,P和S的第一电离能较大的是②
 俗称雄黄,其中基态As原子的核外电子排布式为[Ar]
俗称雄黄,其中基态As原子的核外电子排布式为[Ar] ③P、S、As电负性由大到小的顺序是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】联合国大会将2019年定为“化学元素周期表国际年”,高度体现了元素周期表的重要性。部分元素在周期表中的位置如图:
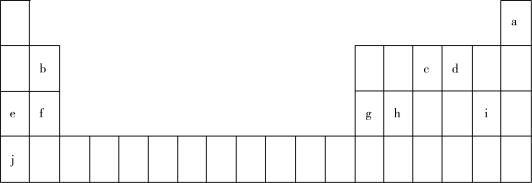
(1)2021年2月22日,嫦娥五号采样返回器带回的月壤公开亮相,对月壤中化学元素的分析有助于认识月球表面环境。
①月壤中含有较丰富的质量数为3的a,它可以作为未来核聚变的重要原料之一,a的这种核素表示为_______ 。
②经分析,月壤中含有大量的元素d和h,原子半径d_______ h(填“>”、“<”或“=”),元素h在周期表中的位置为_______ 。
(2)e和f的单质都是化学家戴维通过电解的方法首次制得。e的单质与水反应的化学方程式为_______ ,用电子式表示f原子与i原子形成化合物的形成过程:_______ 。
(3)d和i两种元素的简单氢化物中,熔沸点较高的氢化物的电子式为_______ 。
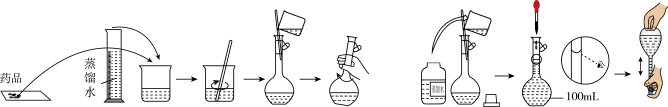
(4)《天工开物》记载,“凡火药,以硝石、硫磺为主,草木灰为辅”,由c、d、j三种元素组成的化合物是硝石的主要成分,化学式为_______ 。实验室按照如图操作配制该溶液,所得溶液浓度_______ (填“偏大”或“偏小”)。
(5)元素b与g的性质相似,可以预测b与g的单质或化合物也可能具有相似的性质。请写出b的最高价氧化物对应水化物与e的最高价氧化物对应水化物反应的化学方程式_______ 。

(1)2021年2月22日,嫦娥五号采样返回器带回的月壤公开亮相,对月壤中化学元素的分析有助于认识月球表面环境。
①月壤中含有较丰富的质量数为3的a,它可以作为未来核聚变的重要原料之一,a的这种核素表示为
②经分析,月壤中含有大量的元素d和h,原子半径d
(2)e和f的单质都是化学家戴维通过电解的方法首次制得。e的单质与水反应的化学方程式为
(3)d和i两种元素的简单氢化物中,熔沸点较高的氢化物的电子式为
(4)《天工开物》记载,“凡火药,以硝石、硫磺为主,草木灰为辅”,由c、d、j三种元素组成的化合物是硝石的主要成分,化学式为

(5)元素b与g的性质相似,可以预测b与g的单质或化合物也可能具有相似的性质。请写出b的最高价氧化物对应水化物与e的最高价氧化物对应水化物反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】X、Y、Z、W、R、Q为原子序数依次增大的六种短周期主族元素。X是原子半径最小的元素;Y原子最外层电子数是核外电子层数的3倍;Z是短周期中金属性最强的元素;W是地壳中含量最多的金属元素;R的最高正价与最低负价代数和为4.回答下列问题:
(1)W在周期表中的位置是___________ 。
(2)ZYX的电子式为___________ ,Z2Y2中含有的化学键类型为___________ 。
(3)Y、Z、W三种元素对应的简单离子半径由大到小的顺序是___________ (用元素的离子符号表示)。
(4)下列说法能证明非金属性Q强于R的是___________ 。(填字母)。
a.简单阴离子的还原性:
b.简单氢化物热稳定性:Q>R
c.氧化物对应的水化物的酸性:
d.Q的单质能从H2R溶液中置换出R单质
(5)W的最高价氧化物对应的水化物与Z的最高价氧化物对应的水化物反应的化学方程式为___________ 。
(1)W在周期表中的位置是
(2)ZYX的电子式为
(3)Y、Z、W三种元素对应的简单离子半径由大到小的顺序是
(4)下列说法能证明非金属性Q强于R的是
a.简单阴离子的还原性:

b.简单氢化物热稳定性:Q>R
c.氧化物对应的水化物的酸性:

d.Q的单质能从H2R溶液中置换出R单质
(5)W的最高价氧化物对应的水化物与Z的最高价氧化物对应的水化物反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】有A、B、C、D、E五种短周期元素,它们的核电荷数按C、A、B、D、E的顺序增大。C、D都能分别与A按原子个数比为1∶1或2∶1形成化合物;CB可与EA2反应生成C2A与气态物质EB4;E的M层电子数是K层电子数的2倍。
(1)写出下列元素的名称:B:________ E:________ 。
(2)写出EB4的化学式:__________ 。
(3)D2A2中含有的化学键类型为____________ 。
(4)由A、C、D三种元素组成的化合物M属于________ (填“离子”或“共价”)化合物,M溶于水后________ (填“能”或“不能”)发生化学变化,原因是(从化学键变化的角度解释):___________________________________ 。
(1)写出下列元素的名称:B:
(2)写出EB4的化学式:
(3)D2A2中含有的化学键类型为
(4)由A、C、D三种元素组成的化合物M属于
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】A、B、C、D、E为原子序数依次增大的5种短周期主族元素,其中仅含有一种金属元素,A单质是自然界中密度最小的气体,A和D最外层电子数相同;B元素原子结构示意图为 ;C和E在周期表中相邻,且E的质子数是C的2倍。请回答下列问题:
;C和E在周期表中相邻,且E的质子数是C的2倍。请回答下列问题:
(1)B位于第____________ 周期_____________ 族;
(2)E的离子结构示意图是_________________ ;DA中含有______________ 。(填化学键类型)
(3)用电子式表示BC2的形成过程________________________________________ ;(用具体元素表示)
(4)C、D、E三种元素简单离子的离子半径由大到小的顺序是______________________ 。(用具体离子符号表示)
 ;C和E在周期表中相邻,且E的质子数是C的2倍。请回答下列问题:
;C和E在周期表中相邻,且E的质子数是C的2倍。请回答下列问题: (1)B位于第
(2)E的离子结构示意图是
(3)用电子式表示BC2的形成过程
(4)C、D、E三种元素简单离子的离子半径由大到小的顺序是
您最近一年使用:0次



