测定溶液中的钙离子浓度的基本操作为:向溶液中加入(NH4)2C2O4将钙离子转化为CaC2O4沉淀,滤出沉淀,将沉淀溶于硫酸中,生成H2C2O4和CaSO4稀溶液。然后加入KMnO4标准溶液,将H2C2O4完全氧化。再用 (NH4)2Fe(SO4)2 溶液滴定过量的KMnO4,现取20.00mL某溶液进行上述处理。加入0.1000mol/LKMnO4标准溶液12.00mL,消耗0.2000mol/L的(NH4)2Fe(SO4)2溶液20.00mL。
(1)写出KMnO4与H2C2O4反应的离子方程式___________ 。
(2)求溶液中钙离子的浓度___________ 。
(1)写出KMnO4与H2C2O4反应的离子方程式
(2)求溶液中钙离子的浓度
更新时间:2021-12-18 18:52:07
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】对于数以千万计的化学物质和为数更多的化学反应,分类法的作用几乎是无可替代的。
(1)现有下列6种物质:H2O、SiO2、CaO、MgO、Fe2O3、Na2O2。按照不同的分类标准,它们中有一种物质与其他5种有明显不同,请找出这种物质,并写出依据(写出两种分类方法):
①__ ;__ ;
②__ ;__ ;
(2)KClO3和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯,其化学方程式为:2KClO3+4HCl(浓)=2KCl+2ClO2↑+Cl2↑+2H2O。(ClO2中氯元素的化合价为+4价)
(i)浓盐酸在反应中表现出来的性质是___ (填写编号)
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(ii)产生0.1molCl2,则消耗浓HCl的物质的量为___ mol。
(1)现有下列6种物质:H2O、SiO2、CaO、MgO、Fe2O3、Na2O2。按照不同的分类标准,它们中有一种物质与其他5种有明显不同,请找出这种物质,并写出依据(写出两种分类方法):
①
②
(2)KClO3和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯,其化学方程式为:2KClO3+4HCl(浓)=2KCl+2ClO2↑+Cl2↑+2H2O。(ClO2中氯元素的化合价为+4价)
(i)浓盐酸在反应中表现出来的性质是
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(ii)产生0.1molCl2,则消耗浓HCl的物质的量为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】根据所学知识,回答下列问题:
(1)自来水厂用氯气杀菌、消毒,其消毒原理主要是氯气溶于水后生成了HClO,写出HClO的电子式:_____ 。
(2)6.0g氮的氧化物NOx中,含N物质的量为0.2mol,则NOx的摩尔质量为_____ 。
(3)已知反应:3Cu+8HNO3(浓)=3Cu(NO3)2+2NO↑+4H2O(稀)。若有64gCu被氧化,则被还原的HNO3的物质的量是_____ 。
(4)ClO2是一种黄绿色气体,被称为“第四代”饮用水消毒剂。制备ClO2的一种方法为在平底烧瓶中加入KClO3固体、足量草酸(H2C2O4)、稀硫酸,60℃~80℃水浴加热。该反应的化学方程式为_____ 。
(1)自来水厂用氯气杀菌、消毒,其消毒原理主要是氯气溶于水后生成了HClO,写出HClO的电子式:
(2)6.0g氮的氧化物NOx中,含N物质的量为0.2mol,则NOx的摩尔质量为
(3)已知反应:3Cu+8HNO3(浓)=3Cu(NO3)2+2NO↑+4H2O(稀)。若有64gCu被氧化,则被还原的HNO3的物质的量是
(4)ClO2是一种黄绿色气体,被称为“第四代”饮用水消毒剂。制备ClO2的一种方法为在平底烧瓶中加入KClO3固体、足量草酸(H2C2O4)、稀硫酸,60℃~80℃水浴加热。该反应的化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】2020年突如其来的“新冠肺炎”使人们认识到日常杀菌消毒的重要性。其中含氯消毒剂在生产生活中有着广泛的用途。
(1)①写出实验室中制取氯气的化学方程式___________ ;实验室用___________ 除去混在氯气中的氯化氢杂质,用___________ 除去混在里面的水蒸气;
②写出次氯酸分解的化学反应方程式___________ ;新制氯水中使其呈现黄绿色的微粒是___________ ;使紫色石蕊溶液显红色的微粒是___________ ;能使红色布条褪色的微粒是___________ 。(填化学式)
(2)常温下,氯气与烧碱溶液反应得“84”消毒液,NaClO是“84”消毒液的有效成分,在此次抗击新冠病毒中发挥了重要作用。
①在空气中喷洒“84”消毒液可以达到对环境消毒的目的,其消毒原理为(用离子方程式表示):________ ;
②某温度下,将氯气通入NaOH溶液中,得到NaCl、NaClO和NaClO3的混合溶液,经测定ClO-与ClO 的离子个数比为1∶3,请配平该反应
的离子个数比为1∶3,请配平该反应_____________ 。
______Cl2+______OH-=______Cl-+1ClO-+3ClO +______H2O
+______H2O
(1)①写出实验室中制取氯气的化学方程式
②写出次氯酸分解的化学反应方程式
(2)常温下,氯气与烧碱溶液反应得“84”消毒液,NaClO是“84”消毒液的有效成分,在此次抗击新冠病毒中发挥了重要作用。
①在空气中喷洒“84”消毒液可以达到对环境消毒的目的,其消毒原理为(用离子方程式表示):
②某温度下,将氯气通入NaOH溶液中,得到NaCl、NaClO和NaClO3的混合溶液,经测定ClO-与ClO
 的离子个数比为1∶3,请配平该反应
的离子个数比为1∶3,请配平该反应______Cl2+______OH-=______Cl-+1ClO-+3ClO
 +______H2O
+______H2O
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】储氢纳米碳管具有广泛的用途,电弧法合成的碳纳米管常伴有大量的杂质碳纳米颗粒,这种碳钠来颗粒可用氧化气化法提纯,反应的化学方程式如下(未配平):




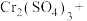

回答下列问题:
(1)配平上述反应方程式,并标出电子转移方向和数目___________ 。
(2) 在该反应中表现出___________(填标号)。
在该反应中表现出___________(填标号)。
(3)生成物中属于非电解质的有___________ 。
磷酸( )、次磷酸(
)、次磷酸( )是精细磷化工产品,均属于中强酸,磷酸为三元酸,而次磷酸为一元酸。回答下列问题:
)是精细磷化工产品,均属于中强酸,磷酸为三元酸,而次磷酸为一元酸。回答下列问题:
(4)① 及
及 均可将溶液中的
均可将溶液中的 还原为银,从而可用于化学镀银。从物质的分类来看,
还原为银,从而可用于化学镀银。从物质的分类来看, 属于
属于___________ (填标号)。
a.正盐 b.酸式盐 c.钠盐 d.氧化物
②写出 与足量NaOH溶液反应的离子方程式
与足量NaOH溶液反应的离子方程式___________ 。
(5)实验室可以用浓磷酸与NaBr(s)加热反应制取HBr气体,利用了浓磷酸的___________ 性,能否用浓硫酸代替浓磷酸制取HBr?说明理由___________ 。





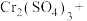

回答下列问题:
(1)配平上述反应方程式,并标出电子转移方向和数目
(2)
 在该反应中表现出___________(填标号)。
在该反应中表现出___________(填标号)。| A.只有酸性 | B.只有氧化性 |
| C.酸性和氧化性 | D.酸性和还原性 |
磷酸(
 )、次磷酸(
)、次磷酸( )是精细磷化工产品,均属于中强酸,磷酸为三元酸,而次磷酸为一元酸。回答下列问题:
)是精细磷化工产品,均属于中强酸,磷酸为三元酸,而次磷酸为一元酸。回答下列问题:(4)①
 及
及 均可将溶液中的
均可将溶液中的 还原为银,从而可用于化学镀银。从物质的分类来看,
还原为银,从而可用于化学镀银。从物质的分类来看, 属于
属于a.正盐 b.酸式盐 c.钠盐 d.氧化物
②写出
 与足量NaOH溶液反应的离子方程式
与足量NaOH溶液反应的离子方程式(5)实验室可以用浓磷酸与NaBr(s)加热反应制取HBr气体,利用了浓磷酸的
您最近一年使用:0次
【推荐3】(1)写出下列物质在水溶液中的电离方程式
①NaHCO3___________ ,
②NaHSO4___________ 。
(2)写出下列微粒的结构示意图
①最外层电子数为次外层电子数2倍的原子的结构示意图___________ ,
②第二层电子数为第一层、第三层电子数之和的原子形成的离子结构示意图:___________ 。
(3)配平并用双线桥表示电子转移的方向和数目:___________KI+___________HNO3——___________KNO3+___________NO↑+___________I2+___________H2O,___________ ,若反应中转移了0.9mol电子,则产生的气体在标准状况下的体积为___________ 。
(4)在一定温度下有分解反应A(s)=B(s)+C(g)+4D(g),若测得生成的气体的质量是同温同压下相同体积氢气的10倍,且当所生成的气体在标况下的体积为44.8L时,所得B的质量为60g,A的摩尔质量为___________ 。
①NaHCO3
②NaHSO4
(2)写出下列微粒的结构示意图
①最外层电子数为次外层电子数2倍的原子的结构示意图
②第二层电子数为第一层、第三层电子数之和的原子形成的离子结构示意图:
(3)配平并用双线桥表示电子转移的方向和数目:___________KI+___________HNO3——___________KNO3+___________NO↑+___________I2+___________H2O,
(4)在一定温度下有分解反应A(s)=B(s)+C(g)+4D(g),若测得生成的气体的质量是同温同压下相同体积氢气的10倍,且当所生成的气体在标况下的体积为44.8L时,所得B的质量为60g,A的摩尔质量为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】维生素C是一种水溶性维生素(其水溶液呈酸性),化学式为C6H8O6。人体缺乏维生素C可得坏血症,故维生素C又称抗坏血酸。新鲜的果蔬、乳制品富含维生素C。某校课外活动小组测定了某牌子橙汁中维生素C的含量。
测定原理: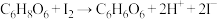
(1)实验用品及试剂:
试剂:___________ 指示剂(填名称),浓度为8.00×10-3mol·L-1的I2标准溶液、蒸馏水等。
I2标准溶液一般用棕色酸式滴定管盛装,请解释原因:___________ 。
(2)实验过程:
A.润洗后装好标准碘溶液、赶气泡、调零待用
B.用蒸馏水洗净所需仪器
C.用20mL移液管向锥形瓶中移入20.00mL待测橙汁
D.检查滴定管是否漏液
E.左手控制滴定管的活塞开关,右手摇动锥形瓶,眼睛注视锥形瓶,直到滴定终点。
F.向待测液中滴入2滴指示剂
①滴定操作的正确顺序是_____________ 。(用序号填写)
②滴定中消耗标准碘溶液体积是15.00mL,则此橙汁中维生素C的含量是_________ mg/L。

(3)问题讨论:
若摇动过程中使锥形瓶内溶液溅出,则测得的结果将会________ (填“偏大”、“偏小”或“不变”,下同);若滴定后发现滴定管尖嘴处还挂有一滴标准液,则测得的结果________ 。
(4)有同学分析实验过程,认为实验结果可能存在较大误差,除了未做防护,维生素C可能被氧化导致误差以外,也有可能是因为______________ 。
测定原理:
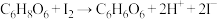
(1)实验用品及试剂:
试剂:
I2标准溶液一般用棕色酸式滴定管盛装,请解释原因:
(2)实验过程:
A.润洗后装好标准碘溶液、赶气泡、调零待用
B.用蒸馏水洗净所需仪器
C.用20mL移液管向锥形瓶中移入20.00mL待测橙汁
D.检查滴定管是否漏液
E.左手控制滴定管的活塞开关,右手摇动锥形瓶,眼睛注视锥形瓶,直到滴定终点。
F.向待测液中滴入2滴指示剂
①滴定操作的正确顺序是
②滴定中消耗标准碘溶液体积是15.00mL,则此橙汁中维生素C的含量是

(3)问题讨论:
若摇动过程中使锥形瓶内溶液溅出,则测得的结果将会
(4)有同学分析实验过程,认为实验结果可能存在较大误差,除了未做防护,维生素C可能被氧化导致误差以外,也有可能是因为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】二氧化氯(ClO2)是一种绿色消毒剂,常温常压下为黄绿色气体,易溶于水。常见的化学合成方法有氧化法和还原法。
(1)过硫酸盐氧化法:用原料亚氯酸钠(NaClO2)和过硫酸钠(Na2S2O8)直接反应,操作简单,同时可得到副产品Na2SO4。
制备时发生反应的离子方程式为___________ 。
(2)盐酸还原法:此法制得的二氧化氯消毒液中常含有ClO2和Cl2两种主要成分。为测定某二氧化氯消毒液中ClO2的浓度,进行如下实验:
量取5.00mL二氧化氯消毒液于锥形瓶中,加蒸馏水稀释到25.00mL,再向其中加入过量KI溶液,充分振荡;用0.10mol/LNa2S2O3标准溶液滴定至浅黄色后,加入指示剂,继续滴定至终点,消耗Na2S2O3标准溶液5.50mL;加入稀H2SO4调节溶液pH=3,再用0.10mol/LNa2S2O3标准溶液滴定,滴至浅黄色时加入指示剂,继续滴定至终点,第二次滴定消耗Na2S2O3溶液20.00mL。
已知:2ClO2+2KI=2KClO2+I2
KClO2+4KI+2H2SO4=KCl+2K2SO4+2I2+2H2O
2Na2S2O3+I2=Na2S4O6+2NaI
计算该二氧化氯消毒液中ClO2的物质的量浓度___________ 。(写出计算过程)
(1)过硫酸盐氧化法:用原料亚氯酸钠(NaClO2)和过硫酸钠(Na2S2O8)直接反应,操作简单,同时可得到副产品Na2SO4。
制备时发生反应的离子方程式为
(2)盐酸还原法:此法制得的二氧化氯消毒液中常含有ClO2和Cl2两种主要成分。为测定某二氧化氯消毒液中ClO2的浓度,进行如下实验:
量取5.00mL二氧化氯消毒液于锥形瓶中,加蒸馏水稀释到25.00mL,再向其中加入过量KI溶液,充分振荡;用0.10mol/LNa2S2O3标准溶液滴定至浅黄色后,加入指示剂,继续滴定至终点,消耗Na2S2O3标准溶液5.50mL;加入稀H2SO4调节溶液pH=3,再用0.10mol/LNa2S2O3标准溶液滴定,滴至浅黄色时加入指示剂,继续滴定至终点,第二次滴定消耗Na2S2O3溶液20.00mL。
已知:2ClO2+2KI=2KClO2+I2
KClO2+4KI+2H2SO4=KCl+2K2SO4+2I2+2H2O
2Na2S2O3+I2=Na2S4O6+2NaI
计算该二氧化氯消毒液中ClO2的物质的量浓度
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】某学习小组为了探究 的电离情况,进行了如下实验。回答下列问题:
的电离情况,进行了如下实验。回答下列问题:
【实验一】测定醋酸溶液的浓度。
用 溶液滴定
溶液滴定 未知浓度的
未知浓度的 溶液。4次滴定所消耗NaOH溶液的体积如下:
溶液。4次滴定所消耗NaOH溶液的体积如下:
(1)该滴定选择的指示剂为___________(填序号)
(2)计算该醋酸溶液的物质的量的浓度为___________ mol∙L−1。
(3)25℃时,当滴入NaOH溶液至pH=7时,溶液中各离子浓度的大小顺序为___________ 。
【实验二】探究浓度对 电离程度的影响。用pH计测定25℃不同浓度醋酸溶液的pH,结果如下:
电离程度的影响。用pH计测定25℃不同浓度醋酸溶液的pH,结果如下:
(4)25℃时,第②组溶液中,由水电离出的
___________ 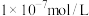 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(5)根据表中第④组数据,该温度下醋酸的电离平衡常数 约为
约为 ,计算a=
,计算a=___________ (保留3位有效数字,忽略水的电离)。
 的电离情况,进行了如下实验。回答下列问题:
的电离情况,进行了如下实验。回答下列问题:【实验一】测定醋酸溶液的浓度。
用
 溶液滴定
溶液滴定 未知浓度的
未知浓度的 溶液。4次滴定所消耗NaOH溶液的体积如下:
溶液。4次滴定所消耗NaOH溶液的体积如下:| 实验次数 | 1 | 2 | 3 | 4 |
| 消耗NaOH溶液的体积/mL | 20.02 | 20.00 | 18.40 | 19.98 |
(1)该滴定选择的指示剂为___________(填序号)
| A.甲基橙 | B.甲基红 | C.石蕊 | D.酚酞 |
(3)25℃时,当滴入NaOH溶液至pH=7时,溶液中各离子浓度的大小顺序为
【实验二】探究浓度对
 电离程度的影响。用pH计测定25℃不同浓度醋酸溶液的pH,结果如下:
电离程度的影响。用pH计测定25℃不同浓度醋酸溶液的pH,结果如下:| 组别 | ① | ② | ③ | ④ | ⑤ |
浓度/( ) ) | 0.0010 | 0.0100 | 0.0200 | 0.1000 | 0.2000 |
| pH | 3.88 | 3.38 | 3.23 | 2.88 | 2.83 |

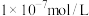 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(5)根据表中第④组数据,该温度下醋酸的电离平衡常数
 约为
约为 ,计算a=
,计算a=
您最近一年使用:0次



