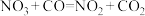下列有关有效碰撞理论和活化能的认识,正确的是
| A.增大反应物浓度,可增大单位体积内活化分子的百分数从而使有效碰撞次数增大 |
| B.有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子的百分数,从而使反应速率增大 |
| C.催化剂不影响活化能但能增大单位体积内活化分子百分数,从而增大反应速率 |
| D.H+和OH-的反应活化能接近于零,反应几乎在瞬间完成 |
更新时间:2021-12-01 22:46:55
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】一定条件下N2(g)、O2(g)反应生成NO(g)的能量关系如图所示,下列说法错误的是
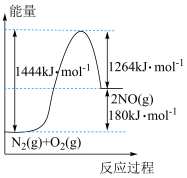

A.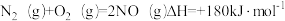 |
| B.该反应中反应物分子的每次碰撞都为有效碰撞 |
| C.正反应的活化能大于逆反应的活化能 |
| D.使用催化剂可增加单位时间内NO的产量 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】合成氨反应为:N2(g)+3H2(g) 2NH3(g) △H=−92.4 kJ∙mol−1。对于合成氨反应,下列有关说法正确的是
2NH3(g) △H=−92.4 kJ∙mol−1。对于合成氨反应,下列有关说法正确的是
 2NH3(g) △H=−92.4 kJ∙mol−1。对于合成氨反应,下列有关说法正确的是
2NH3(g) △H=−92.4 kJ∙mol−1。对于合成氨反应,下列有关说法正确的是| A.反应的ΔS>0 |
| B.反应的ΔH=6E(N−H) −E(N≡N) −3E(H−H)(E表示键能) |
| C.使用催化剂能改变反应途径,降低反应的活化能 |
| D.升高温度,正反应速率减小,逆反应速率增大,反应逆向进行 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】在密闭容器中进行反应: 。下列说法错误的是
。下列说法错误的是
 。下列说法错误的是
。下列说法错误的是| A.升高温度,增加反应物分子中活化分子的百分数 |
| B.降低温度,降低反应物分子的能量 |
| C.增大H2的浓度,单位体积内活化分子数增加 |
| D.增大压强,单位体积内活化分子百分数增加 |
您最近一年使用:0次
【推荐2】金属插入CH4的C—H键形成高氧化态过渡金属化合物的反应频繁出现在光分解作用、金属有机化学等领域,如图是CH4与Zr形成过渡金属化合物的过程。下列说法不正确的是( )
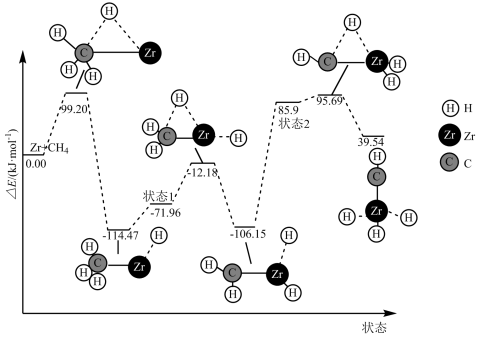

| A.整个反应快慢,由CH2—Zr···H2→状态2反应决定 |
| B.Zr+CH4→CH—Zr···H3 ΔH=-39.54 kJ·mol-1 |
| C.在中间产物中CH3—Zr···H状态最稳定 |
| D.Zr+CH4→CH3—Zr···H活化能为99.20 kJ·mol-1 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】我们把能够发生化学反应的碰撞叫做有效碰撞;发生有效碰撞的分子必须具有足够的能量,这种分子叫做活化分子;活化分子具有的平均能量与反应物分子具有的平均能量之差,叫做反应的活化能。下列说法不正确 的是
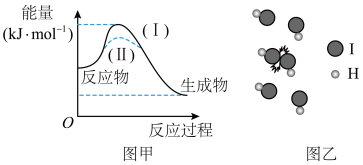

| A.图甲中曲线Ⅱ可以表示催化剂降低了反应的活化能 |
| B.图乙中HI分子发生了有效碰撞 |
| C.盐酸和氢氧化钠溶液的反应活化能接近于零 |
| D.增大反应物浓度,单位体积内活化分子数增多,单位时间内有效碰撞次数增加 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】以 为催化剂的光热化学循环分解
为催化剂的光热化学循环分解 反应为温室气体减排提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图所示:
反应为温室气体减排提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图所示:

下列说法不正确的是( )
 为催化剂的光热化学循环分解
为催化剂的光热化学循环分解 反应为温室气体减排提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图所示:
反应为温室气体减排提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图所示:
下列说法不正确的是( )
| A.过程①中钛氧键断裂会吸收能量 |
| B.该反应中,光能和热能转化为化学能 |
C.使用 作为催化剂可以降低反应的活化能,从而提高化学反应速率 作为催化剂可以降低反应的活化能,从而提高化学反应速率 |
D. 分解反应的热化学方程式为 分解反应的热化学方程式为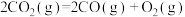  |
您最近一年使用:0次

 。反应历程中,M为中间产物。其它条件相同时,下列说法错误的是
。反应历程中,M为中间产物。其它条件相同时,下列说法错误的是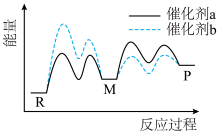

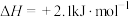 ,则灰锡更稳定,且常温常压下为灰锡状态
,则灰锡更稳定,且常温常压下为灰锡状态 且一定条件下能自发进行的化学反应,其
且一定条件下能自发进行的化学反应,其