催化剂a和b均能催化反应 。反应历程中,M为中间产物。其它条件相同时,下列说法错误的是
。反应历程中,M为中间产物。其它条件相同时,下列说法错误的是
 。反应历程中,M为中间产物。其它条件相同时,下列说法错误的是
。反应历程中,M为中间产物。其它条件相同时,下列说法错误的是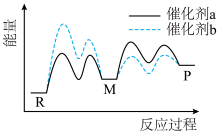
| A.使用催化剂a和b,反应历程都分4步进行 |
| B.反应达平衡后,升高温度,P的浓度增大 |
| C.使用催化剂b时,反应体系更快达到平衡 |
| D.使用催化剂a时,反应过程中M所能达到的最高浓度更大 |
更新时间:2024-05-20 12:42:36
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】对化学反应速率和平衡的研究具有十分重要的意义,下列认识正确的是
| A.用冰箱冷藏食物,能使其永远不腐败变质 |
| B.尾气转化催化剂可以完全消除汽车尾气污染 |
| C.调整反应条件无法使可逆反应正向进行到底 |
| D.化学反应速率越快可逆反应正向进行的程度越大 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】利用铜-铈氧化物(xCuO·yCeO2,Ce是活泼金属)催化氧化可除去H2中少量CO,催化氧化过程中Cu、Ce的化合价均发生变化,可能的机理如图。下列说法错误的是
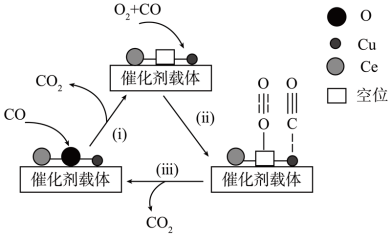

A.反应(i)中 、 、 化合价均升高 化合价均升高 |
B.铜-铈氧化物降低了反应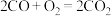 的活化能 的活化能 |
C.若用 参与反应,一段时间后, 参与反应,一段时间后, 可能出现在铜铈氧化物中 可能出现在铜铈氧化物中 |
| D.温度过高,催化剂的催化活性可能下降 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】下列说法正确的是
| A.活化分子间所发生的碰撞即为有效碰撞 |
| B.能够发生有效碰撞的分子叫做活化分子,活化分子具有的平均能量叫活化能 |
| C.增大反应物浓度,可增大单位体积内活化分子的百分数,从而使反应速率增大 |
| D.升高温度能使化学反应速率增大,是因为增加了反应物中活化分子的百分数 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】下列有关有效碰撞理论和活化能的认识,不正确的是
| A.增大压强(对于气体反应),单位体积活化分子数增大,增加了碰撞频率,故反应速率增大 |
| B.温度升高,分子动能增加,活化分子百分数增大,增加了碰撞频率,故反应速率增大 |
| C.选用适当的催化剂,降低活化能,活化分子百分数增加,故反应速率增大 |
| D.增大反应物浓度,使活化分子的百分数增大,碰撞频率增加,故反应速率增大 |
您最近一年使用:0次
【推荐1】在含 (过二硫酸根)和
(过二硫酸根)和 的溶液中,发生反应:
的溶液中,发生反应: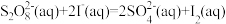 ,其分解机理及反应过程中的能量变化如图所示:
,其分解机理及反应过程中的能量变化如图所示:
 (过二硫酸根)和
(过二硫酸根)和 的溶液中,发生反应:
的溶液中,发生反应: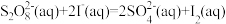 ,其分解机理及反应过程中的能量变化如图所示:
,其分解机理及反应过程中的能量变化如图所示:
| A.步骤②决定总反应的速率 |
| B.步骤①是吸热过程,步骤②是放热过程 |
C.由反应机理可以看出, 是中间产物 是中间产物 |
| D.反应中S元素不参与电子转移 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】中国科学家使用三元Ni-Fe-V催化剂,通过电催化实现了在温和的条件下人工固氮,电极上的催化机理如图所示。下列说法不正确的是

A.①②③中均断开N原子间的π键,形成 σ键 σ键 |
B.电催化过程的电极反应: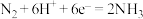 |
C.该电极上可能发生生成 的反应 的反应 |
| D.三元Ni-Fe-V催化剂可降低固氮反应的活化能 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】高温下,某反应达平衡,平衡常数K= ,恒容时,温度升高,H2浓度减小,下列说法
,恒容时,温度升高,H2浓度减小,下列说法正确 的是( )
 ,恒容时,温度升高,H2浓度减小,下列说法
,恒容时,温度升高,H2浓度减小,下列说法| A.该反应的焓变为正值 |
| B.恒温恒容下,增大压强,H2浓度一定减小 |
| C.升高温度,逆反应速率增大,正反应速率减小 |
D.该反应的化学方程式为CO+H2O CO2+H2 CO2+H2 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】对已经达到化学平衡状态的下列反应2X(g)+Y2(g)⇌Z(g),ΔH<0,降低温度时,对反应产生的影响是( )
| A.v逆减小,v正增大,平衡正向移动 |
| B.v正、v逆都增大,平衡正向移动 |
| C.v逆增大,v正减小,平衡逆向移动 |
| D.v正、v逆都减小,平衡正向移动 |
您最近一年使用:0次

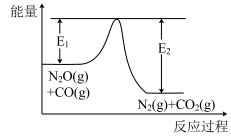
 反应过程中的能量变化如图所示,下列说法正确的是
反应过程中的能量变化如图所示,下列说法正确的是