有5瓶白色固体试剂,分别是BaCl2、NaOH、Na2SO4、(NH4)2SO4、无水CuSO4,现只提供蒸馏水,通过下面的步骤就可以鉴别它们。请填写下列空白:
(1)各取适量固体试剂分别加入5支试管中,加入适量蒸馏水,振荡试管,观察到5种固体全部溶解,1支试管中得到蓝色溶液,被检出物质的化学式是___________ 。
(2)分别取四种未检出的溶液,往其中加入上述已检出的溶液,观察到1支试管中有白色沉淀生成,则被检出物质的化学式是___________ ,相应的离子方程式是___________ ;另1支试管中有蓝色沉淀生成,则被检出物质的化学式是___________ ,相应的离子方程式是___________ 。
(3)取(2)中产生蓝色沉淀的原无色溶液,分别加入尚未检出的最后两溶液中,并加热,有刺激性气味气体产生的原未知液是___________ 。
(1)各取适量固体试剂分别加入5支试管中,加入适量蒸馏水,振荡试管,观察到5种固体全部溶解,1支试管中得到蓝色溶液,被检出物质的化学式是
(2)分别取四种未检出的溶液,往其中加入上述已检出的溶液,观察到1支试管中有白色沉淀生成,则被检出物质的化学式是
(3)取(2)中产生蓝色沉淀的原无色溶液,分别加入尚未检出的最后两溶液中,并加热,有刺激性气味气体产生的原未知液是
更新时间:2021-12-02 17:11:20
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】化学小组欲从含CuCl2、NaCl及少量K2SO4的混合溶液中分离出CuCl2和NaCl,设计实验流程如下:

已知:氯化钠、氯化钾在不同温度下的溶解度如表所示:
回答下列问题:
(1)试剂甲、乙分别是______ 。
(2)向滤渣中加入试剂丙后发生反应的离子方程式是______ 。
(3)操作1的名称是_____ 。
(4)操作2包括蒸发结晶、过滤等过程。实验时需在结晶后趁热完成过滤的目的是_____ ,过滤时应首先进行的操作是______ 。
(5)取操作2所得氯化钠晶体少许溶于酒精,得乳白色液体,用一束可见光照射液体,若在入射光的侧面观察到_______ ,则证明所得液体为胶体。

已知:氯化钠、氯化钾在不同温度下的溶解度如表所示:
| 0 | 20 | 40 | 60 | 80 | 100 | ||
| 溶解度/g | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
| KCl | 27.6 | 34.0 | 40.0 | 45.5 | 51.1 | 56.7 | |
回答下列问题:
(1)试剂甲、乙分别是
(2)向滤渣中加入试剂丙后发生反应的离子方程式是
(3)操作1的名称是
(4)操作2包括蒸发结晶、过滤等过程。实验时需在结晶后趁热完成过滤的目的是
(5)取操作2所得氯化钠晶体少许溶于酒精,得乳白色液体,用一束可见光照射液体,若在入射光的侧面观察到
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】物质A~L有如图转化关系,其中A为用途广泛的金属,其合金是制造飞机和宇宙飞船的理想材料,D、E为气体单质。已知一般情况下,难溶性氢氧化物在加热条件下会分解为对应的氧化物和水。试回答下列问题。
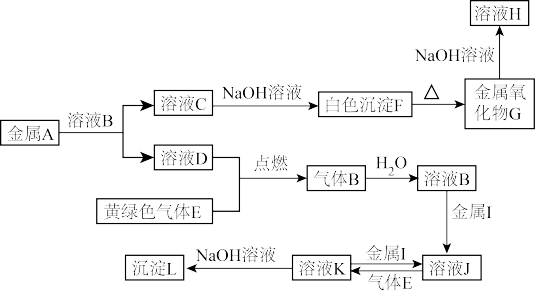
(1)金属A为___________ ,(填写化学式,下同)气体B为___________ ,沉淀L为___________ 。
(2)写出G→H的离子方程式:___________ 。
(3)写出J→K的离子方程式:___________ 。
(4)检验溶液H中的金属阳离子的方法是___________ 。
(5)向200 mL 3 mol·L-1溶液K中加入60 g铁、铜混合物(铁和铜的物质的量之比为1∶1),充分反应后过滤,所得滤液中溶质的物质的量为___________ 。

(1)金属A为
(2)写出G→H的离子方程式:
(3)写出J→K的离子方程式:
(4)检验溶液H中的金属阳离子的方法是
(5)向200 mL 3 mol·L-1溶液K中加入60 g铁、铜混合物(铁和铜的物质的量之比为1∶1),充分反应后过滤,所得滤液中溶质的物质的量为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】以硫铁矿(主要成分为FeS2,还有少量CuS、SiO2等杂质)为原料制备绿矾晶体FeSO4•7H2O的工艺流程如下:

(1)硫铁矿的主要成分FeS2中铁元素化合价为___________ ,第③步混合物分离的方法是___________ 。
(2)“酸浸”过程,矿渣中的Fe2O3与稀H2SO4反应的离子方程式:___________ 。
(3)烟气中的SO2会污染环境,可用足量氢氧化钠溶液吸收,写出该反应的离子方程式:___________ 。
(4)用铁粉还原后的混合物分离后的固体中,除了铁和铜外还有的成分是___________ (写化学式)。
(5)燃料细菌脱硫法是用氧化亚铁硫杆菌(T.f)对硫铁矿进行催化脱硫,同时得到FeSO4溶液。其过程如图所示:

已知总反应为:FeS2 + 14Fe3+ + 8H2O=2 +15Fe2+ + 16H+。写出过程II反应的离子方程式:
+15Fe2+ + 16H+。写出过程II反应的离子方程式:___________ 。

(1)硫铁矿的主要成分FeS2中铁元素化合价为
(2)“酸浸”过程,矿渣中的Fe2O3与稀H2SO4反应的离子方程式:
(3)烟气中的SO2会污染环境,可用足量氢氧化钠溶液吸收,写出该反应的离子方程式:
(4)用铁粉还原后的混合物分离后的固体中,除了铁和铜外还有的成分是
(5)燃料细菌脱硫法是用氧化亚铁硫杆菌(T.f)对硫铁矿进行催化脱硫,同时得到FeSO4溶液。其过程如图所示:

已知总反应为:FeS2 + 14Fe3+ + 8H2O=2
 +15Fe2+ + 16H+。写出过程II反应的离子方程式:
+15Fe2+ + 16H+。写出过程II反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】有一无色透明溶液,欲确定是否含有下列离子:K+、Mg2+、Al3+、Fe2+、Ba2+、NO3-、SO42-、Cl-、I-、HCO3-。取该溶液进行实验:
由此判断:
(1)溶液中肯定不存在的离子是___________ ,溶液中肯定存在的离子是____________ 。
(2)请设计实验验证其中可能存在的阴离子的方法(写明操作、现象、结论):_______ 。
| 实验步骤 | 实验现象 |
| ①取少量该溶液,测定溶液pH | pH=0 |
| ②取少量该溶液加热浓缩,加Cu片和浓H2SO4,加热 | 有无色气体产生,气体遇空气变成红棕色 |
| ③取少量该溶液,加少量BaCl2溶液 | 有白色沉淀 |
| ④取③中上层清液,加足量AgNO3溶液 | 有白色沉淀,且不溶于稀HNO3 |
| ⑤取少量该溶液,加NaOH溶液 | 有白色沉淀,NaOH过量时沉淀部分溶解 |
(1)溶液中肯定不存在的离子是
(2)请设计实验验证其中可能存在的阴离子的方法(写明操作、现象、结论):
您最近一年使用:0次
【推荐2】某无色溶液100mL,其中可能含Fe3+、Al3+、Na+、Mg2+、Cu2+、NH4+、K+、CO32-、SO42-等离子中的几种,为分析其成分,取此溶液分别进行了四个实验,其操作和有关现象如图所示。

请回答下列问题:
(1)焰色反应是___ (填“物理”或“化学”)变化;实验③中产生的无色无味气体是___ (填化学式)。
(2)原溶液中一定存在的离子有___ ;一定不存在的离子有___ 。
(3)若溶液中K+物质的量为0.04mol,则c(Na+)=___ mol/L。

请回答下列问题:
(1)焰色反应是
(2)原溶液中一定存在的离子有
(3)若溶液中K+物质的量为0.04mol,则c(Na+)=
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】某校化学兴趣小组同学猜想自来水中可能含有大量Cu2+、Ca2+、Mg2+和某些阴离子,从而进行了三组实验:
①取适量自来水于试管中,滴加足量的NaOH溶液,产生白色沉淀;
②过滤后取滤液于试管中,滴加足量的Na2CO3溶液,又有白色沉淀生成;
③另取适量自来水于试管中,滴加足量稀硝酸后再滴加AgNO3溶液,也产生白色沉淀。
请回答以下问题:
(1)不用做实验就可排除的离子是________ 。
(2)通过实验可初步确定自来水中含有大量Ca2+、Mg2+;判断依据的离子方程式有__________ 、__________ 。
(3)自来水中所含阴离子可以确定有_________ ,理由是__________ (用离子方程式表示)。
(4)确定实验②中滴加的Na2CO3溶液已过量的检验方法是__________ 。
①取适量自来水于试管中,滴加足量的NaOH溶液,产生白色沉淀;
②过滤后取滤液于试管中,滴加足量的Na2CO3溶液,又有白色沉淀生成;
③另取适量自来水于试管中,滴加足量稀硝酸后再滴加AgNO3溶液,也产生白色沉淀。
请回答以下问题:
(1)不用做实验就可排除的离子是
(2)通过实验可初步确定自来水中含有大量Ca2+、Mg2+;判断依据的离子方程式有
(3)自来水中所含阴离子可以确定有
(4)确定实验②中滴加的Na2CO3溶液已过量的检验方法是
您最近一年使用:0次
【推荐1】将两种化合物一起溶于水得到一种无色透明溶液,溶液中含有下列离子中的某些离子: 、
、 、
、 、
、 、
、 、
、 、
、 和
和 ,取该溶液进行如下实验:
,取该溶液进行如下实验:
Ⅰ.取少量溶液滴入紫色石蕊试液,溶液呈蓝色。
Ⅱ.取少许溶液滴入 溶液,无白色沉淀产生。
溶液,无白色沉淀产生。
Ⅲ.取少许溶液先滴加硝酸再加 溶液,产生白色沉淀。
溶液,产生白色沉淀。
Ⅳ.再取少许原溶液滴入少量 溶液,有白色沉淀产生。
溶液,有白色沉淀产生。
(1)根据以上现象判断,原溶液中肯定不存在的离子是___________ ;肯定存在的离子是___________ 。
(2)写出实验Ⅲ中可能发生反应的离子方程式:Ⅲ.___________ ,___________ 。
(3)如溶液中各种离子的浓度相等,确定溶液中___________ (填有或无) ,判断依据是
,判断依据是___________ 。
 、
、 、
、 、
、 、
、 、
、 、
、 和
和 ,取该溶液进行如下实验:
,取该溶液进行如下实验:Ⅰ.取少量溶液滴入紫色石蕊试液,溶液呈蓝色。
Ⅱ.取少许溶液滴入
 溶液,无白色沉淀产生。
溶液,无白色沉淀产生。Ⅲ.取少许溶液先滴加硝酸再加
 溶液,产生白色沉淀。
溶液,产生白色沉淀。Ⅳ.再取少许原溶液滴入少量
 溶液,有白色沉淀产生。
溶液,有白色沉淀产生。(1)根据以上现象判断,原溶液中肯定不存在的离子是
(2)写出实验Ⅲ中可能发生反应的离子方程式:Ⅲ.
(3)如溶液中各种离子的浓度相等,确定溶液中
 ,判断依据是
,判断依据是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】氧化亚砜(SOCl2)是一种液态化合物,沸点77℃,在农药、医药行业中用途广泛。SOCl2遇水剧烈反应,液面上产生白雾,并有刺激性气味的气体产生。实验室合成原理为:SO2+Cl2+SCl2 2SOCl2(SCl2常温常压下为樱桃红色液体),其装置图如图。请回答下列问题:
2SOCl2(SCl2常温常压下为樱桃红色液体),其装置图如图。请回答下列问题:

(1)仪器X的名称是___ ,仪器C的作用除了吸收Cl2和SO2外,还具有的作用___ 。
(2)戊是贮气装置,则E中的溶液是___ 。
(3)若缺少装置乙和丁,三颈烧瓶会发生的主要副反应的化学方程式___ 。(任写一个)
(4)有关实验叙述不正确的是___ 。(填选项序号)
a.X、Y内的试剂是70%H2SO4和Na2SO3固体
b.活性炭的作用是作催化剂
e.冷凝管B也可以用于蒸馏
d.三颈烧瓶温度过高时应适当冷却以提高SOCl2的产率
(5)少量SOCl2加入5mL1mol/LAgNO3溶液有白色沉淀生成,该白色沉淀成分是___ (写化学式)。
(6)①蒸干MgCl2溶液不能得到无水MgCl2,用SOCl2与MgCl2·6H2O混合加热。可得到无水MgCl2写出反应的化学方程式___ 。
②SOCl2与FeCl3·6H2O混合加热不宜制取无水FeCl3,是因为该方案可能发生副反应使产品不纯。
某同学设计了如下实验方案判断副反应的可能性:
ⅰ.取少量FeCl3·6H2O于试管中,加入足量SOCl2,振荡使两种物质充分反应;
ⅱ.往上述试管中加水溶解,取溶解后的溶液少许于两支试管,进行实验验证,完成表格内容。(供选试剂:AgNO3溶液、稀盐酸、稀HNO3、酸性KMnO4溶液、BaCl2溶液、K3[Fe(CN)6]溶液、溴水)
 2SOCl2(SCl2常温常压下为樱桃红色液体),其装置图如图。请回答下列问题:
2SOCl2(SCl2常温常压下为樱桃红色液体),其装置图如图。请回答下列问题:
(1)仪器X的名称是
(2)戊是贮气装置,则E中的溶液是
(3)若缺少装置乙和丁,三颈烧瓶会发生的主要副反应的化学方程式
(4)有关实验叙述不正确的是
a.X、Y内的试剂是70%H2SO4和Na2SO3固体
b.活性炭的作用是作催化剂
e.冷凝管B也可以用于蒸馏
d.三颈烧瓶温度过高时应适当冷却以提高SOCl2的产率
(5)少量SOCl2加入5mL1mol/LAgNO3溶液有白色沉淀生成,该白色沉淀成分是
(6)①蒸干MgCl2溶液不能得到无水MgCl2,用SOCl2与MgCl2·6H2O混合加热。可得到无水MgCl2写出反应的化学方程式
②SOCl2与FeCl3·6H2O混合加热不宜制取无水FeCl3,是因为该方案可能发生副反应使产品不纯。
某同学设计了如下实验方案判断副反应的可能性:
ⅰ.取少量FeCl3·6H2O于试管中,加入足量SOCl2,振荡使两种物质充分反应;
ⅱ.往上述试管中加水溶解,取溶解后的溶液少许于两支试管,进行实验验证,完成表格内容。(供选试剂:AgNO3溶液、稀盐酸、稀HNO3、酸性KMnO4溶液、BaCl2溶液、K3[Fe(CN)6]溶液、溴水)
| 方案 | 操作 | 现象 | 结论 |
| 方案一 | 往一支试管中滴加 | 若有白色沉淀生成 | 则发生了上述副反应 |
| 方案二 | 往另一支试管中滴加 | 则没有发生上述副反应 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】某溶液由Ba2+、Fe3+、Na+、Cu2+、SO42-、Cl-、AlO2-、CO32-中的若干种离子组成。取适量该溶液进行如下实验:①向其中加入过量盐酸,有气体生成,并得到无色透明溶液;②向①所得的溶液中加入过量氨水,产生白色沉淀,过滤;③向②所得的滤液中加入过量氢氧化钡溶液,产生白色沉淀,过滤;④向③所得的滤液中加入过量稀硝酸,再加入硝酸银溶液,产生白色沉淀。根据上述实验回答下列问题:
(1)原溶液中一定不存在的离子是__________________________ ;
(2)原溶液中可能存在的离子是________ 。为检验该离子是否存在,应补充的实验为(写出实验过程):____ 。
(1)原溶液中一定不存在的离子是
(2)原溶液中可能存在的离子是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】现有M、N两种溶液,其中M溶液为无色溶液。经测定这两种溶液共含有下列10种离子:Cl-、Na+、K+、 、OH-、Fe2+、
、OH-、Fe2+、 、H+、
、H+、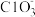 、
、 。
。
(1)完成下列表格中实验①的结论和实验②的实验内容以及现象:
(2)已知:酸性环境中,Fe2+被 氧化,生成Fe3+和NO气体,请写出对应的离子方程式:
氧化,生成Fe3+和NO气体,请写出对应的离子方程式:___________ ;结合(1)可判断出, 存在于
存在于 ___________ 溶液中。
(3)为了验证M溶液中是否含有Cl-,还需要补充的实验操作是(请用简单的文字说明)___________ 。
 、OH-、Fe2+、
、OH-、Fe2+、 、H+、
、H+、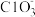 、
、 。
。(1)完成下列表格中实验①的结论和实验②的实验内容以及现象:
| 实验内容以及现象 | 结论 |
| ①取少量N溶液滴加足量的硝酸钡溶液,无沉淀产生 | |
| ② | 确定M溶液中含有Na+,不含K+ |
| ③用pH试纸检测M溶液,pH试纸呈蓝色 |
 氧化,生成Fe3+和NO气体,请写出对应的离子方程式:
氧化,生成Fe3+和NO气体,请写出对应的离子方程式: 存在于
存在于 (3)为了验证M溶液中是否含有Cl-,还需要补充的实验操作是(请用简单的文字说明)
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】加碘食盐中加入的KIO3是一种白色晶体,常温下很稳定,加热至560℃才开始分解。工业生产碘酸钾的流程如下:

(1)已知“反应”的化学方程式为6I2+11KClO3+3H2O=6KH(IO3)2+5KCl+3Cl2↑,用单线桥标出该反应中电子转移的方向和数目______ 。
(2)由KClO3固体配制0.050 mol·L-1 KClO3溶液,下列操作可能使所配KClO3溶液浓度偏小的是______ (填写字母)。

a.稀释和转移用的烧杯、玻璃棒未洗涤
b.如图所示,定容时俯视容量瓶的刻度线
c.配溶液前容量瓶中有少量蒸馏水
d.加水时超过刻度线,用胶头滴管吸出多余的液体
(3)某加碘盐用KI代替KIO3,请设计检验加碘盐中含有I-的实验方案:______ 。实验中可供选择的试剂:淀粉溶液、FeCl3溶液。
(4)为测定某加碘盐中碘元素的含量,实验过程为:称取加碘盐20.00 g于锥形瓶中,加水溶解,向其中加入过量的KI溶液和适量的稀硫酸,充分反应,用0.0010 mol·L-1 Na2S2O3溶液滴定,恰好完全反应时消耗Na2S2O3溶液体积为30.00 mL。计算20.00 g该加碘盐中碘元素的质量______ (质量单位以mg记,并写出计算过程)。测定过程中发生的反应为:5KI+KIO3+3H2SO4=3I2+3K2SO4+3H2O;I2+2Na2S2O3=2NaI+Na2S4O6

(1)已知“反应”的化学方程式为6I2+11KClO3+3H2O=6KH(IO3)2+5KCl+3Cl2↑,用单线桥标出该反应中电子转移的方向和数目
(2)由KClO3固体配制0.050 mol·L-1 KClO3溶液,下列操作可能使所配KClO3溶液浓度偏小的是

a.稀释和转移用的烧杯、玻璃棒未洗涤
b.如图所示,定容时俯视容量瓶的刻度线
c.配溶液前容量瓶中有少量蒸馏水
d.加水时超过刻度线,用胶头滴管吸出多余的液体
(3)某加碘盐用KI代替KIO3,请设计检验加碘盐中含有I-的实验方案:
(4)为测定某加碘盐中碘元素的含量,实验过程为:称取加碘盐20.00 g于锥形瓶中,加水溶解,向其中加入过量的KI溶液和适量的稀硫酸,充分反应,用0.0010 mol·L-1 Na2S2O3溶液滴定,恰好完全反应时消耗Na2S2O3溶液体积为30.00 mL。计算20.00 g该加碘盐中碘元素的质量
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】天然气中常混有 ,现用如下方法测定天然气中
,现用如下方法测定天然气中 的含量。反应中涉及的方程式有:
的含量。反应中涉及的方程式有:
①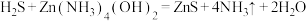
②
③
(1)反应①中, 体现
体现_______ (选填“酸性”“氧化性”或“还原性”)。
采用以下方法测定 的含量。
的含量。
步骤I:将1L天然气中的 溶于水并进行反应①,配制成500mL溶液。
溶于水并进行反应①,配制成500mL溶液。
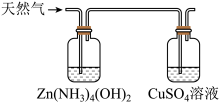
步骤II:加入0.001mol的I2(过量)使ZnS完全转化为ZnI2,加入淀粉溶液作为指示剂,用0.1mol·L-1的 滴定过量的I2,做几组平行实验,平均消耗15.00mL。
滴定过量的I2,做几组平行实验,平均消耗15.00mL。
(2)①滴定达到终点的现象为:溶液由_______ 色变_______ 色,且半分钟不恢复原色。
②根据条件计算天然气中H2S的含量为_______ mg·L-1。
③若在步骤I收集H2S的过程中,有少量硫化氢进入 溶液中,则测得H2S的含量
溶液中,则测得H2S的含量_______ (选填“偏高”“偏低”或“无影响”)。
(3)假设在反应②中,碘单质全部转化为易溶于水的ZnI2,如何检验体系中的I-_______ 。
(4)利用硫碘循环处理H2S的方法如图所示:
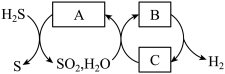
写出上述流程中A、B、C的化学式。
A:_______ ;B:_______ ;C:_______ 。
 ,现用如下方法测定天然气中
,现用如下方法测定天然气中 的含量。反应中涉及的方程式有:
的含量。反应中涉及的方程式有:①
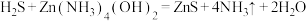
②

③

(1)反应①中,
 体现
体现采用以下方法测定
 的含量。
的含量。步骤I:将1L天然气中的
 溶于水并进行反应①,配制成500mL溶液。
溶于水并进行反应①,配制成500mL溶液。
步骤II:加入0.001mol的I2(过量)使ZnS完全转化为ZnI2,加入淀粉溶液作为指示剂,用0.1mol·L-1的
 滴定过量的I2,做几组平行实验,平均消耗15.00mL。
滴定过量的I2,做几组平行实验,平均消耗15.00mL。(2)①滴定达到终点的现象为:溶液由
②根据条件计算天然气中H2S的含量为
③若在步骤I收集H2S的过程中,有少量硫化氢进入
 溶液中,则测得H2S的含量
溶液中,则测得H2S的含量(3)假设在反应②中,碘单质全部转化为易溶于水的ZnI2,如何检验体系中的I-
(4)利用硫碘循环处理H2S的方法如图所示:

写出上述流程中A、B、C的化学式。
A:
您最近一年使用:0次



