2020年突如其来的“新冠肺炎”使人们认识到日常杀菌消毒的重要性。氯气、漂白液、漂白粉都是生活中常用的含氯消毒剂。家庭中常常使用的消毒剂主要是84消毒液,可以说化学让生活更美好。下图为84消毒液说明书。请回答下列问题。
(1)84消毒液的有效氯指的是每升含氯消毒剂的氧化能力(得失电子数)相当于多少克Cl2的氧化能力(Cl均转化为Cl-)。若该84消毒液商品的有效氯按53.25g·L-1计算,该消毒液的NaClO的物质的量浓度是___________ 。
(2)常温下用烧碱溶液吸收Cl2制备84消毒液。写出该反应的离子方程式:___________ ,若将Cl2通入热的烧碱溶液中,可以得到NaCl、NaClO和NaClO3的混合液。当混合液中Cl-和ClO 的个数比为15∶2时,混合液中ClO-和ClO
的个数比为15∶2时,混合液中ClO-和ClO 的个数比为
的个数比为___________ ,从氧化还原角度分析Cl2表现了___________ 性。
(3)家庭用84消毒液用法强调,为家庭物品消毒时,要做适当的稀释,喷洒后也不要急于用清水擦拭,要浸泡,这样效果会更好,原因是(用离子方程式表示)___________ (已知酸性:H2CO3>HClO>HCO )。
)。
(4)游泳池水的消毒多用漂粉精,但酸碱性对漂粉精的消毒效果影响明显。池水碱性过强,杀毒作用会___________ (填“增强”或“减弱”)。
(5)Cl2可直接用于杀菌消毒,但常常把氯气制成漂白粉、84消毒液,主要目的是___________。
 | 药品名称 | 84消毒液 |
| 主要成分 | NaClO,有效氯含量50.00g·L-1~60.00g·L-1 | |
| 注意事项 | 不可与其他洗涤剂或消毒液混合使用 | |
| 用法用量 | 稀释后浸泡或洗刷白色衣物、浴缸等1∶200水溶液 餐饮具、瓜果等1∶100水溶液 |
(2)常温下用烧碱溶液吸收Cl2制备84消毒液。写出该反应的离子方程式:
 的个数比为15∶2时,混合液中ClO-和ClO
的个数比为15∶2时,混合液中ClO-和ClO 的个数比为
的个数比为(3)家庭用84消毒液用法强调,为家庭物品消毒时,要做适当的稀释,喷洒后也不要急于用清水擦拭,要浸泡,这样效果会更好,原因是(用离子方程式表示)
 )。
)。(4)游泳池水的消毒多用漂粉精,但酸碱性对漂粉精的消毒效果影响明显。池水碱性过强,杀毒作用会
(5)Cl2可直接用于杀菌消毒,但常常把氯气制成漂白粉、84消毒液,主要目的是___________。
| A.增强漂白能力和消毒作用 |
| B.使它转化为较稳定物质,便于保存和运输 |
| C.使它转化为较易溶于水的物质 |
| D.提高氯的质量分数,有利于漂白、消毒 |
更新时间:2021-12-21 11:10:02
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】中科院官方微信中科院之于2017年3月9日发表《一个“网红”的转化-灰霾专题》,提出灰霾细颗粒物的成因,部分分析如下图所示。
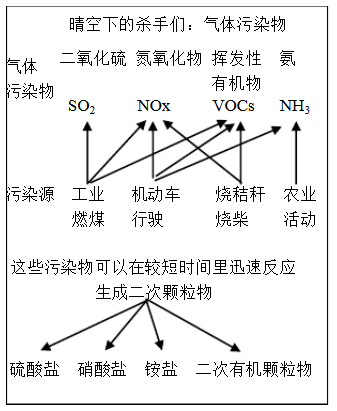
(1)根据上图信息可以看出,下列哪种污染源不产生NOx_________ .
A.工业燃煤 B.机动车尾气 C.烧秸秆 D.农业活动
(2)若某地空气潮湿,且空气含有的大气污染物主要是SO2、NH3,根据上图中所举的“SO2 SO32-
SO32- 盐
盐 SO42-
SO42- 盐”的流程,请写出该地形成二次颗粒物硫酸盐的化学反应方程式:
盐”的流程,请写出该地形成二次颗粒物硫酸盐的化学反应方程式:_____________ 。
(3)当前频繁出现的雾霾天气与汽车尾气的排放有一定的关系,为了减少污染,可尝试使用汽车尾气净化装置,其原理如图所示。

写出净化过程中的总化学方程式:________
(4)将装有amLNO和NO2混合气体的集气瓶倒立在水槽中,然后鼓入一定量O2,最终集气瓶里面剩余气体体积为bmL,则集气瓶内所得HNO3的物质的量浓度为______ mol/L(不考虑集气瓶内硝酸扩散到水槽中,设气体摩尔体积为Vm)。

(1)根据上图信息可以看出,下列哪种污染源不产生NOx
A.工业燃煤 B.机动车尾气 C.烧秸秆 D.农业活动
(2)若某地空气潮湿,且空气含有的大气污染物主要是SO2、NH3,根据上图中所举的“SO2
 SO32-
SO32- 盐
盐 SO42-
SO42- 盐”的流程,请写出该地形成二次颗粒物硫酸盐的化学反应方程式:
盐”的流程,请写出该地形成二次颗粒物硫酸盐的化学反应方程式:(3)当前频繁出现的雾霾天气与汽车尾气的排放有一定的关系,为了减少污染,可尝试使用汽车尾气净化装置,其原理如图所示。

写出净化过程中的总化学方程式:
(4)将装有amLNO和NO2混合气体的集气瓶倒立在水槽中,然后鼓入一定量O2,最终集气瓶里面剩余气体体积为bmL,则集气瓶内所得HNO3的物质的量浓度为
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】氯及其化合物在生产、生活中都有重要的应用,实验室要配制一定物质的量浓度的稀盐酸。
(1)如图是某市售盐酸试剂瓶标签上的部分数据,则该盐酸的物质的量浓度___________ 
(2)某同学需要240mL1.00mol/L的稀盐酸,用该市售盐酸试剂稀释配制,请回答下列问题:
①通过计算可知,雷要用量筒量取该市售盐酸试剂___________ mL。配制过程需要的仪器有:量筒、烧杯、玻璃棒、胶头滴管、______________ 。
②用该市售盐酸试剂配制1.00mol/L的稀盐酸过程中,其正确的操作顺序是(字母表示,每个字母只能用一次)__________________ 。
A.用胶头滴管加水至溶液凹液面与刻度线相切
B.用量筒准确量取浓盐酸的体积,沿内壁加入盛有少量水(约80mL)的烧杯中,用玻璃棒慢慢搅动
C.将已冷却的盐酸溶液沿玻璃棒注入选定的容量瓶中
D.将容量瓶盖紧,颠倒摇匀
E.继续往容量瓶内小心加水,直到液面接近刻度1-2cm处
F.用蒸馏水洗涤烧杯和玻璃棒2-3次,并将每次洗涤液都注入容量瓶中
③下列配制过程中导致溶液浓度偏低的是___________ 。
A.定容时俯视刻度线
B.配制前,容量瓶中有少量蒸馏水
C.配制时,盐酸溶液未冷却直接定容
D.定容摇匀后液面低于刻度线,又加蒸馏水至刻度线
E.向容量瓶中转移溶液时不慎有液滴洒在容量瓶外面
(3)取任意体积该市售盐酸试剂,下列物理量不随所取体积的多少而变化的是___________ 。若取出10mL该市售盐酸试剂加水稀释100倍,稀释前后保持不变的是___________ 。
A.溶液中HCl的物质的量 B.溶液中 的浓度
的浓度
C.溶液中 分子的数目 D.溶液的密度
分子的数目 D.溶液的密度
(1)如图是某市售盐酸试剂瓶标签上的部分数据,则该盐酸的物质的量浓度

| 化学式:HCl 相对分子质量:36.5 密度:1.18g/mL 质量分数:36.5% 符合 GB622-89 |
(2)某同学需要240mL1.00mol/L的稀盐酸,用该市售盐酸试剂稀释配制,请回答下列问题:
①通过计算可知,雷要用量筒量取该市售盐酸试剂
②用该市售盐酸试剂配制1.00mol/L的稀盐酸过程中,其正确的操作顺序是(字母表示,每个字母只能用一次)
A.用胶头滴管加水至溶液凹液面与刻度线相切
B.用量筒准确量取浓盐酸的体积,沿内壁加入盛有少量水(约80mL)的烧杯中,用玻璃棒慢慢搅动
C.将已冷却的盐酸溶液沿玻璃棒注入选定的容量瓶中
D.将容量瓶盖紧,颠倒摇匀
E.继续往容量瓶内小心加水,直到液面接近刻度1-2cm处
F.用蒸馏水洗涤烧杯和玻璃棒2-3次,并将每次洗涤液都注入容量瓶中
③下列配制过程中导致溶液浓度偏低的是
A.定容时俯视刻度线
B.配制前,容量瓶中有少量蒸馏水
C.配制时,盐酸溶液未冷却直接定容
D.定容摇匀后液面低于刻度线,又加蒸馏水至刻度线
E.向容量瓶中转移溶液时不慎有液滴洒在容量瓶外面
(3)取任意体积该市售盐酸试剂,下列物理量不随所取体积的多少而变化的是
A.溶液中HCl的物质的量 B.溶液中
 的浓度
的浓度C.溶液中
 分子的数目 D.溶液的密度
分子的数目 D.溶液的密度
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】已知下列十种物质:(l) H2O (2) Cu (3) NO (4) Fe2O3 (5)稀硫酸(6)氢氧化钡(7)饱和FeCl3溶液(8)氨水(9)稀硝酸(10)硫酸铝,根据上述提供的物质,回答下列问题:
(1)属于纯净物的是________ (填序号),属于电解质的是________ (填序号)。
(2)上述物质间发生的某反应的离子方程式为H++OH-=H2O,则该反应的化学方程式为__________ 。
(3)实验室制备少量Fe(OH)3胶体所用的物质有_____ (填序号),反应的离子方程式为____________ 。
(4)实验室配制245mL 0.5mol/L的硫酸铝溶液,需要称取的溶质的质量为_____ g,从配制好的溶液中取出l00mL,其中含有的SO42-的数目为_______ (设NA为阿伏伽德罗常数的值)。
(1)属于纯净物的是
(2)上述物质间发生的某反应的离子方程式为H++OH-=H2O,则该反应的化学方程式为
(3)实验室制备少量Fe(OH)3胶体所用的物质有
(4)实验室配制245mL 0.5mol/L的硫酸铝溶液,需要称取的溶质的质量为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】工业上通过氮气和氢气反应合成氨,氨经一系列反应可以得到硝酸。反应如下图所示:
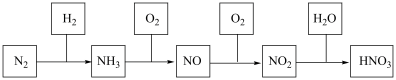
请回答:
(1)合成氨反应的化学方程式是___________ 。
(2)NH3与O2制取NO的化学反应方程式___________ 。
(3)工业制硝酸时尾气中含有NO、NO2,可用以下方法吸收:
①水吸收法。结合化学方程式说明用水吸收NO2的缺陷___________ 。
② NaOH溶液吸收法。发生的反应有:
2NaOH + NO + NO2 = 2NaNO2+ H2O
NaOH + NO2 →___________ + NaNO2 + H2O(填化学式,不需要配平方程式)
③用不同浓度的NaOH溶液吸收NO2含量不同的尾气,关系如下图:

(α 表示尾气NO、NO2中NO2的含量)
根据上图可知___________ (填字母)。
a. NaOH溶液浓度越大,氮氧化物的吸收率越大
b.NO2含量越大,氮氧化物的吸收率越大
(4)NOx含量的测定:
将VL气样通入适量酸化的H2O2溶液中,使NOx完全被氧化为NO ,加水稀释至100 mL。量取25mL该溶液,加入V1mL c1 mol·L−1 FeSO4溶液(过量),充分反应后,用c2 mol·L−1 K2Cr2O7溶液和剩余的Fe2+恰好反应,消耗V2mL。测定过程中发生下列反应:3Fe2++NO
,加水稀释至100 mL。量取25mL该溶液,加入V1mL c1 mol·L−1 FeSO4溶液(过量),充分反应后,用c2 mol·L−1 K2Cr2O7溶液和剩余的Fe2+恰好反应,消耗V2mL。测定过程中发生下列反应:3Fe2++NO +4H+=NO↑+3Fe3++2H2O、Cr2O
+4H+=NO↑+3Fe3++2H2O、Cr2O + 6Fe2+ +14H+ =2Cr3+ +6Fe3++7H2O。
+ 6Fe2+ +14H+ =2Cr3+ +6Fe3++7H2O。
①写出NO被H2O2氧化为NO 的离子方程式:
的离子方程式:___________ 。
②气样中NOx折合成NO的含量为___________ mg·L−1。

请回答:
(1)合成氨反应的化学方程式是
(2)NH3与O2制取NO的化学反应方程式
(3)工业制硝酸时尾气中含有NO、NO2,可用以下方法吸收:
①水吸收法。结合化学方程式说明用水吸收NO2的缺陷
② NaOH溶液吸收法。发生的反应有:
2NaOH + NO + NO2 = 2NaNO2+ H2O
NaOH + NO2 →
③用不同浓度的NaOH溶液吸收NO2含量不同的尾气,关系如下图:

(α 表示尾气NO、NO2中NO2的含量)
根据上图可知
a. NaOH溶液浓度越大,氮氧化物的吸收率越大
b.NO2含量越大,氮氧化物的吸收率越大
(4)NOx含量的测定:
将VL气样通入适量酸化的H2O2溶液中,使NOx完全被氧化为NO
 ,加水稀释至100 mL。量取25mL该溶液,加入V1mL c1 mol·L−1 FeSO4溶液(过量),充分反应后,用c2 mol·L−1 K2Cr2O7溶液和剩余的Fe2+恰好反应,消耗V2mL。测定过程中发生下列反应:3Fe2++NO
,加水稀释至100 mL。量取25mL该溶液,加入V1mL c1 mol·L−1 FeSO4溶液(过量),充分反应后,用c2 mol·L−1 K2Cr2O7溶液和剩余的Fe2+恰好反应,消耗V2mL。测定过程中发生下列反应:3Fe2++NO +4H+=NO↑+3Fe3++2H2O、Cr2O
+4H+=NO↑+3Fe3++2H2O、Cr2O + 6Fe2+ +14H+ =2Cr3+ +6Fe3++7H2O。
+ 6Fe2+ +14H+ =2Cr3+ +6Fe3++7H2O。①写出NO被H2O2氧化为NO
 的离子方程式:
的离子方程式:②气样中NOx折合成NO的含量为
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】实验室使用稀硫酸和 溶解铜片,该反应的化学方程式为
溶解铜片,该反应的化学方程式为_______ 。
 溶解铜片,该反应的化学方程式为
溶解铜片,该反应的化学方程式为
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】电化学理论在钢铁防腐、废水处理中有着重要应用价值。请按要求回答下列问题。
(1)在潮湿的空气里,钢铁易发生电化学腐蚀,其中正极的电极反应式为_______ 。
(2)在海洋工程上,通常用铝锌镉合金(金属性:Al Zn
Zn Cd)保护海底钢铁设施,其原理如图所示:
Cd)保护海底钢铁设施,其原理如图所示:
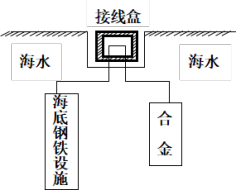
其负极电极反应式为_______ ;在实际应用中,用铝合金而不选用纯铝,纯铝不能很好地起到保护作用,其原因是_______ 。
(3)工业上处理含 的酸性工业废水常用以下方法:
的酸性工业废水常用以下方法:
a.往工业废水里加入适量的NaCl,搅拌均匀
b.用Fe作电极进行电解,一段时间后有Cr(OH)3和Fe(OH)3沉淀产生
c.过滤回收沉淀,废水达到排放标准
①电解时阳极反应式:_______ 。
② 转变成Cr3+的离子方程式:
转变成Cr3+的离子方程式:_______ 。
③解释Cr(OH)3、Fe(OH)3沉淀的产生原因:_______ 。
④能否用Cu电极来代替Fe电极?_______ (填“能”或“不能”),简述理由:_______ 。
(1)在潮湿的空气里,钢铁易发生电化学腐蚀,其中正极的电极反应式为
(2)在海洋工程上,通常用铝锌镉合金(金属性:Al
 Zn
Zn Cd)保护海底钢铁设施,其原理如图所示:
Cd)保护海底钢铁设施,其原理如图所示:
其负极电极反应式为
(3)工业上处理含
 的酸性工业废水常用以下方法:
的酸性工业废水常用以下方法:a.往工业废水里加入适量的NaCl,搅拌均匀
b.用Fe作电极进行电解,一段时间后有Cr(OH)3和Fe(OH)3沉淀产生
c.过滤回收沉淀,废水达到排放标准
①电解时阳极反应式:
②
 转变成Cr3+的离子方程式:
转变成Cr3+的离子方程式:③解释Cr(OH)3、Fe(OH)3沉淀的产生原因:
④能否用Cu电极来代替Fe电极?
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】海水中存在大量的氯元素,通过对海水中氯元素的提取,可制取单质氯气,也可制取氯的多种氧化物。回答下列问题:
(1)氯气可溶于水形成氯水,溶液中含氯元素的微粒有_______ 种。氯水中属于弱电解质的是_______ (除水外,写化学式),写出该物质的电离方程式_______ 。
(2)常温时,氯气可与 NaOH 溶液反应制取漂白液(俗称 84 消毒液),漂白液的有效成分是_______ 。84 消毒液可作家庭消毒剂,但不能与洁厕精(主要成分是盐酸)混合使用,原因是_______ (用离子反应方程式表示)。
(3)一定条件下,氯气与 NaOH 溶液充分反应后溶液中的 ClO3-和 ClO-的个数比为 1:2,则溶液中 ClO-和 Cl-的个数比为_______ 。
(4)Cl2O 是一种酸性氧化物,常温时是一种棕黄色气体,有毒。制备原理如下: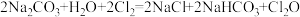 ,请用双线桥表示出该反应中电子转移的方向和数目
,请用双线桥表示出该反应中电子转移的方向和数目_______ 。制备过程中可用NaOH溶液除去剩余Cl2O,写出该反应的化学反应方程式_______ 。
(1)氯气可溶于水形成氯水,溶液中含氯元素的微粒有
(2)常温时,氯气可与 NaOH 溶液反应制取漂白液(俗称 84 消毒液),漂白液的有效成分是
(3)一定条件下,氯气与 NaOH 溶液充分反应后溶液中的 ClO3-和 ClO-的个数比为 1:2,则溶液中 ClO-和 Cl-的个数比为
(4)Cl2O 是一种酸性氧化物,常温时是一种棕黄色气体,有毒。制备原理如下:
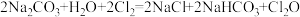 ,请用双线桥表示出该反应中电子转移的方向和数目
,请用双线桥表示出该反应中电子转移的方向和数目
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】富马酸亚铁(结构简式为 ,M=170)常用于治疗缺铁性贫血,也可作食品营养强化剂。某化学兴趣小组用富马酸(HOOCCH=CHCOOH)和FeSO4制备富马酸亚铁,并对其纯度进行测定,过程如下:
,M=170)常用于治疗缺铁性贫血,也可作食品营养强化剂。某化学兴趣小组用富马酸(HOOCCH=CHCOOH)和FeSO4制备富马酸亚铁,并对其纯度进行测定,过程如下:

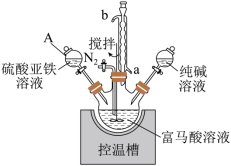
取0.4000g样品置于250mL锥形瓶中,加入15.00mL硫酸,加热溶解后冷却,再加入50.00mL新煮沸过的冷水和2滴邻二氮菲指示液,此时溶液星红色;立即用0.1000mol/L的硫酸铈铵(NH4)2Ce(SO4)3标准液滴定(还原产物为Ce3+),滴定终点溶液变为浅蓝色。平行测定三次,平均消耗22.00mL标准液。
滴定过程的硫酸铈铵[(NH4)2Ce(SO4)3]标准液应装入
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
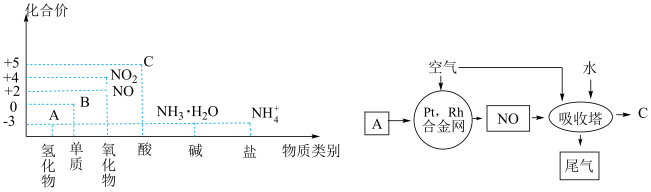
【推荐3】下面左图为氮元素的“价-类”二维图,下面右图为工业上以A为原料制备C的工艺流程图。___________ ;
(2)铜和足量的C的稀溶液反应方程式___________ ,反应中C表现的性质为___________ (填字母)。
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
(3)写出 与稀盐酸反应的离子方程式:
与稀盐酸反应的离子方程式:___________ 。
(4)写出在合金网的催化作用下A与空气中的氧气反应得到NO的化学方程式:___________ 。
(5)上述工艺流程的“尾气”中主要含有氮氧化物(NO、 )。
)。
①若5mol A恰好能将6mol由NO和 组成的混合气体完全转化为B和水,则混合气体中
组成的混合气体完全转化为B和水,则混合气体中
___________ 。
②在酸性条件下用酸性高锰酸钾溶液吸收NO,产物为 和
和 ,则该反应中
,则该反应中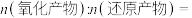
___________
(6)氮的另一种氢化物的分子式为 若将
若将 看作二元碱,则其与
看作二元碱,则其与 形成的酸式盐化学式为
形成的酸式盐化学式为___________ 。
(2)铜和足量的C的稀溶液反应方程式
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
(3)写出
 与稀盐酸反应的离子方程式:
与稀盐酸反应的离子方程式:(4)写出在合金网的催化作用下A与空气中的氧气反应得到NO的化学方程式:
(5)上述工艺流程的“尾气”中主要含有氮氧化物(NO、
 )。
)。①若5mol A恰好能将6mol由NO和
 组成的混合气体完全转化为B和水,则混合气体中
组成的混合气体完全转化为B和水,则混合气体中
②在酸性条件下用酸性高锰酸钾溶液吸收NO,产物为
 和
和 ,则该反应中
,则该反应中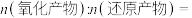
(6)氮的另一种氢化物的分子式为
 若将
若将 看作二元碱,则其与
看作二元碱,则其与 形成的酸式盐化学式为
形成的酸式盐化学式为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】现有以下物质:①石灰乳; ②氯气; ③CaCO3固体; ④熔融KHSO4; ⑤Fe(OH)3胶体; ⑥铜; ⑦CO2; ⑧稀醋酸。
(1)上述物质中属于非电解质的是___________ ;(填序号)
(2)写出④的电离方程式是________________________ ;
(3)向①中通入②制漂白粉,发生反应的化学方程式是____________________________ 。漂白粉的有效成分是________________________ (填化学式);
(4)在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮沸至溶液呈_______ 色,停止加热即制得Fe(OH)3胶体。写出制备物质⑤的化学方程式:________________ 。
(1)上述物质中属于非电解质的是
(2)写出④的电离方程式是
(3)向①中通入②制漂白粉,发生反应的化学方程式是
(4)在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮沸至溶液呈
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】按要求回答下列问题:
(1)画出氯离子的结构示意图_____ 。
(2)写出漂白粉有效成分的化学式_____ 。
(3)19g 某二价金属氯化物 ACl2 中含有 0.4 molCl-,则 ACl2 的摩尔质量为_____ g/mol。
(4)写出一水合氨的电离方程式_________ 。
(5)表示“氯碱工业”的离子方程式_________ 。
(6)NH4HCO3 溶液中加入过量 NaOH 溶液的离子方程式为_________ 。
(1)画出氯离子的结构示意图
(2)写出漂白粉有效成分的化学式
(3)19g 某二价金属氯化物 ACl2 中含有 0.4 molCl-,则 ACl2 的摩尔质量为
(4)写出一水合氨的电离方程式
(5)表示“氯碱工业”的离子方程式
(6)NH4HCO3 溶液中加入过量 NaOH 溶液的离子方程式为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】(1)室温时,在下列物质中:①Na ②Cl2 ③Na2O ④FeCl2溶液 ⑤NaHCO3 ⑥蔗糖 ⑦NH3 ⑧NaCl晶体 ⑨HClO ⑩ Fe(OH)2
属于碱性氧化物的是(用序号填写,下同)_______ ,属于酸的是_____ ,属于强电解质的是______ ,属于非电解质的是_______ ,能导电的是________ 。
(2)Na2O2与CO2的反应化学方程式__________ ;
(3)向硫酸氢钠溶液中逐滴加入氢氧化钡溶液到中性,请写出发生反应的离子方程式______ 。
(4)制取漂白粉的反应化学方程式_________ ;其有效成分是_______ ;
属于碱性氧化物的是(用序号填写,下同)
(2)Na2O2与CO2的反应化学方程式
(3)向硫酸氢钠溶液中逐滴加入氢氧化钡溶液到中性,请写出发生反应的离子方程式
(4)制取漂白粉的反应化学方程式
您最近半年使用:0次



