新型冠状病毒肺炎疫情是2020年最大的公共安全事件,当前的重要工作是“外防输入,内防反弹”。依据研究,含氯消毒剂可以有效灭活新型冠状病毒,为阻断新型冠状病毒疫情做出了巨大贡献。
I.实验室用如图所示装置制备NaClO溶液
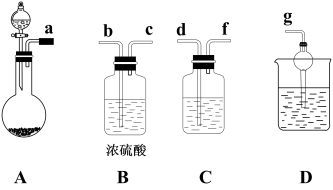
(1)A中盛装浓盐酸的装置的名称是___________ 。
(2)装置A发生的反应为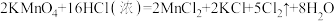 ,用单线桥表示该反应电子转移情况
,用单线桥表示该反应电子转移情况___________ 。
(3)写出按上图装置制备NaClO溶液,你认为最简易的装置其连接顺序为___________ (填接口字母,仪器可重复使用,也可以不选)。写出该实验中制备NaClO溶液的离子方程式:_____
II.某同学购买了一瓶“84消毒液”,并查阅相关资料和消毒液包装说明得到如下信息:“84消毒液”:含25%NaClO、1000mL、密度1.192g/cm3,稀释100倍(体积比)后使用。该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480mL含NaClO质量分数为25%的消毒液。请你补全下面的实验方案:
(4)仪器:托盘天平、烧杯、量筒、___________ 、胶头滴管、玻璃棒…
(5)在配制过程中,其他操作都是正确的,下列操作会引起浓度偏高的是_______(填序号)。
(6)某同学取10mL该“84消毒液”,稀释后用于消毒,则稀释后的溶液中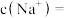
_____  。
。
I.实验室用如图所示装置制备NaClO溶液

(1)A中盛装浓盐酸的装置的名称是
(2)装置A发生的反应为
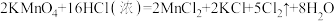 ,用单线桥表示该反应电子转移情况
,用单线桥表示该反应电子转移情况(3)写出按上图装置制备NaClO溶液,你认为最简易的装置其连接顺序为
II.某同学购买了一瓶“84消毒液”,并查阅相关资料和消毒液包装说明得到如下信息:“84消毒液”:含25%NaClO、1000mL、密度1.192g/cm3,稀释100倍(体积比)后使用。该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480mL含NaClO质量分数为25%的消毒液。请你补全下面的实验方案:
(4)仪器:托盘天平、烧杯、量筒、
(5)在配制过程中,其他操作都是正确的,下列操作会引起浓度偏高的是_______(填序号)。
| A.未洗涤烧杯和玻璃棒 |
| B.定容时仰视视刻度线 |
| C.未冷却到室温就将溶液转移到容量瓶并定容 |
| D.配制前容量瓶内有少量蒸馏水 |
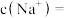
 。
。
更新时间:2022-01-16 09:08:28
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】下表给出了六种元素的相关信息,其中A、B、C、D、E、F为短周期元素,原子序数依次递增。
根据上述信息填空:
(1)元素D在元素周期表中的位置是____________ 。E基态原子的电子排布式_______________________ 。
(2)化合物甲是一种强氧化剂,由元素D和E组成,写出一种甲的用途:_______________ ,
书写化合物甲与BD2的反应式并标出电子转移情况:_______________ 。
(3)化合物乙由元素D和F组成,气体乙与A2F反应的化学方程式是______________ 。化合物乙的危害_______________________ 。(写一种)
| 元素 | 相关信息 |
| A | 单质为密度最小的气体 |
| B | 元素最高正价与最低负价之和为0 |
| D | 可形成D2、D3两种气态单质,其中一单质是保护地球地表环境的重要屏障 |
| E | 存在质量数为23,中子数为12的核素 |
| F | 单质F为淡黄色固体 |
(1)元素D在元素周期表中的位置是
(2)化合物甲是一种强氧化剂,由元素D和E组成,写出一种甲的用途:
书写化合物甲与BD2的反应式并标出电子转移情况:
(3)化合物乙由元素D和F组成,气体乙与A2F反应的化学方程式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】A、B、C、D、E、X是中学常见的无机物,存在如图转化关系(部分生成物和反应条件略去),回答下列问题。
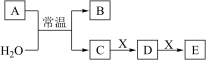
(1)若A为金属单质,C俗称烧碱。
①A的化学式为_____ ,A与H2O反应的化学方程式为_____ 。
②若X为无色无味的气体,且能使澄清石灰水变浑浊,写出E的化学式:_____ ,写出C与E反应的离子方程式:_____ 。100mL1mol•L-1C的溶液吸收1.68L气体X(标准状况下)后,溶液中的溶质为_____ (填化学式),取出10mL,此种溶液,加水稀释至1L,则溶液中c(Na+)=_____ mol•L-1。
(2)若A为淡黄色固体,则每生成3.2g气体B,反应中转移的电子的物质的量为_____ mol,用双线桥法标明A与H2O反应时电子转移的方向和数目:_____ 。

(1)若A为金属单质,C俗称烧碱。
①A的化学式为
②若X为无色无味的气体,且能使澄清石灰水变浑浊,写出E的化学式:
(2)若A为淡黄色固体,则每生成3.2g气体B,反应中转移的电子的物质的量为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】氯元素的单质、化合物在实验室以及生活生产中都有着重要的应用。
I.下图是实验室制取无水氯化铜的装置图,已知干燥管E中盛有碱石灰。请完成下列问题:

(1)写出装置A烧瓶中发生反应的化学方程式,并用单线桥表示电子转移的方向和数目_________
(2)玻璃管D中发生反应的化学方程式是_________
(3)装置E中碱石灰的作用是_________
II.亚氯酸钠(NaClO2)是一种高效氧化、杀菌及漂白剂,以NaClO3为原料生产亚氯酸钠的工艺流程如下:
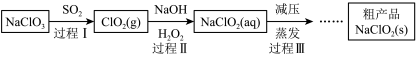
(4)过程I在生成ClO2的同时,还会得到另一种常见的盐,请写出其化学方程式_________
(5)过程I中常伴有少量Cl2生成。结合下表信息,设计实验方案除去ClO2中的Cl2_________
(6)过程Ⅱ中H2O2的作用是___________ (填“氧化剂”或“还原剂”)
(7)理论上每生成1molNaClO2 ,消耗SO2的质量是___________
(8)已知:压强越大,物质的沸点越高。NaClO2饱和溶液在38℃~60℃时析出NaClO2晶体,高于60℃时分解成NaClO3和NaCl。请根据以上信息分析:过程III采用“减压蒸发”操作的原因是_________ 。
I.下图是实验室制取无水氯化铜的装置图,已知干燥管E中盛有碱石灰。请完成下列问题:

(1)写出装置A烧瓶中发生反应的化学方程式,并用单线桥表示电子转移的方向和数目
(2)玻璃管D中发生反应的化学方程式是
(3)装置E中碱石灰的作用是
II.亚氯酸钠(NaClO2)是一种高效氧化、杀菌及漂白剂,以NaClO3为原料生产亚氯酸钠的工艺流程如下:

(4)过程I在生成ClO2的同时,还会得到另一种常见的盐,请写出其化学方程式
(5)过程I中常伴有少量Cl2生成。结合下表信息,设计实验方案除去ClO2中的Cl2
| ClO2 | Cl2 | |
| 在水中的溶解性 | 易溶 | 溶 |
| 在CCl4中的溶解性 | 难溶 | 溶 |
(7)理论上每生成1molNaClO2 ,消耗SO2的质量是
(8)已知:压强越大,物质的沸点越高。NaClO2饱和溶液在38℃~60℃时析出NaClO2晶体,高于60℃时分解成NaClO3和NaCl。请根据以上信息分析:过程III采用“减压蒸发”操作的原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】碘酸钙是动物饲料的微量元素添加剂。Ca(IO3)2·6H2O制备步骤及装置如图:
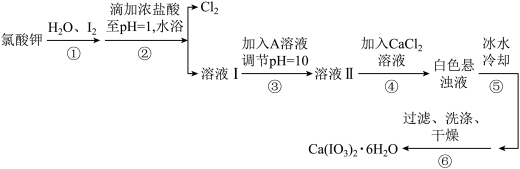
已知:冷却结晶过程中得到的产物随温度不同会带不同数目的结晶水,如下表:
请回答:

(1)d烧杯内装的溶液是_______ ;作用是_______ 。
(2)步骤②碘反应完全的现象是_______ 。
(3)步骤⑥,洗涤后检验沉淀洗涤是否干净的方法是_______ 。
(4)下列说法不正确的是_______。
(5)产品纯度分析:已知2 +I2=
+I2= +2I-,可采用如下方法测定产品中Ca(IO3)2·6H2O纯度。从下列选项中选择最佳操作并排序
+2I-,可采用如下方法测定产品中Ca(IO3)2·6H2O纯度。从下列选项中选择最佳操作并排序_______ 。
准确称取0.600g样品→(_______)→(_______)→(_______)→(_______)→计算
a.加水微热溶解试样,冷却后转移到250ml容量瓶,用水稀释至刻度,摇匀得试液
b.加入1:1高氯酸微热溶解试样,冷却后转移到250ml容量瓶,用水稀释至刻度,摇匀得试液
c.加50ml水,用浓度为0.100mol/L Na2S2O3标准溶液滴定至浅黄色
d.加50ml水,用浓度为0.100mol/L Na2S2O3标准溶液滴定至浅黄色,加入2ml淀粉溶液
e.准确量取50.00ml试液于250ml碘量瓶(如图)中,加入3g碘化钾,盖上瓶塞,暗处反应3min
f.准确量取50.00ml试液于250ml锥形瓶中,加入3g碘化钾,暗处反应3min
g.继续用Na2S2O3标准溶液滴定,至浅黄色溶液变为无色,半分钟内不恢复,读数
h.继续用Na2S2O3标准溶液滴定,溶液蓝色消失,半分钟内不恢复,读数

已知:冷却结晶过程中得到的产物随温度不同会带不同数目的结晶水,如下表:
| 碘酸钙存在形式 | Ca(IO3)2 | Ca(IO3)2·H2O | Ca(IO3)2·6H2O |
| 稳定温度 | >57.5℃ | 32~57.5℃ | <32℃ |

(1)d烧杯内装的溶液是
(2)步骤②碘反应完全的现象是
(3)步骤⑥,洗涤后检验沉淀洗涤是否干净的方法是
(4)下列说法不正确的是_______。
| A.步骤②,水浴加热时,冷凝管下口出现固体未作处理会使产率偏低 |
| B.步骤③,可加入K2CO3溶液调节pH |
| C.步骤⑤,未使用冰水浴,会使产率偏高 |
| D.步骤⑥,洗涤沉淀时可先用冰水洗涤,再用无水乙醇洗涤,后晾干 |
 +I2=
+I2= +2I-,可采用如下方法测定产品中Ca(IO3)2·6H2O纯度。从下列选项中选择最佳操作并排序
+2I-,可采用如下方法测定产品中Ca(IO3)2·6H2O纯度。从下列选项中选择最佳操作并排序准确称取0.600g样品→(_______)→(_______)→(_______)→(_______)→计算
a.加水微热溶解试样,冷却后转移到250ml容量瓶,用水稀释至刻度,摇匀得试液
b.加入1:1高氯酸微热溶解试样,冷却后转移到250ml容量瓶,用水稀释至刻度,摇匀得试液
c.加50ml水,用浓度为0.100mol/L Na2S2O3标准溶液滴定至浅黄色
d.加50ml水,用浓度为0.100mol/L Na2S2O3标准溶液滴定至浅黄色,加入2ml淀粉溶液
e.准确量取50.00ml试液于250ml碘量瓶(如图)中,加入3g碘化钾,盖上瓶塞,暗处反应3min

f.准确量取50.00ml试液于250ml锥形瓶中,加入3g碘化钾,暗处反应3min
g.继续用Na2S2O3标准溶液滴定,至浅黄色溶液变为无色,半分钟内不恢复,读数
h.继续用Na2S2O3标准溶液滴定,溶液蓝色消失,半分钟内不恢复,读数
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】Ⅰ.实验是化学研究的一种重要手段,现有下图所示A~G七种仪器,请根据要求填空。

(1)写出仪器名称:E_____________ ,F_____________ 。
(2)下列实验操作中用到仪器D的是_________ (选填下列选项的编号字母 )。
A.分离水和CCl4的混合物 B.分离水和酒精的混合物 C.分离水和泥砂的混合物
Ⅱ.某课外兴趣小组需要200 mL1 mol/L的Na2CO3溶液,请回答下列问题:
(1)配制溶液所需仪器及药品:
(2)配制时,其正确的操作顺序是(用字母表示,每个操作只能用一次)______________ 。
A.将已冷却的溶液沿玻璃棒注入容量瓶中
B.用托盘天平准确称量所需Na2CO3的质量,倒入烧杯中,再加入适量水,用玻璃棒慢慢搅动,使其溶解(必要时可加热)
C.用适量水洗涤烧杯2~3次,洗涤液均注入容量瓶中,振荡
D.改用胶头滴管加水,使溶液凹液面恰好与刻度线相切
E.将容量瓶盖紧,振荡,摇匀
F.继续往容量瓶内小心加水,直到液面接近刻度1~2 cm处
(3)若出现如下情况,对所配溶液浓度将有何影响 (填“偏高”、“偏低”或“无影响”)?
没有进行C操作________ ;配制溶液时,容量瓶未干燥_________ ;定容时俯视刻度线_________ 。

(1)写出仪器名称:E
(2)下列实验操作中用到仪器D的是
A.分离水和CCl4的混合物 B.分离水和酒精的混合物 C.分离水和泥砂的混合物
Ⅱ.某课外兴趣小组需要200 mL1 mol/L的Na2CO3溶液,请回答下列问题:
(1)配制溶液所需仪器及药品:
| 应称取Na2CO3的质量 | 应选用容量瓶的规格 | 除容量瓶外还需要的其它玻璃仪器是上图中的 |
A.将已冷却的溶液沿玻璃棒注入容量瓶中
B.用托盘天平准确称量所需Na2CO3的质量,倒入烧杯中,再加入适量水,用玻璃棒慢慢搅动,使其溶解(必要时可加热)
C.用适量水洗涤烧杯2~3次,洗涤液均注入容量瓶中,振荡
D.改用胶头滴管加水,使溶液凹液面恰好与刻度线相切
E.将容量瓶盖紧,振荡,摇匀
F.继续往容量瓶内小心加水,直到液面接近刻度1~2 cm处
(3)若出现如下情况,对所配溶液浓度将有何影响 (填“偏高”、“偏低”或“无影响”)?
没有进行C操作
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某次实验需用450mL0.35mol/L的 溶液,某同学用密度为
溶液,某同学用密度为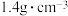 质量分数49%的
质量分数49%的 溶液进行配制,请回答下列问题:
溶液进行配制,请回答下列问题:
(1)实验需要的玻璃仪器除了烧杯、量筒、玻璃棒,还有_______ 、_______ 。
(2)计算:配制本次实验需要的稀硫酸需用量筒量取上述49%的
_______ mL。
(3)配制过程:①用量筒量取所需质量分数为49%的 溶液
溶液
②将浓硫酸缓缓注入盛有适量蒸馏水的烧杯中,边加边搅拌
③用玻璃棒引流将烧杯中的溶液转移到已经检漏的合适规格的容量瓶中
④洗涤烧杯和玻璃棒2~3次,洗涤液也注入容量瓶中,轻轻摇动容量瓶,使溶液混合均匀
⑤向容量瓶中加入蒸馏水,在距离刻度1~2cm时,改用胶头滴管加蒸馏水至刻度线
⑥盖好瓶塞,反复上下颠倒,摇匀
⑦将配制好的溶液转移至试剂瓶中待用
上述配制溶液的步骤存在缺失,缺少的步骤是_____ ,应放在步骤_____ 之前进行(填“序号”)。
(4)在横线上填写下列各种情况对所配制溶液浓度的影响(选填“偏高”、“偏低”或“无影响”)。
①所用的浓硫酸长时间放置在密封不好的容器中_______ 。
②用量筒量取浓硫酸时仰视液面_______ 。
 溶液,某同学用密度为
溶液,某同学用密度为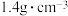 质量分数49%的
质量分数49%的 溶液进行配制,请回答下列问题:
溶液进行配制,请回答下列问题:(1)实验需要的玻璃仪器除了烧杯、量筒、玻璃棒,还有
(2)计算:配制本次实验需要的稀硫酸需用量筒量取上述49%的

(3)配制过程:①用量筒量取所需质量分数为49%的
 溶液
溶液②将浓硫酸缓缓注入盛有适量蒸馏水的烧杯中,边加边搅拌
③用玻璃棒引流将烧杯中的溶液转移到已经检漏的合适规格的容量瓶中
④洗涤烧杯和玻璃棒2~3次,洗涤液也注入容量瓶中,轻轻摇动容量瓶,使溶液混合均匀
⑤向容量瓶中加入蒸馏水,在距离刻度1~2cm时,改用胶头滴管加蒸馏水至刻度线
⑥盖好瓶塞,反复上下颠倒,摇匀
⑦将配制好的溶液转移至试剂瓶中待用
上述配制溶液的步骤存在缺失,缺少的步骤是
(4)在横线上填写下列各种情况对所配制溶液浓度的影响(选填“偏高”、“偏低”或“无影响”)。
①所用的浓硫酸长时间放置在密封不好的容器中
②用量筒量取浓硫酸时仰视液面
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】粉煤灰是燃煤产生的重要污染物,主要成分有 、
、 、
、 和
和 等物质。综合利用粉煤灰不仅能够防止环境污染,还能获得纳米
等物质。综合利用粉煤灰不仅能够防止环境污染,还能获得纳米 等重要物质。
等重要物质。
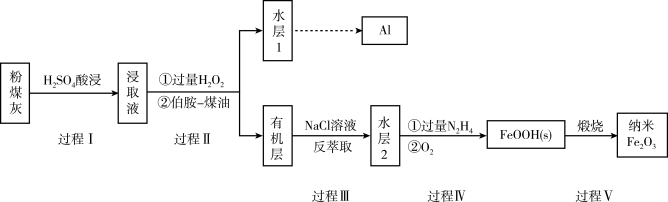
已知:
ⅰ.伯胺 能与
能与 反应的方程式如下,产物易溶于煤油:
反应的方程式如下,产物易溶于煤油: 。
。
ⅱ. 在水溶液中易与
在水溶液中易与 反应:
反应: 。
。
(1)写出过程Ⅰ中 发生反应的离子方程式:
发生反应的离子方程式:_________ 。
(2)过程Ⅱ加入过量 的作用是
的作用是_________ 。
(3)过程Ⅱ加入伯胺-煤油对浸取液进行分离,该操作的名称是_________ 。
(4)从化学平衡角度解释过程Ⅲ利用NaCl溶液进行反萃取的原理:_________ 。
(5) 具有碱性,可与
具有碱性,可与 结合生成
结合生成 。过程Ⅳ中先用过量的
。过程Ⅳ中先用过量的 将水层2中
将水层2中 转化为
转化为 并生成
并生成 ,反应的离子方程式为
,反应的离子方程式为_________ ,得到的 再被
再被 氧化为FeOOH。
氧化为FeOOH。
(6)纳米 在常压电化学法合成氨过程中起催化作用。该电解装置如图所示。
在常压电化学法合成氨过程中起催化作用。该电解装置如图所示。
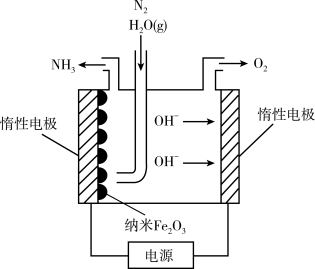
已知熔融 为电解液,
为电解液, 在阴极发生电极反应生成中间体Fe。用化学用语表示
在阴极发生电极反应生成中间体Fe。用化学用语表示 在阴极催化生成
在阴极催化生成 的反应过程。
的反应过程。
第一步:_________ ;
第二步:_________ 。
 、
、 、
、 和
和 等物质。综合利用粉煤灰不仅能够防止环境污染,还能获得纳米
等物质。综合利用粉煤灰不仅能够防止环境污染,还能获得纳米 等重要物质。
等重要物质。
已知:
ⅰ.伯胺
 能与
能与 反应的方程式如下,产物易溶于煤油:
反应的方程式如下,产物易溶于煤油: 。
。ⅱ.
 在水溶液中易与
在水溶液中易与 反应:
反应: 。
。(1)写出过程Ⅰ中
 发生反应的离子方程式:
发生反应的离子方程式:(2)过程Ⅱ加入过量
 的作用是
的作用是(3)过程Ⅱ加入伯胺-煤油对浸取液进行分离,该操作的名称是
(4)从化学平衡角度解释过程Ⅲ利用NaCl溶液进行反萃取的原理:
(5)
 具有碱性,可与
具有碱性,可与 结合生成
结合生成 。过程Ⅳ中先用过量的
。过程Ⅳ中先用过量的 将水层2中
将水层2中 转化为
转化为 并生成
并生成 ,反应的离子方程式为
,反应的离子方程式为 再被
再被 氧化为FeOOH。
氧化为FeOOH。(6)纳米
 在常压电化学法合成氨过程中起催化作用。该电解装置如图所示。
在常压电化学法合成氨过程中起催化作用。该电解装置如图所示。
已知熔融
 为电解液,
为电解液, 在阴极发生电极反应生成中间体Fe。用化学用语表示
在阴极发生电极反应生成中间体Fe。用化学用语表示 在阴极催化生成
在阴极催化生成 的反应过程。
的反应过程。第一步:
第二步:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】据公安部统计,截至2023年6月底,成都汽车保有量超过600万辆,仅次于北京,居全国第二、高密度的车辆行驶,容易引发交通事故,若车辆受到相对较大撞击,就会引起安全气囊弹出,从而保护车内乘客。叠氮化钠是汽车安全气囊内的重要填充物质。某化学兴趣小组根据工业制备叠氮化钠(NaN3)的方法在实验室设计出制备该物质的装置如下:
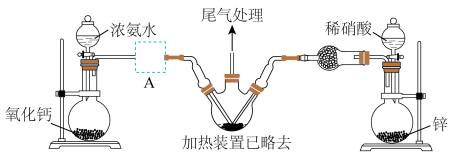
已知:ⅰ.工业上制备 的原理分两步进行:
的原理分两步进行:
①将 通入熔融状态的Na中先制得
通入熔融状态的Na中先制得 ,
,
②将 与
与 加热至
加热至 左右合成
左右合成 ,在合成过程中,易发生副反应:
,在合成过程中,易发生副反应: ;
;
ⅱ. 和
和 的性质如下表:
的性质如下表:
ⅲ. 属于危险化学药品,工业上一般用NaClO销毁剩余
属于危险化学药品,工业上一般用NaClO销毁剩余 ;
;
ⅳ. 与
与 离子反应产生鲜明的血红色,此反应非常灵敏。
离子反应产生鲜明的血红色,此反应非常灵敏。
回答下列问题:
(1)盛装浓氨水的仪器的名称是___________ 。
(2)连接好装置之后,应进行的操作是___________ 。
(3)实验室用 和稀硝酸反应制备
和稀硝酸反应制备 ,其离子方程式为
,其离子方程式为___________ 。
(4)图中虚线框处应选用的装置是___________ (填标号)。

(5)安全气囊中填充 的理由是
的理由是___________ 。
(6)在销毁多余 时会有
时会有 和
和 生成,该反应的化学方程式为
生成,该反应的化学方程式为___________ ;如何检测销毁是否彻底,请提供一种检测方法:___________ 。

已知:ⅰ.工业上制备
 的原理分两步进行:
的原理分两步进行:①将
 通入熔融状态的Na中先制得
通入熔融状态的Na中先制得 ,
,②将
 与
与 加热至
加热至 左右合成
左右合成 ,在合成过程中,易发生副反应:
,在合成过程中,易发生副反应: ;
;ⅱ.
 和
和 的性质如下表:
的性质如下表:| 物质 |  |  |
| 性质 | 白色固体,易溶于水,有一定危险性,受撞击易快速分解出一种无色、无味、无毒的气体,且有固体Na生成。 | 无色、有甜味的气体,有轻微麻醉作用,常用于医疗,有一定氧化性。 |
 属于危险化学药品,工业上一般用NaClO销毁剩余
属于危险化学药品,工业上一般用NaClO销毁剩余 ;
;ⅳ.
 与
与 离子反应产生鲜明的血红色,此反应非常灵敏。
离子反应产生鲜明的血红色,此反应非常灵敏。回答下列问题:
(1)盛装浓氨水的仪器的名称是
(2)连接好装置之后,应进行的操作是
(3)实验室用
 和稀硝酸反应制备
和稀硝酸反应制备 ,其离子方程式为
,其离子方程式为(4)图中虚线框处应选用的装置是

(5)安全气囊中填充
 的理由是
的理由是(6)在销毁多余
 时会有
时会有 和
和 生成,该反应的化学方程式为
生成,该反应的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】硫酸亚铁是一种补铁剂,某兴趣小组利用经初步处理的含有 的废液制备硫酸亚铁晶体的流程如下:
的废液制备硫酸亚铁晶体的流程如下:

(1)加入饱和 溶液后,得到白色沉淀,则操作1为
溶液后,得到白色沉淀,则操作1为___________ ,若 溶液浓度偏低可能会形成胶体,验证的方法为
溶液浓度偏低可能会形成胶体,验证的方法为___________ 。
(2)加入铁粉的作用是___________ 。
(3)测定废液中 的浓度可使用已知浓度的酸性高锰酸钾溶液,请配平以下方程式,并用单线桥法表示电子转移过程:
的浓度可使用已知浓度的酸性高锰酸钾溶液,请配平以下方程式,并用单线桥法表示电子转移过程:___________
___________ ___________
___________ ___________
___________ ___________
___________ ___________
___________ ___________
___________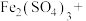 ___________
___________
(4)该兴趣小组在研究硫酸亚铁(FeSO4)热稳定性时,作出了两种假设:
①假设一:按 受热分解的方式分解,则
受热分解的方式分解,则 受热分解的化学方程式为
受热分解的化学方程式为___________ ;
②假设二:按 受热分解的方式分解,且产物中有一种碱性氧化物和两种酸性氧化物生成,则
受热分解的方式分解,且产物中有一种碱性氧化物和两种酸性氧化物生成,则 受热分解的化学方程式为
受热分解的化学方程式为___________ 。
(5) 和
和 的相互转化可用于物质含量的测定,如测定某氯化亚铜样品中CuCl的含量,流程如下:准确称取氯化亚铜样品mg,将其置于过量的
的相互转化可用于物质含量的测定,如测定某氯化亚铜样品中CuCl的含量,流程如下:准确称取氯化亚铜样品mg,将其置于过量的 溶液中,发生以下反应:
溶液中,发生以下反应: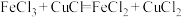 ,待固体完全溶解后,加入适量稀硫酸,用
,待固体完全溶解后,加入适量稀硫酸,用 的
的 溶液氧化反应生成的
溶液氧化反应生成的 (该条件下
(该条件下 不被氧化),消耗
不被氧化),消耗 溶液bmL,反应中
溶液bmL,反应中 被还原为
被还原为 。则样品中CuCl的质量分数为
。则样品中CuCl的质量分数为___________ 。
 的废液制备硫酸亚铁晶体的流程如下:
的废液制备硫酸亚铁晶体的流程如下:
(1)加入饱和
 溶液后,得到白色沉淀,则操作1为
溶液后,得到白色沉淀,则操作1为 溶液浓度偏低可能会形成胶体,验证的方法为
溶液浓度偏低可能会形成胶体,验证的方法为(2)加入铁粉的作用是
(3)测定废液中
 的浓度可使用已知浓度的酸性高锰酸钾溶液,请配平以下方程式,并用单线桥法表示电子转移过程:
的浓度可使用已知浓度的酸性高锰酸钾溶液,请配平以下方程式,并用单线桥法表示电子转移过程:___________
 ___________
___________ ___________
___________ ___________
___________ ___________
___________ ___________
___________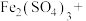 ___________
___________
(4)该兴趣小组在研究硫酸亚铁(FeSO4)热稳定性时,作出了两种假设:
①假设一:按
 受热分解的方式分解,则
受热分解的方式分解,则 受热分解的化学方程式为
受热分解的化学方程式为②假设二:按
 受热分解的方式分解,且产物中有一种碱性氧化物和两种酸性氧化物生成,则
受热分解的方式分解,且产物中有一种碱性氧化物和两种酸性氧化物生成,则 受热分解的化学方程式为
受热分解的化学方程式为(5)
 和
和 的相互转化可用于物质含量的测定,如测定某氯化亚铜样品中CuCl的含量,流程如下:准确称取氯化亚铜样品mg,将其置于过量的
的相互转化可用于物质含量的测定,如测定某氯化亚铜样品中CuCl的含量,流程如下:准确称取氯化亚铜样品mg,将其置于过量的 溶液中,发生以下反应:
溶液中,发生以下反应: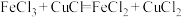 ,待固体完全溶解后,加入适量稀硫酸,用
,待固体完全溶解后,加入适量稀硫酸,用 的
的 溶液氧化反应生成的
溶液氧化反应生成的 (该条件下
(该条件下 不被氧化),消耗
不被氧化),消耗 溶液bmL,反应中
溶液bmL,反应中 被还原为
被还原为 。则样品中CuCl的质量分数为
。则样品中CuCl的质量分数为
您最近一年使用:0次



