酸碱滴定法与氧化还原滴定法均为重要的定量分析法,应用广泛。回答下列问题:
Ⅰ.酸碱中和滴定
选择酚酞作指示剂,用标准NaOH溶液测定白醋中醋酸的浓度,以检测白醋是否符合国家标准。测定过程如图所示:
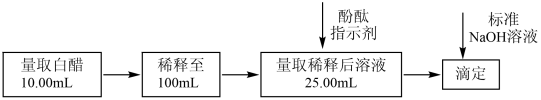
已知:国家标准规定酿造白醋中醋酸含量不得低于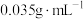 。
。
(1)①滴定达到终点时的现象是滴入半滴标准NaOH溶液后_______ 。
②某次实验滴定开始和结束时。碱式滴定管中的液面如图所示,则消耗NaOH溶液的体积为_______ mL。
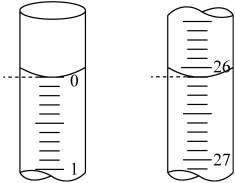
③已知实验所用标准NaOH溶液的浓度为 ,根据上述滴定结果可知该白醋
,根据上述滴定结果可知该白醋_______ (填“符合”或“不符合”)国家标准。
④下列操作中,可能使所测白醋中醋酸的浓度数值偏低的是_______ (填编号)。
A.碱式滴定管未用标准NaOH溶液润洗就直接注入标准NaOH溶液
B.滴定前盛放白醋稀溶液的锥形瓶用蒸馏水洗净后没有干燥
C.滴定过程中摇动锥形瓶时有液滴溅出
D.读取NaOH溶液体积时,开始时仰视读数,滴定结束时俯视读数
E.碱式滴定管在滴定前有气泡,滴定后气泡消失
(2)若用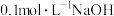 溶液分别滴定体积均为20.00 mL、浓度均为
溶液分别滴定体积均为20.00 mL、浓度均为 的盐酸和醋酸溶液,得到滴定过程中pH随加入NaOH溶液体积而变化的两条滴定曲线如图所示。
的盐酸和醋酸溶液,得到滴定过程中pH随加入NaOH溶液体积而变化的两条滴定曲线如图所示。

①滴定醋酸的曲线是_______ (填“Ⅰ”或“Ⅱ”)。
② 和
和 的关系:
的关系:
_______  (填“>”“=”或“<”)。
(填“>”“=”或“<”)。
③若25℃时, 的醋酸与
的醋酸与 的氢氧化钠溶液等体积混合显中性,则醋酸的电离常数为
的氢氧化钠溶液等体积混合显中性,则醋酸的电离常数为_______ (用含a的代数式表示)。
Ⅱ.氧化还原滴定
(3) 的纯度(杂质不参与反应)通常利用“间接碘量法”测定。已知:
的纯度(杂质不参与反应)通常利用“间接碘量法”测定。已知: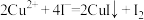
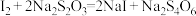 。步骤如下:
。步骤如下:
①称取1.250 g胆矾产品配成100 mL溶液;
②取其中25.00 mL溶液,滴加KI溶液至不再产生沉淀;
③用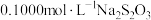 标准溶液滴定,平行滴定3次。
标准溶液滴定,平行滴定3次。
若 标准溶液的平均用量为10.00 mL,则胆矾产品纯度为
标准溶液的平均用量为10.00 mL,则胆矾产品纯度为_______ %。
Ⅰ.酸碱中和滴定
选择酚酞作指示剂,用标准NaOH溶液测定白醋中醋酸的浓度,以检测白醋是否符合国家标准。测定过程如图所示:

已知:国家标准规定酿造白醋中醋酸含量不得低于
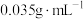 。
。(1)①滴定达到终点时的现象是滴入半滴标准NaOH溶液后
②某次实验滴定开始和结束时。碱式滴定管中的液面如图所示,则消耗NaOH溶液的体积为

③已知实验所用标准NaOH溶液的浓度为
 ,根据上述滴定结果可知该白醋
,根据上述滴定结果可知该白醋④下列操作中,可能使所测白醋中醋酸的浓度数值偏低的是
A.碱式滴定管未用标准NaOH溶液润洗就直接注入标准NaOH溶液
B.滴定前盛放白醋稀溶液的锥形瓶用蒸馏水洗净后没有干燥
C.滴定过程中摇动锥形瓶时有液滴溅出
D.读取NaOH溶液体积时,开始时仰视读数,滴定结束时俯视读数
E.碱式滴定管在滴定前有气泡,滴定后气泡消失
(2)若用
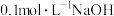 溶液分别滴定体积均为20.00 mL、浓度均为
溶液分别滴定体积均为20.00 mL、浓度均为 的盐酸和醋酸溶液,得到滴定过程中pH随加入NaOH溶液体积而变化的两条滴定曲线如图所示。
的盐酸和醋酸溶液,得到滴定过程中pH随加入NaOH溶液体积而变化的两条滴定曲线如图所示。
①滴定醋酸的曲线是
②
 和
和 的关系:
的关系:
 (填“>”“=”或“<”)。
(填“>”“=”或“<”)。③若25℃时,
 的醋酸与
的醋酸与 的氢氧化钠溶液等体积混合显中性,则醋酸的电离常数为
的氢氧化钠溶液等体积混合显中性,则醋酸的电离常数为Ⅱ.氧化还原滴定
(3)
 的纯度(杂质不参与反应)通常利用“间接碘量法”测定。已知:
的纯度(杂质不参与反应)通常利用“间接碘量法”测定。已知: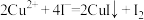
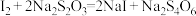 。步骤如下:
。步骤如下:①称取1.250 g胆矾产品配成100 mL溶液;
②取其中25.00 mL溶液,滴加KI溶液至不再产生沉淀;
③用
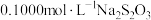 标准溶液滴定,平行滴定3次。
标准溶液滴定,平行滴定3次。若
 标准溶液的平均用量为10.00 mL,则胆矾产品纯度为
标准溶液的平均用量为10.00 mL,则胆矾产品纯度为
更新时间:2022-01-17 09:58:48
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】Ⅰ.滴定实验是化学学科中最重要的定量实验之一、葡萄酒中抗氧化剂残留量的测定,常采用氧化还原滴定法。葡萄酒常用 作抗氧化剂,测定某葡萄酒中抗氧化剂的残留量(以游离
作抗氧化剂,测定某葡萄酒中抗氧化剂的残留量(以游离 计算)的方案如下:
计算)的方案如下:

往实验中加入盐酸的目的是将 转化成
转化成 ;滴定过程中发生的反应是:
;滴定过程中发生的反应是:
(1)滴定时,该滴定过程的指示剂是___________ ,滴定终点的判断方法___________ 。
(2)实验消耗标准 溶液50.00ml,所测样品中抗氧化剂的残留量(以游离
溶液50.00ml,所测样品中抗氧化剂的残留量(以游离 计算)为
计算)为___________  。
。
(3)下列情形会造成测定结果偏高的是___________(填序号)。
Ⅱ.回答下列问题
(4) 随意排放会造成严重的大气污染。某小组同学利用
随意排放会造成严重的大气污染。某小组同学利用 溶液氧化吸收烟气中
溶液氧化吸收烟气中
①该反应的离子方程式___________ (反应a)。
为验证该反应,同学们将 通入0.05mol/L
通入0.05mol/L 溶液中,溶液很快由黄色变为红褐色;将溶液长时间放置后,最终变为浅绿色。关于红褐色液体,以下是同学们的分析推测与实验。
溶液中,溶液很快由黄色变为红褐色;将溶液长时间放置后,最终变为浅绿色。关于红褐色液体,以下是同学们的分析推测与实验。
②利用胶体的___________ (填性质)可以检验步骤Ⅰ中是否得到了 胶体。
胶体。
③根据反应b说明步骤II中液体颜色变化的原因是___________ (用离子方程式及必要的文字说明)。
④经讨论后得出结论: 溶液和
溶液和 反应过程中,反应a、b在体系中共存。请从化学反应速率和反应限度的角度分析,
反应过程中,反应a、b在体系中共存。请从化学反应速率和反应限度的角度分析, 通入
通入 溶液产生上述现象的原因
溶液产生上述现象的原因___________ 。
 作抗氧化剂,测定某葡萄酒中抗氧化剂的残留量(以游离
作抗氧化剂,测定某葡萄酒中抗氧化剂的残留量(以游离 计算)的方案如下:
计算)的方案如下:
往实验中加入盐酸的目的是将
 转化成
转化成 ;滴定过程中发生的反应是:
;滴定过程中发生的反应是:
(1)滴定时,该滴定过程的指示剂是
(2)实验消耗标准
 溶液50.00ml,所测样品中抗氧化剂的残留量(以游离
溶液50.00ml,所测样品中抗氧化剂的残留量(以游离 计算)为
计算)为 。
。(3)下列情形会造成测定结果偏高的是___________(填序号)。
| A.滴定持续时间稍长,溶液中部分HI被空气氧化 |
B.盛装标准 溶液的滴定管用蒸馏水洗净后,未润洗 溶液的滴定管用蒸馏水洗净后,未润洗 |
| C.滴定前平视,滴定后俯视 |
| D.滴定前滴定管尖嘴有气泡滴定后气泡消失 |
Ⅱ.回答下列问题
(4)
 随意排放会造成严重的大气污染。某小组同学利用
随意排放会造成严重的大气污染。某小组同学利用 溶液氧化吸收烟气中
溶液氧化吸收烟气中
①该反应的离子方程式
为验证该反应,同学们将
 通入0.05mol/L
通入0.05mol/L 溶液中,溶液很快由黄色变为红褐色;将溶液长时间放置后,最终变为浅绿色。关于红褐色液体,以下是同学们的分析推测与实验。
溶液中,溶液很快由黄色变为红褐色;将溶液长时间放置后,最终变为浅绿色。关于红褐色液体,以下是同学们的分析推测与实验。| 分析推测 | 实验步骤及现象 |
甲:生成了 胶体 胶体乙:经查阅资料,可能发生反应: 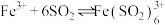 (反应b)(红褐色) (反应b)(红褐色) | Ⅰ.制备 胶体并检验 胶体并检验Ⅱ.分别向  胶体和该红褐色液体中加入适量铁粉,振荡后前者不变色,后者变为浅绿色 胶体和该红褐色液体中加入适量铁粉,振荡后前者不变色,后者变为浅绿色 |
 胶体。
胶体。③根据反应b说明步骤II中液体颜色变化的原因是
④经讨论后得出结论:
 溶液和
溶液和 反应过程中,反应a、b在体系中共存。请从化学反应速率和反应限度的角度分析,
反应过程中,反应a、b在体系中共存。请从化学反应速率和反应限度的角度分析, 通入
通入 溶液产生上述现象的原因
溶液产生上述现象的原因
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】氧泡泡是一种多功能新型漂白剂,其有效成分是过碳酸钠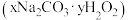 ,溶于水可分解成
,溶于水可分解成 和
和 。
。
(1) 常用作过碳酸钠分解时的催化剂。
常用作过碳酸钠分解时的催化剂。 在
在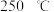 时分解可得到
时分解可得到 、
、 、
、 ,写出该反应的化学方程式:
,写出该反应的化学方程式:_______ 。
测定氧泡泡样品中过碳酸钠化学式的实验步骤如下(样品中其他物质不参加反应):
步骤①:用电子天平称取两份等质量的样品。
步骤②:将一份置于锥形瓶中,加水溶解,用甲基橙作指示剂,用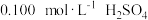 溶液滴定至终点,消耗硫酸
溶液滴定至终点,消耗硫酸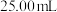 。
。
步骤③:将另一份加水溶解后用稀硫酸酸化,用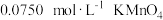 溶液滴定至终点
溶液滴定至终点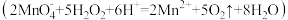 ,消耗
,消耗 溶液
溶液 。
。
(2)步骤②中,滴定终点的现象是_______ 。
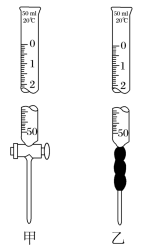
(3)步骤③中, 溶液盛放在如图中
溶液盛放在如图中_______ (填“甲”或“乙”)滴定管中。装液前要进行润洗,具体操作是:向滴定管中注入少量 标准溶液
标准溶液_______ 。
(4)下列操作会导致 的测定结果偏低的是_______。
的测定结果偏低的是_______。
(5)通过计算确定该过碳酸钠化学式_______ (写出计算过程)。
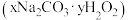 ,溶于水可分解成
,溶于水可分解成 和
和 。
。(1)
 常用作过碳酸钠分解时的催化剂。
常用作过碳酸钠分解时的催化剂。 在
在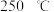 时分解可得到
时分解可得到 、
、 、
、 ,写出该反应的化学方程式:
,写出该反应的化学方程式:测定氧泡泡样品中过碳酸钠化学式的实验步骤如下(样品中其他物质不参加反应):
步骤①:用电子天平称取两份等质量的样品。
步骤②:将一份置于锥形瓶中,加水溶解,用甲基橙作指示剂,用
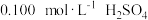 溶液滴定至终点,消耗硫酸
溶液滴定至终点,消耗硫酸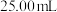 。
。步骤③:将另一份加水溶解后用稀硫酸酸化,用
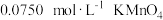 溶液滴定至终点
溶液滴定至终点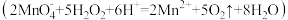 ,消耗
,消耗 溶液
溶液 。
。(2)步骤②中,滴定终点的现象是
(3)步骤③中,
 溶液盛放在如图中
溶液盛放在如图中 标准溶液
标准溶液
(4)下列操作会导致
 的测定结果偏低的是_______。
的测定结果偏低的是_______。| A.样品溶于水酸化后放置一段时间,然后再进行滴定 |
| B.滴定管用蒸馏水洗净后未用标准溶液润洗 |
| C.滴定前读数时仰视滴定管读数 |
D.滴定前尖嘴部分有气泡,滴定后尖嘴部分充满 溶液 溶液 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。为测定补血剂中铁元素的含量,某化学兴趣小组设计了两套实验方案。
方案一 滴定法:用酸性KMnO4溶液滴定,测定铁元素的含量
(1)写出该滴定反应的离子方程式_______________________ 。
(2)某同学设计的下列滴定方式中,最合理的是________ (夹持部分略去)(填字母序号)

(3)实验前,首先要精确配制一定物质的量浓度的KMnO4溶液250 mL,配制时需要的仪器除天平、药匙、烧杯、胶头滴管外,还需___________ (填仪器名称)。
在溶液配制过程中,下列操作会导致配制结果偏低的是___________ (填写代号)。
a. 定容时,俯视容量瓶刻度线
b. 容量瓶在使用前内有少量蒸馏水
c. 转移溶液后的烧杯、玻璃棒未洗涤
d. 定容后摇匀,发现液面降低,又补加少量水,重新达到刻度线
(4)上述实验中KMnO4溶液需要酸化,用于酸化的酸是________ 。
a.浓盐酸 b.稀硫酸 c.稀硝酸 d.浓硫酸
方案二 称量法:操作流程如下:

(5)写出步骤②中H2O2氧化Fe2+的离子方程式_______________ 。
步骤②中除用H2O2外还可以使用的物质是___________
步骤②是否可以省略________ ,理由是_______________ 。
(6)步骤④一系列操作依次是:过滤、洗涤、____________ 、冷却、称量。
(7)假设实验无损耗,则每片补血剂含铁元素的质量________ g(用含a的代数式表示)。
方案一 滴定法:用酸性KMnO4溶液滴定,测定铁元素的含量
(1)写出该滴定反应的离子方程式
(2)某同学设计的下列滴定方式中,最合理的是

(3)实验前,首先要精确配制一定物质的量浓度的KMnO4溶液250 mL,配制时需要的仪器除天平、药匙、烧杯、胶头滴管外,还需
在溶液配制过程中,下列操作会导致配制结果偏低的是
a. 定容时,俯视容量瓶刻度线
b. 容量瓶在使用前内有少量蒸馏水
c. 转移溶液后的烧杯、玻璃棒未洗涤
d. 定容后摇匀,发现液面降低,又补加少量水,重新达到刻度线
(4)上述实验中KMnO4溶液需要酸化,用于酸化的酸是
a.浓盐酸 b.稀硫酸 c.稀硝酸 d.浓硫酸
方案二 称量法:操作流程如下:

(5)写出步骤②中H2O2氧化Fe2+的离子方程式
步骤②中除用H2O2外还可以使用的物质是
步骤②是否可以省略
(6)步骤④一系列操作依次是:过滤、洗涤、
(7)假设实验无损耗,则每片补血剂含铁元素的质量
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】今有①CH3COOH;②HCl;③H2SO4三种溶液,(1)~(3)题请选择填空:
A.①>②>③ B.①<②<③ C.①=②=③ E.①>②=③
D.①=③>② F.①<②=③ G.①=②<③ H.①=②>③
(1)当它们pH相同时,其物质的量浓度关系是___________ 。
(2)体积和物质的量浓度相同的①、②、③三溶液,分别与同浓度的烧碱溶液反应,要使反应后的溶液呈中性,所需烧碱溶液的体积关系为_________________ 。
(3)当它们pH相同、体积相同时,分别加入足量锌,则开始时反应速率_________ ,相同状况下产生气体体积关系为____________ 。
(4)某学生用0.2000mol/L NaOH溶液滴定未知浓度的盐酸溶液,其操作可分解为如下几步:
(A)移取20.00mL待测的盐酸溶液注入洁净的锥形瓶,并加入2-3滴酚酞
(B)用标准溶液润洗滴定管2-3次
(C)把盛有标准溶液的滴定管固定好,调节液面使滴定管尖嘴充满溶液
(D)取标准NaOH溶液注入滴定管至0刻度以上2-3cm
(E)调节液面至0或0刻度以下,记下读数
(F)把锥形瓶放在滴定管的下面,用标准NaOH溶液滴定至终点,记下滴定管液面的刻度
完成以下填空:
①正确操作的顺序是(用序号字母填写)___________________________ ,
②实验中,眼睛应注视___________________________ ,直至滴定终点。
③几次滴定消耗NaOH溶液的体积如下:
则该盐酸溶液的准确浓度为_____________ 。(保留小数点后4位)
(5)用标准的NaOH滴定未知浓度的盐酸,选用酚酞为指示剂,造成测定结果偏高的原因可能是____________ 。
A. 配制标准溶液的氢氧化钠中混有Na2CO3杂质
B. 滴定终点读数时,俯视滴定管的刻度,其它操作均正确
C. 盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗
D. 滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
E. 未用标准液润洗滴定管
A.①>②>③ B.①<②<③ C.①=②=③ E.①>②=③
D.①=③>② F.①<②=③ G.①=②<③ H.①=②>③
(1)当它们pH相同时,其物质的量浓度关系是
(2)体积和物质的量浓度相同的①、②、③三溶液,分别与同浓度的烧碱溶液反应,要使反应后的溶液呈中性,所需烧碱溶液的体积关系为
(3)当它们pH相同、体积相同时,分别加入足量锌,则开始时反应速率
(4)某学生用0.2000mol/L NaOH溶液滴定未知浓度的盐酸溶液,其操作可分解为如下几步:
(A)移取20.00mL待测的盐酸溶液注入洁净的锥形瓶,并加入2-3滴酚酞
(B)用标准溶液润洗滴定管2-3次
(C)把盛有标准溶液的滴定管固定好,调节液面使滴定管尖嘴充满溶液
(D)取标准NaOH溶液注入滴定管至0刻度以上2-3cm
(E)调节液面至0或0刻度以下,记下读数
(F)把锥形瓶放在滴定管的下面,用标准NaOH溶液滴定至终点,记下滴定管液面的刻度
完成以下填空:
①正确操作的顺序是(用序号字母填写)
②实验中,眼睛应注视
③几次滴定消耗NaOH溶液的体积如下:
| 实验序号 | 1 | 2 | 3 | 4 |
| 消耗NaOH溶液的体积(mL) | 20.05 | 20.00 | 18.80 | 19.95 |
(5)用标准的NaOH滴定未知浓度的盐酸,选用酚酞为指示剂,造成测定结果偏高的原因可能是
A. 配制标准溶液的氢氧化钠中混有Na2CO3杂质
B. 滴定终点读数时,俯视滴定管的刻度,其它操作均正确
C. 盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗
D. 滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
E. 未用标准液润洗滴定管
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某学生用0.1000mol·L-1的KOH标准溶液滴定未知浓度的盐酸,其操作分解为如下几步:
A.移取20mL待测盐酸注入洁净的锥形瓶,并加入2~3滴酚酞
B.调节液面至“0”或“0”以下某一刻度,记下读数
C.把盛有标准溶液的碱式滴定管固定好,调节滴定管尖嘴使之充满溶液
D.取标准KOH溶液注入碱式滴定管至“0”刻度以上1~2cm
E.用标准溶液润洗滴定管2~3次
F.把锥形瓶放在滴定管的下面,用标准KOH溶液滴定至终点并记下滴定管液面的刻度
就此实验完成填空:
(1)正确操作步骤的顺序是(用序号字母填写) A→_______ →F;
(2)若无上述E步骤操作,则测定结果会_______ (填“偏高”、“偏低”或“无影响”,下同);
(3)上述A步骤之前,若先用待测液润洗锥形瓶,则对滴定结果的影响是_______ ;
(4)判断到达滴定终点的现象是_______ ;
(5)若该学生在实验过程中,记录滴定前滴定管内液面读数为2.60ml,滴定后液面如图,则此时消耗标准溶液的体积为_______ mL。

(6)KMnO4常用于氧化还原滴定。滴定时应将KMnO4加入_______ 滴定管中(填“酸式”或“碱式”)。
A.移取20mL待测盐酸注入洁净的锥形瓶,并加入2~3滴酚酞
B.调节液面至“0”或“0”以下某一刻度,记下读数
C.把盛有标准溶液的碱式滴定管固定好,调节滴定管尖嘴使之充满溶液
D.取标准KOH溶液注入碱式滴定管至“0”刻度以上1~2cm
E.用标准溶液润洗滴定管2~3次
F.把锥形瓶放在滴定管的下面,用标准KOH溶液滴定至终点并记下滴定管液面的刻度
就此实验完成填空:
(1)正确操作步骤的顺序是(用序号字母填写) A→
(2)若无上述E步骤操作,则测定结果会
(3)上述A步骤之前,若先用待测液润洗锥形瓶,则对滴定结果的影响是
(4)判断到达滴定终点的现象是
(5)若该学生在实验过程中,记录滴定前滴定管内液面读数为2.60ml,滴定后液面如图,则此时消耗标准溶液的体积为

(6)KMnO4常用于氧化还原滴定。滴定时应将KMnO4加入
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】二氧化氯 (ClO2)是一种黄绿色气体,易溶于水,在混合气体中的体积分数大于10%就可能发生爆炸,在工业上常用作水处理剂、漂白剂。回答下列问题:
(1)某小组按照文献中制备 的方法设计了如图所示的实验装置用于制备
的方法设计了如图所示的实验装置用于制备 。
。

①通入氮气的主要作用有2个,一是可以起到搅拌作用,二是___________ 。
②装置B的作用是___________ 。
③A装置中,装 溶液的仪器名称为:
溶液的仪器名称为:___________ 。
(2)测定装置C中 溶液的浓度:取
溶液的浓度:取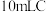 中溶液于锥形瓶中,加入足量的
中溶液于锥形瓶中,加入足量的 溶液和
溶液和 酸化 (
酸化 (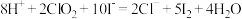 ),然后加入
),然后加入___________ 作指示剂,用 的
的 标准液滴定锥形瓶中的溶液(
标准液滴定锥形瓶中的溶液( ),当看到
),当看到___________ 现象时,测得标准液消耗的体积为 ,通过计算可知C中
,通过计算可知C中 溶液的浓度为
溶液的浓度为___________  。
。
(3)下列操作使测定结果偏低的是___________
(1)某小组按照文献中制备
 的方法设计了如图所示的实验装置用于制备
的方法设计了如图所示的实验装置用于制备 。
。
①通入氮气的主要作用有2个,一是可以起到搅拌作用,二是
②装置B的作用是
③A装置中,装
 溶液的仪器名称为:
溶液的仪器名称为:(2)测定装置C中
 溶液的浓度:取
溶液的浓度:取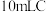 中溶液于锥形瓶中,加入足量的
中溶液于锥形瓶中,加入足量的 溶液和
溶液和 酸化 (
酸化 (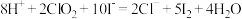 ),然后加入
),然后加入 的
的 标准液滴定锥形瓶中的溶液(
标准液滴定锥形瓶中的溶液( ),当看到
),当看到 ,通过计算可知C中
,通过计算可知C中 溶液的浓度为
溶液的浓度为 。
。(3)下列操作使测定结果偏低的是___________
| A.滴定前俯视,滴定终点仰视读数 |
B.盛放 标准溶液的滴定管未用标准液润洗 标准溶液的滴定管未用标准液润洗 |
| C.锥形瓶用蒸馏水洗净后未干燥直接装入待测液 |
| D.滴定前正常,滴定后滴定管尖嘴内有气泡 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】用实验确定某酸HA是否为弱电解质,两位同学的方案如下:
甲:①称取一定质量的HA,配制0.1mol•L-1的溶液100mL;②用pH计测出该溶液的pH,根据测定结果即可判断HA是否为弱电解质。
乙:①用已知物质的量浓度的HA溶液、盐酸分别配制pH=2的两种酸溶液各100mL;②分别取这两种溶液各10mL,加水稀释为100mL;③各取相同体积的两种稀释液于两支试管中,同时加入相同纯度的锌粒,根据观察到的实验现象即可判断HA是否为弱电解质。
(1)在两个方案的步骤①中,都要用到的定量仪器是____ 。
(2)甲方案中,若测得溶液的pH____ (填“>”“<”或“=”)1,则可说明HA是弱电解质。
(3)乙方案中,能说明HA是弱电解质的现象是____ (填字母序号)。
A.装盐酸的试管中放出H2的速率较大
B.装HA溶液的试管中放出H2的速率较大
C.两支试管中产生气体的速率一样大
(4)请你对两种方案的可行性作出评价____ 。
(5)请你再设计一个合理而比较容易进行的实验方案(药品可任取),并作简明扼要的表述_____ 。
甲:①称取一定质量的HA,配制0.1mol•L-1的溶液100mL;②用pH计测出该溶液的pH,根据测定结果即可判断HA是否为弱电解质。
乙:①用已知物质的量浓度的HA溶液、盐酸分别配制pH=2的两种酸溶液各100mL;②分别取这两种溶液各10mL,加水稀释为100mL;③各取相同体积的两种稀释液于两支试管中,同时加入相同纯度的锌粒,根据观察到的实验现象即可判断HA是否为弱电解质。
(1)在两个方案的步骤①中,都要用到的定量仪器是
(2)甲方案中,若测得溶液的pH
(3)乙方案中,能说明HA是弱电解质的现象是
A.装盐酸的试管中放出H2的速率较大
B.装HA溶液的试管中放出H2的速率较大
C.两支试管中产生气体的速率一样大
(4)请你对两种方案的可行性作出评价
(5)请你再设计一个合理而比较容易进行的实验方案(药品可任取),并作简明扼要的表述
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)在一定温度下,有a.盐酸 b.硫酸 c.醋酸三种酸:
a.当三种酸物质的量浓度相同时,c(H+)由大到小的顺序是_______ (用字母表示,下同)。
b.同体积、同物质的量浓度的三种酸,中和NaOH 的能力由大到小的顺序是_______ 。
c.若三者c(H+)相同时,物质的量浓度由大到小的顺序是_______ 。
d.将c(H+)相同且体积也相同的三种酸,分别与等浓度的NaOH稀溶液反应至pH=7,则消耗NaOH溶液液的体积大小关系为_______ 。
e.将c(H+)相同的三种酸均加水稀释至原来的100倍后,c(H+)由大到小的顺序是_______ 。
(2)当H2S浓度较低时常用纯碱溶液进行吸收。表为H2S、H2CO3 的电离平衡常数。
纯碱溶液吸收少量H2S的离子方程式为_______ 。
(3)磷酸是三元弱酸,常温下三级电离常数分别是Ka1=7.1×10-3,Ka2=6.2×10-8,Ka3=4.5×10-13,解答下列问题:
a.常温下同浓度①Na3PO4、②Na2HPO4、③NaH2PO4的pH由小到大的顺序是_______ (填序号)。
b.常温下,NaH2PO4的水溶液pH_______ (填“>”“<”或“=”)7。
c.常温下,Na2HPO4的水溶液呈_______ (填“酸”“碱”或“中”)性
a.当三种酸物质的量浓度相同时,c(H+)由大到小的顺序是
b.同体积、同物质的量浓度的三种酸,中和NaOH 的能力由大到小的顺序是
c.若三者c(H+)相同时,物质的量浓度由大到小的顺序是
d.将c(H+)相同且体积也相同的三种酸,分别与等浓度的NaOH稀溶液反应至pH=7,则消耗NaOH溶液液的体积大小关系为
e.将c(H+)相同的三种酸均加水稀释至原来的100倍后,c(H+)由大到小的顺序是
(2)当H2S浓度较低时常用纯碱溶液进行吸收。表为H2S、H2CO3 的电离平衡常数。
| 电离平衡常数 | Kal | Ka2 |
| H2S | 9.1×10-8 | 1.1×10-12 |
| H2CO3 | 4.3×10-7 | 5.61×10-11 |
纯碱溶液吸收少量H2S的离子方程式为
(3)磷酸是三元弱酸,常温下三级电离常数分别是Ka1=7.1×10-3,Ka2=6.2×10-8,Ka3=4.5×10-13,解答下列问题:
a.常温下同浓度①Na3PO4、②Na2HPO4、③NaH2PO4的pH由小到大的顺序是
b.常温下,NaH2PO4的水溶液pH
c.常温下,Na2HPO4的水溶液呈
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】甲、乙两位同学设计用实验确定某酸HA是弱电解质,存在电离平衡,且改变条件平衡发生移动。实验方案如下:

甲:①准确配制0.1mol·L-1的HA、HCl溶液各100mL;
②取纯度相同,质量、大小相等的锌粒放入两支试管中,同时加入0.1mol·L-1的HA、HCl溶液各100mL,按上图装好,观察现象。
乙:①用pH计测定物质的量浓度均为0.1mol·L-1的HA和HCl溶液的pH;
②再取0.1mol·L-1的HA和HCl溶液各2滴(1滴约为 mL)分别稀释至100mL,
mL)分别稀释至100mL,
再用pH计测其pH变化。
(1)乙方案中说明HA是弱电解质的理由是,测得0.1mol·L-1的HA溶液的pH____ 1(填“>”“<”或“=”);甲方案中,说明HA是弱电解质的实验现象是_____ 。
A.装HCl的试管中放出的氢气速率大
B.装HA溶液的试管中放出氢气的速率大
C.两个试管中产生气体速率一样大
(2)乙同学设计的实验第②步,能证明改变条件,弱电解质平衡发生移动。加水稀释,弱酸HA的电离程度_______ (填“增大、减小、不变”)
(3)甲同学为了进一步证明弱电解质电离平衡移动的情况,设计如下实验:使HA的电离程度和c(H+)都减小,c(A-)增大,可在0.1mol·L-1的HA溶液中,选择加入____________ 试剂。
A.NaA固体(可完全溶于水) B.1mol·L-1NaOH溶液
C.1mol·L-1H2SO4 D.2mol·L-1HA
(4)pH=1的两种酸溶液A、B各1mL,分别加水稀释到1000mL,其pH与溶液体积V的关系如图所示,则下列说法不正确的有_________

A.若a=4,则A是强酸,B是弱酸
B.若1<a<4,则A、B都是弱酸
C.两种酸溶液的物质的量浓度一定相等
D.稀释后,A溶液的酸性比B溶液弱

甲:①准确配制0.1mol·L-1的HA、HCl溶液各100mL;
②取纯度相同,质量、大小相等的锌粒放入两支试管中,同时加入0.1mol·L-1的HA、HCl溶液各100mL,按上图装好,观察现象。
乙:①用pH计测定物质的量浓度均为0.1mol·L-1的HA和HCl溶液的pH;
②再取0.1mol·L-1的HA和HCl溶液各2滴(1滴约为
 mL)分别稀释至100mL,
mL)分别稀释至100mL,再用pH计测其pH变化。
(1)乙方案中说明HA是弱电解质的理由是,测得0.1mol·L-1的HA溶液的pH
A.装HCl的试管中放出的氢气速率大
B.装HA溶液的试管中放出氢气的速率大
C.两个试管中产生气体速率一样大
(2)乙同学设计的实验第②步,能证明改变条件,弱电解质平衡发生移动。加水稀释,弱酸HA的电离程度
(3)甲同学为了进一步证明弱电解质电离平衡移动的情况,设计如下实验:使HA的电离程度和c(H+)都减小,c(A-)增大,可在0.1mol·L-1的HA溶液中,选择加入
A.NaA固体(可完全溶于水) B.1mol·L-1NaOH溶液
C.1mol·L-1H2SO4 D.2mol·L-1HA
(4)pH=1的两种酸溶液A、B各1mL,分别加水稀释到1000mL,其pH与溶液体积V的关系如图所示,则下列说法不正确的有

A.若a=4,则A是强酸,B是弱酸
B.若1<a<4,则A、B都是弱酸
C.两种酸溶液的物质的量浓度一定相等
D.稀释后,A溶液的酸性比B溶液弱
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】三草酸合铁(Ⅲ)酸钾晶体,即K3[Fe(C2O4)3]•3H2O,摩尔质量为491g•mol-1,绿色晶体,溶于水,难溶于乙醇,110℃下失去结晶水,230℃分解,见光易分解。某小组制备三草酸合铁(Ⅲ)酸钾晶体并研究其性质及组成。
I.制备三草酸合铁酸钾晶体
步骤i:往2.88g草酸亚铁悬浊液中加入过量K2C2O4溶液,水浴加热至40℃。再滴入过量H2O2溶液,一段时间后,出现红褐色浑浊。
步骤ii:加热溶液至沸,加入H2C2O4溶液。保持微沸,边搅拌边逐滴加入饱和H2C2O4溶液,至溶液呈亮绿透明状。
步骤iii:待溶液稍冷,加入无水乙醇,冷却结晶。
步骤iv:减压过滤,洗涤,低温烘干,得到7.86g亮绿色晶体。
(1)步骤i中,在过量K2C2O4存在时,草酸亚铁和H2O2生成三草酸合铁酸钾与另一种铁的化合物。写出该反应的化学方程式:___ 。
(2)步骤ii加入H2C2O4的目的是___ 。
(3)步骤iii中加入无水乙醇的作用是___ 。
(4)该实验的产率为___ (结果保留三位有效数字)。产率偏低的主要原因可能是___ 。
Ⅱ.三草酸合铁酸钾性质探究
取少量K3[Fe(C2O4)3]•3H2O和K3[Fe(CN)6]固体,溶于水,用毛笔蘸取该溶液在滤纸上写字,在日光下放置一段时间,滤纸上就会显现深蓝色的字迹。
(5)根据上述实验现象可知,K3[Fe(C2O4)3]光照分解产物有___ (填化学式)。
Ⅲ.三草酸合铁酸钾配离子电荷数(n)的测定
称取0.25gK3[Fe(C2O4)3]•3H2O加蒸馏水溶解。将溶液全部通过氯型阴离子交换柱,充分交换出Cl-,用100mL容量瓶承接洗脱液。用蒸馏水不断淋洗交换柱,最终配成100mL溶液。取25.00mL于250mL锥形瓶中,加入少量K2CrO4溶液。用0.1mol·L-1AgNO3标准溶液滴定至终点,消耗AgNO3溶液VmL。已知:n=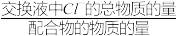
(6)列出n的计算表达式:____ 。
I.制备三草酸合铁酸钾晶体
步骤i:往2.88g草酸亚铁悬浊液中加入过量K2C2O4溶液,水浴加热至40℃。再滴入过量H2O2溶液,一段时间后,出现红褐色浑浊。
步骤ii:加热溶液至沸,加入H2C2O4溶液。保持微沸,边搅拌边逐滴加入饱和H2C2O4溶液,至溶液呈亮绿透明状。
步骤iii:待溶液稍冷,加入无水乙醇,冷却结晶。
步骤iv:减压过滤,洗涤,低温烘干,得到7.86g亮绿色晶体。
(1)步骤i中,在过量K2C2O4存在时,草酸亚铁和H2O2生成三草酸合铁酸钾与另一种铁的化合物。写出该反应的化学方程式:
(2)步骤ii加入H2C2O4的目的是
(3)步骤iii中加入无水乙醇的作用是
(4)该实验的产率为
Ⅱ.三草酸合铁酸钾性质探究
取少量K3[Fe(C2O4)3]•3H2O和K3[Fe(CN)6]固体,溶于水,用毛笔蘸取该溶液在滤纸上写字,在日光下放置一段时间,滤纸上就会显现深蓝色的字迹。
(5)根据上述实验现象可知,K3[Fe(C2O4)3]光照分解产物有
Ⅲ.三草酸合铁酸钾配离子电荷数(n)的测定
称取0.25gK3[Fe(C2O4)3]•3H2O加蒸馏水溶解。将溶液全部通过氯型阴离子交换柱,充分交换出Cl-,用100mL容量瓶承接洗脱液。用蒸馏水不断淋洗交换柱,最终配成100mL溶液。取25.00mL于250mL锥形瓶中,加入少量K2CrO4溶液。用0.1mol·L-1AgNO3标准溶液滴定至终点,消耗AgNO3溶液VmL。已知:n=
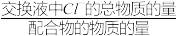
(6)列出n的计算表达式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】铁是人体必需的微量元素,严重缺铁时需要服用补铁剂。已知某补铁剂不溶于水但能溶于人体中的胃液(含盐酸)。某同学为了检测该补铁剂中 的存在,设计并进行了如下实验:
的存在,设计并进行了如下实验:

(1)试剂2的化学式是_________ 。加入试剂2后溶液变为浅红色,此现象说明溶液①中含有_______ (填微粒符号)。
(2)加入新制氯水,溶液中发生反应的离子方程式是___________ 。
(3)不仅溶液中Fe2+易被氧化成Fe3+,溶液中白色沉淀Fe(OH)2更易被O2氧化,请写出反应的化学方程式________________ 。
(4)某同学通过如下实验测定该补铁剂中铁元素的含量。试计算:每片该补铁剂含铁元素的质量为_______ g(用含a、m的代数式表示)。

 的存在,设计并进行了如下实验:
的存在,设计并进行了如下实验:
(1)试剂2的化学式是
(2)加入新制氯水,溶液中发生反应的离子方程式是
(3)不仅溶液中Fe2+易被氧化成Fe3+,溶液中白色沉淀Fe(OH)2更易被O2氧化,请写出反应的化学方程式
(4)某同学通过如下实验测定该补铁剂中铁元素的含量。试计算:每片该补铁剂含铁元素的质量为

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】硫酸铜受热分解生成氧化铜和气体,加热温度不同,气体成分也不同。气体成分可能含SO2、SO3和O2中的一种、两种或三种。某化学课外活动小组通过设计探究性实验,测定反应产生的SO2、SO3和O2的物质的量,并计算确定各物质的化学计量数,从而确定CuSO4分解的化学方程式。实验用到的仪器如下图所示:
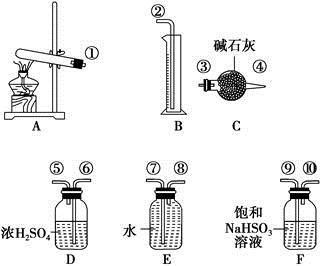
[提出猜想]
Ⅰ.所得气体的成分可能只含SO3一种;
Ⅱ.所得气体的成分可能含有_______ 两种;
Ⅲ.所得气体的成分可能含有_______ 三种。
[实验探究]
实验操作过程略。已知实验结束时,硫酸铜完全分解。
(1)请你组装探究实验的装置,按从左至右的方向,各仪器接口的连接顺序为①→⑨→⑩→⑥→⑤→_______ →_______ →_______ →_______ →②(填接口序号)。
(2)若实验结束时B中量筒没有收集到水,则证明猜想_______ 正确。
(3)有两个实验小组进行该实验,由于加热时的温度不同,实验结束后测得相关数据也不同,数据如下:
请通过计算,推断出第一小组和第二小组的实验条件下CuSO4分解的化学方程式。
第一小组:_______________________________________________________ ;
第二小组:_______________________________________________________ 。

[提出猜想]
Ⅰ.所得气体的成分可能只含SO3一种;
Ⅱ.所得气体的成分可能含有
Ⅲ.所得气体的成分可能含有
[实验探究]
实验操作过程略。已知实验结束时,硫酸铜完全分解。
(1)请你组装探究实验的装置,按从左至右的方向,各仪器接口的连接顺序为①→⑨→⑩→⑥→⑤→
(2)若实验结束时B中量筒没有收集到水,则证明猜想
(3)有两个实验小组进行该实验,由于加热时的温度不同,实验结束后测得相关数据也不同,数据如下:
| 实验小组 | 称取CuSO4的质量/g | 装置C增加的质量/g | 量筒中水的体积折算成标准状况下气体的体积/mL |
| 一 | 6.4 | 2.56 | 448 |
| 二 | 6.4 | 2.56 | 224 |
请通过计算,推断出第一小组和第二小组的实验条件下CuSO4分解的化学方程式。
第一小组:
第二小组:
您最近一年使用:0次



