为研究沉淀的生成及转化,某小组进行如下实验。关于该实验的分析不正确的是
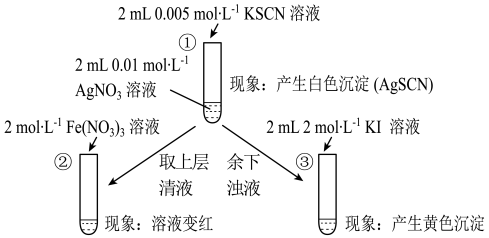

A.①浊液中存在平衡:AgSCN(s)  Ag+ (aq)+ SCN-(aq) Ag+ (aq)+ SCN-(aq) |
| B.②中颜色变化说明上层清液中含有SCN- |
| C.③中颜色变化说明有AgI生成 |
| D.该实验可以证明:Ksp(AgI)<Ksp(AgSCN) |
更新时间:2022-01-24 19:36:23
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】在一定温度下,当 固体在水中达到溶解平衡时,若使固体
固体在水中达到溶解平衡时,若使固体 的量减少,而
的量减少,而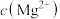 不变,可采取的措施是
不变,可采取的措施是
 固体在水中达到溶解平衡时,若使固体
固体在水中达到溶解平衡时,若使固体 的量减少,而
的量减少,而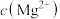 不变,可采取的措施是
不变,可采取的措施是A.加 固体 固体 | B.加少量 | C.加 固体 固体 | D.通入 气体 气体 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】硫化镉(CdS)是一种难溶于水的黄色颜料,其在水中的沉淀溶解平衡曲线如图所示。下列说法不正确的是( )


| A.图中a和b分别为T1、T2温度下CdS在水中的溶解度 |
| B.图中各点对应的Ksp的关系为:Ksp(m)=Ksp(n)<Ksp(p)<Ksp(q) |
| C.向n点的溶液中加入少量CdCl2固体,溶液组成由n沿npm线向m方向移动 |
| D.温度升高时,p点的饱和溶液的组成由p沿pq线向q方向移动 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列实验事实不能用平衡移动原理解释的是( )
| A.CaCO3溶于稀盐酸 |
| B.镁条与氯化铵溶液反应生成氢气 |
| C.升高温度,水的离子积增大 |
| D.加入少量CuSO4可增大锌与稀硫酸反应的速率 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】某闪锌矿的主要成分为ZnS,还含有SiO2、FeS2等,利用该闪锌矿制备皓钒(ZnSO4·7H2O)的工艺流程如下图所示。

下列说法错误的是

下列说法错误的是
| A.“破碎”可加快“煅烧”速率,并使反应更充分 |
| B.“废气”合理处理可用于工业制硫酸 |
| C.“滤渣”的主要成分为Fe2O3,可用于冶炼铁 |
| D.“一系列操作”包括蒸发浓缩、冷却结晶、过滤等 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】为完成下列各组实验,所选实验器材和试剂均完整正确的是
| 选项 | 实验 | 实验器材 | 试剂 |
| A | 配制100mL一定物质的量浓度的NaCl溶液 | 100mL容量瓶、胶头滴管、烧杯、量筒、玻璃棒 | 蒸馏水、NaCl固体 |
| B | 测定酸碱滴定曲线 | 酸式滴定管、碱式滴定管、滴定管夹、烧杯、锥形瓶、铁架台 | 0.1000mol•L-1NaOH溶液、0.1000mol•L-1盐酸溶液、甲基橙 |
| C | 淀粉水解产物检验 | 试管、胶头滴管、酒精灯 | 淀粉溶液、10%NaOH溶液、2%CuSO4溶液 |
| D | 证明Ksp(CuS)<Ksp(ZnS) | 试管、胶头滴管 | 0.10mol•L-1CuSO4溶液、0.10mol•L-1ZnSO4溶液、1mol•L-1Na2S溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】下列化学用语对现象变化的解释不准确 的
A.澄清的石灰水久置后出现白色浑浊: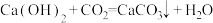 |
B.用石墨电极电解 溶液,阴极附近溶液蓝色变浅: 溶液,阴极附近溶液蓝色变浅: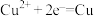 |
C.向 溶液中加入 溶液中加入 水,溶液呈黄色: 水,溶液呈黄色: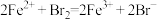 |
D.向 悬浊液中滴加 悬浊液中滴加 溶液出现红褐色沉淀: 溶液出现红褐色沉淀: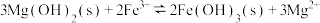 |
您最近一年使用:0次

 Mg+Cl2↑
Mg+Cl2↑ =BaCO3↓
=BaCO3↓ (aq)
(aq)

