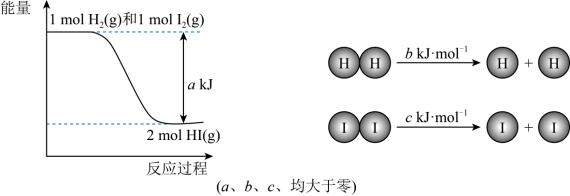
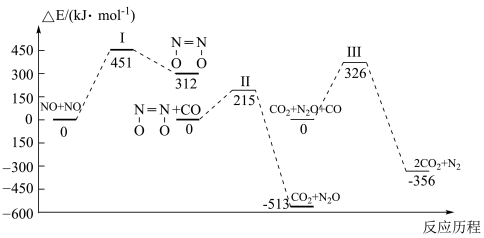
我国学者结合实验与计算机模拟结果,研究了均相NO-CO的反应历程,该反应经历了I、II、III三个过渡态。图中显示的是反应路径中每一阶段内各驻点的能量相对于此阶段内反应物能量的差值。下列说法正确的是

A. 比 比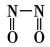 更容易与CO发生反应 更容易与CO发生反应 |
| B.整个反应分为三个基元反应阶段,其中第一个反应阶段活化能最大 |
C.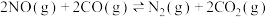  |
| D.其他条件不变,增大压强或使用催化剂均可以增大反应速率,提高反应物平衡转化率 |
更新时间:2022-01-21 19:27:05
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】氮的氧化物转化是环境化学热点问题之一、研究发现, 还原NO的反应
还原NO的反应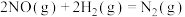
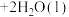 分两步进行:①
分两步进行:① ;②
;② ,其能量变化如图所示(Ts代表过渡态)。下列叙述正确的是
,其能量变化如图所示(Ts代表过渡态)。下列叙述正确的是
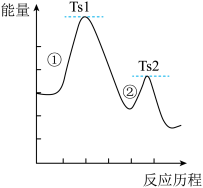
 还原NO的反应
还原NO的反应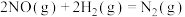
 分两步进行:①
分两步进行:① ;②
;② ,其能量变化如图所示(Ts代表过渡态)。下列叙述正确的是
,其能量变化如图所示(Ts代表过渡态)。下列叙述正确的是
| A.②是放热反应,①是吸热反应 | B. 是该反应的催化剂 是该反应的催化剂 |
| C.反应①的活化能大于反应② | D.加入催化剂的目的是降低Ts2的能量 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】乙烯在酸催化下水合制乙醇的反应机理、能量与反应进程的关系如图所示。下列说法正确的是
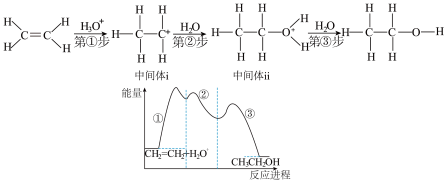

| A.由图可知,总反应为放热反应,所以不需加热就能进行 |
| B.第①步反应只断裂非极性键 |
| C.增大催化剂酸的浓度,可以加快总反应速率 |
| D.中间体i比中间体ii更稳定 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】通过以下反应可获得新型能源二甲醚( )。下列说法不正确的是
)。下列说法不正确的是
①
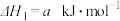
②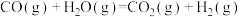
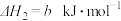
③
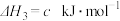
④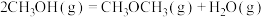
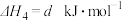
 )。下列说法不正确的是
)。下列说法不正确的是①

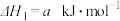
②
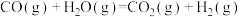
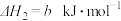
③

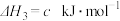
④
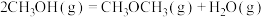
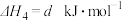
| A.反应①②为反应③提供原料气 |
B.反应③也是 资源化利用的方法之一 资源化利用的方法之一 |
C.反应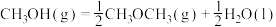 的 的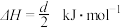 |
D.反应 的 的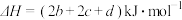 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】已知:在标准压强(101kPa)、298K下,由最稳定的单质合成1mol物质B的反应焓变,叫作物质B的标准摩尔生成焓,用 表示。部分物质的
表示。部分物质的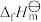 如图所示。
如图所示。 、
、 、
、 的标准摩尔生成焓为0.下列有关判断正确的是
的标准摩尔生成焓为0.下列有关判断正确的是
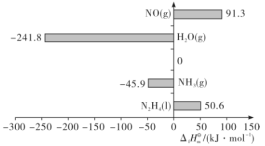
 表示。部分物质的
表示。部分物质的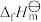 如图所示。
如图所示。 、
、 、
、 的标准摩尔生成焓为0.下列有关判断正确的是
的标准摩尔生成焓为0.下列有关判断正确的是
A.2mol 的键能大于1mol 的键能大于1mol 与1mol 与1mol 的键能之和 的键能之和 |
| B.根据图中信息,可判断热稳定性肼大于氨 |
C.0.5mol 和1.5mol 和1.5mol 合成氨,正反应的活化能一定大于 合成氨,正反应的活化能一定大于 |
D.NO与 反应的热化学方程式为 反应的热化学方程式为  |
您最近半年使用:0次
【推荐1】常温下,将一定量的铁粉加入到50 mL 10 mol·L-1硝酸中,待其充分反应后,收集到的气体换算成标准状况下的体积为4.2 L,所得溶液能够使淀粉碘化钾溶液变蓝,该溶液也能使酸性高锰酸钾褪色。下列说法正确的是
| A.铁与硝酸的反应是吸热反应 | B.生成的气体一定为NO |
| C.反应后硝酸可能有剩余 | D.所得溶液中一定含有Fe2+ |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列实验操作、实验现象及解释或结论都正确且有因果关系的是
| 选项 | 实验操作 | 实验现象 | 解释或结论 |
| A | 工业上用SiO2与焦炭在高温条件制备粗硅 | 生成可燃性气体,得到固体粗硅 | 非金属性:C>Si |
| B | 常温下,用pH计分别测定等体积1mol·L−1 CH3COONH4溶液和0.1mol·L−1 CH3COONH4溶液的pH | 测得pH都等于7 | 同温下,不同浓度的CH3COONH4溶液中水的电离程度相同 |
| C | 向两支试管中各加入4mL 0.01mol·L−1 KMnO4溶液和4mL 0.1mol·L−1 KMnO4溶液,再分别通入足量SO2,分别记录溶液褪色所需的时间 | 0.1mol·L−1 KMnO4溶液褪色所需时间更短 | 其他条件相同时,增大反应物浓度,反应速率增大 |
| D | 往烧杯中加入约20g研细的Ba(OH)2·8H2O晶体和10gNH4Cl晶体,并将烧杯放在滴有水的玻璃片上,用玻璃棒迅速搅拌 | 有刺激性气味气体生成,烧杯底部结冰,与玻璃片粘在一起 | 吸热反应不一定需要加热才能进行 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
【推荐1】CO与N2O气体均会造成环境污染,研究表明二者可在Pt2O+表面转化为无害气体N2和CO2,其反应过程中的能量变化如图所示。下列说法错误的是
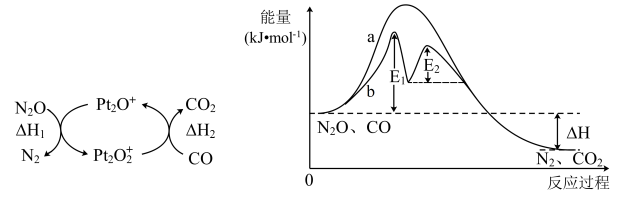

| A.使用催化剂可改变反应历程,降低反应活化能 |
| B.有催化剂条件下,E1时的反应速率比E2慢 |
| C.N2O(g)+CO(g)=N2(g)+CO2(g) △H=△H1+△H2 |
D.Pt2O+是反应的中间体,Pt2O 是反应的催化剂 是反应的催化剂 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】研究表明N2O与CO在Fe+作用下发生可逆反应的能量变化及反应历程如图所示。下列说法不正确 的是
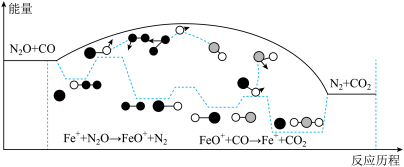

| A.反应中Fe+是催化剂,FeO+是中间产物 |
| B.总反应速率由反应②的速率决定 |
| C.反应①②均为放热反应 |
| D.当有14gN2生成时,转移1mole- |
您最近半年使用:0次