汽车剧烈碰撞时,安全气囊中发生反应:10NaN3+2KNO3=K2O+5Na2O+16N2。若氧化产物比还原产物多24.5g,则下列判断正确的是
| A.反应过程中KNO3被氧化 | B.反应生成的N2的总质量为28g |
| C.氧化产物与还原产物的质量比为1:15 | D.该反应一共转移10个电子 |
更新时间:2022/01/10 18:07:21
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】据统计,城市机动车辆每年以15%至20%的速度增长,汽车在剧烈碰撞时,安全气囊中发生反应: 。下列判断正确的是
。下列判断正确的是
 。下列判断正确的是
。下列判断正确的是| A.还原剂与氧化产物的物质的量之比为3:2 |
B. 是只含有离子键的离子化合物 是只含有离子键的离子化合物 |
C.当转移1mol电子时,可以得到35.84L |
D.每生成3.2mol ,则有0.4mol ,则有0.4mol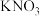 被还原 被还原 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】单晶硅是现代信息技术的基础材料。工业上制备硅的反应原理为 ,下列说法不正确的是
,下列说法不正确的是
 ,下列说法不正确的是
,下列说法不正确的是| A.该反应为置换反应 | B. 是氧化剂 是氧化剂 |
| C.1molC参加反应转移4mol电子 | D.单晶硅是良好的半导体材料 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】实验是探究物质性质的重要方法,下列实验中,根据操作和现象得出的结论正确的是
| 选项 | 操作 | 现象 | 结论 |
| A | 向麦芽糖溶液中加少量稀硫酸,加热一段时间,冷却后加过量NaOH溶液至碱性,再加银氨溶液,水浴加热 | 出现银镜 | 麦芽糖的水解产物具有还原性 |
| B | 在烧瓶中加入木炭颗粒与浓硝酸,然后加热 | 烧瓶中出现红棕色气体 | 木炭具有还原性,能还原 |
| C | 向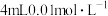 酸性 酸性 溶液中加入 溶液中加入 溶液 溶液 | 产生气泡的速率先增大后减小 | 该反应一定为放热反应 |
| D | 向 溶液中加入 溶液中加入 溶液,再加入苯,振荡后静置 溶液,再加入苯,振荡后静置 | 上层呈紫红色,下层有白色沉淀生成 |  可以氧化 可以氧化 ,白色沉淀可能为 ,白色沉淀可能为 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】氧化还原反应实际上包含氧化和还原两个过程.下面是一个还原过程的反应式:NO3-+4H++3e-═NO↑+2H2O,KMnO4、Na2CO3、Cu2O、FeSO4四种物质中有物质(甲)能使上述还原过程发生。则下列说法中正确的是
| A.物质甲可能是KMnO4 |
| B.反应中只体现了硝酸的强氧化性 |
| C.氧化过程的反应式一定为Cu2O-2e-+2H+═2Cu2++H2O |
| D.反应中若产生3.0 g气体,则转移电子数约为0.3×6.02×1023 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】黑火药爆炸时的反应为S+2KNO3+3C=K2S+N2↑+3CO2↑,下列说法正确的是
| A.S发生氧化反应 |
| B.S和KNO3都作氧化剂 |
| C.参加反应的氧化剂与还原剂的物质的量之比为1∶3 |
| D.生成1molN2时,转移10mol电子 |
您最近一年使用:0次
【推荐2】高锰酸钾溶液在酸性条件下可以与硫酸亚铁反应,化学方程式如下:KMnO4+FeSO4+H2SO4→K2SO4+MnSO4+Fe2(SO4)3+H2O(未配平)。下列说法正确的是
| A.FeSO4没有氧化性 |
| B.生成1mol水时,转移1.25mol电子 |
| C.氧化剂和还原剂物质的量之比为5∶1 |
| D.KMnO4是氧化剂,Fe2(SO4)3是还原产物 |
您最近一年使用:0次

 和
和 为动力源,发生反应:
为动力源,发生反应: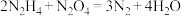 ,反应温度可高达2700℃,对于该反应,下列说法中正确的是
,反应温度可高达2700℃,对于该反应,下列说法中正确的是 、
、 具有杀菌、消毒、漂白等作用。硫磺、黄铁矿(
具有杀菌、消毒、漂白等作用。硫磺、黄铁矿( )可作为工业制硫酸的原料,辉铜矿(
)可作为工业制硫酸的原料,辉铜矿( )煅烧时可发生反应:
)煅烧时可发生反应: 。
。 直接排放会造成环境污染,可将其转化或用石灰乳、
直接排放会造成环境污染,可将其转化或用石灰乳、 等物质进行回收再利用。
等物质进行回收再利用。 的水溶液反应可制备硒。下列说法不正确的是
的水溶液反应可制备硒。下列说法不正确的是
 ,反应共转移6mol电子
,反应共转移6mol电子 MnCl2+2H2O+Cl2↑,下列说法错误的是
MnCl2+2H2O+Cl2↑,下列说法错误的是

