阅读下列科普短文并填空:
海洋约占地球表面积的71%,其中水资源和其他化学资源具有巨大的开发潜力。海水中含有多种盐类,如①NaCl、②MgSO4等。目前,经海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和③食盐水用以生产④NaOH、⑤NaHCO3、⑥Na、⑦Cl2、⑧盐酸等,苦卤经过氯气氧化,热空气吹出、⑨SO2吸收等一系列操作可获得Br2。海水淡化与化工生产、能源开发等相结合已经成为海水综合利用的重要方向。
(1)上述标有序号的物质中属于电解质的是___ (填序号,下同);属于非电解质的是___ ;能导电的物质是____ 。
(2)写出⑤溶于水的电离方程式:___ 。实验产生的SO2可用足量④吸收,写出对应的离子方程式:___ 。
(3)海水提溴的过程中涉及的反应有2Br-+Cl2=Br2+2Cl-,2H2O+SO2+Br2=4H++2Br-+ ,根据上述反应可判断Cl-、Br-、SO2的还原性由强到弱的顺序为
,根据上述反应可判断Cl-、Br-、SO2的还原性由强到弱的顺序为___ 。
海洋约占地球表面积的71%,其中水资源和其他化学资源具有巨大的开发潜力。海水中含有多种盐类,如①NaCl、②MgSO4等。目前,经海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和③食盐水用以生产④NaOH、⑤NaHCO3、⑥Na、⑦Cl2、⑧盐酸等,苦卤经过氯气氧化,热空气吹出、⑨SO2吸收等一系列操作可获得Br2。海水淡化与化工生产、能源开发等相结合已经成为海水综合利用的重要方向。
(1)上述标有序号的物质中属于电解质的是
(2)写出⑤溶于水的电离方程式:
(3)海水提溴的过程中涉及的反应有2Br-+Cl2=Br2+2Cl-,2H2O+SO2+Br2=4H++2Br-+
 ,根据上述反应可判断Cl-、Br-、SO2的还原性由强到弱的顺序为
,根据上述反应可判断Cl-、Br-、SO2的还原性由强到弱的顺序为
更新时间:2022-03-01 11:16:56
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】现有9种物质:①铜;②稀硫酸;③HCl;④乙醇;⑤NaCl;⑥H2S;⑦CaCO3;⑧蔗糖;⑨Fe(OH)3。
(1)属于非电解质的有___________ (填序号,下同)。
(2)属于电解质,但液态时不能导电的是___________ 。
(3)既不是电解质,也不是非电解质,但本身能导电的是___________ 。
(4)属于强电解质的是___________ 。
(5)分别写出③、⑥、⑨的电离方程式:___________ 、___________ 、___________ 。
(1)属于非电解质的有
(2)属于电解质,但液态时不能导电的是
(3)既不是电解质,也不是非电解质,但本身能导电的是
(4)属于强电解质的是
(5)分别写出③、⑥、⑨的电离方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】现有10种物质:①铜 ②稀硫酸 ③氯化氢 ④氨气 ⑤空气 ⑥二氧化碳 ⑦酒精 ⑧氯化钠 ⑨硫酸钡 ⑩氯气,按照下表中提示的信息,把符合左栏条件的物质的化学式或名称填入右栏相应的位置。
| 序号 | 符合的条件 | 物质的化学式或名称 |
| (1) | 混合物 | |
| (2) | 电解质,但熔融状态下并不导电 | |
| (3) | 电解质,但难溶于水 | |
| (4) | 非电解质 | |
| (5) | 既不是电解质,也不是非电解质,但本身能导电 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】现有以下物质:①氢氧化钡②Cu③BaCO3④Fe(OH)3胶体⑤酒精⑥NH3⑦稀硫酸⑧Al2(SO4)3
(1)以上物质中属于混合物的是_________ (填序号,下空同),属于电解质的是_________ ,能导电的是_________
(2)向④中逐滴滴加⑦,可观察到的现象是_________ 。
(3)写出物质⑧在水中的电离方程式_________ 。
(4)写出物质①和⑦反应的离子方程式_________ 。
(5)8.5g⑥约含有_________ 个分子,含_________ mol质子。
(6)将34.2g⑧溶于水配成100mL溶液,从该溶液中取出10mL,其中 的物质的量浓度为
的物质的量浓度为_________ 。
(1)以上物质中属于混合物的是
(2)向④中逐滴滴加⑦,可观察到的现象是
(3)写出物质⑧在水中的电离方程式
(4)写出物质①和⑦反应的离子方程式
(5)8.5g⑥约含有
(6)将34.2g⑧溶于水配成100mL溶液,从该溶液中取出10mL,其中
 的物质的量浓度为
的物质的量浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】完成下列问题
(1)研究物质性质及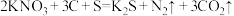 。其中作氧化剂的是
。其中作氧化剂的是_______ (填化学式)。
(2)中国古代著作中有“银针验毒”的记录,其原理为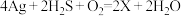 ,则X的化学式是
,则X的化学式是_______ ,其中 在该反应中
在该反应中_______ (填标号)。
A.作氧化剂
B.作还原剂
C.既是氧化剂又是还原剂
D.既不是氧化剂又不是还原剂
(3)按如图所示操作,充分反应后:
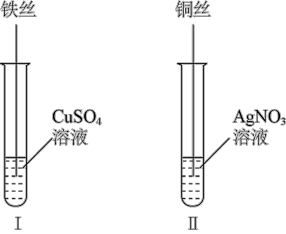
Ⅰ中铁丝上观察到的现象是_______ 。结合Ⅰ、Ⅱ实验现象可知Fe2+、Cu2+、Ag+的氧化性由强到弱的顺序为_______ 。
(4)取少量Fe2O3粉末溶于适量盐酸,得到黄色溶液,用此溶液进行以下实验:在烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中加入制取的黄色溶液5~6滴,继续煮沸至液体呈_______ 色,停止加热,用激光笔照射烧杯中的液体,可以观察到液体中_______ ,用这个实验可以区别_______ 和_______ 。
(1)研究物质性质及
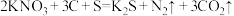 。其中作氧化剂的是
。其中作氧化剂的是(2)中国古代著作中有“银针验毒”的记录,其原理为
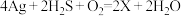 ,则X的化学式是
,则X的化学式是 在该反应中
在该反应中A.作氧化剂
B.作还原剂
C.既是氧化剂又是还原剂
D.既不是氧化剂又不是还原剂
(3)按如图所示操作,充分反应后:

Ⅰ中铁丝上观察到的现象是
(4)取少量Fe2O3粉末溶于适量盐酸,得到黄色溶液,用此溶液进行以下实验:在烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中加入制取的黄色溶液5~6滴,继续煮沸至液体呈
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Ⅰ.根据①~④四个反应,回答下列问题:
①Cl2+2KI=2KCl+I2
②2FeCl2+Cl2=2FeCl3
③2FeCl3+2HI=2FeCl2+2HCl+I2
④H2S+I2=S+2HI
(1)反应①的反应类型为_______。
(2)对于反应②,还原剂与氧化剂的质量之比为_______ 。
(3)对于反应③,当有1个Fe2+生成时,转移电子数目为_______ 。
(4)根据上述四个反应可判断出Cl2、I2、Fe3+、H2S四种物质的氧化性强弱顺序为_______ 。
Ⅱ.根据氧化还原反应的规律和概念填写:
(5)人体血红蛋白分子中含有Fe2+,正是这些Fe2+使血红蛋白分子具有载氧功能。亚硝酸钠(NaNO2)可将人体血红蛋白中的Fe2+转化为Fe3+,生成高铁血红蛋白而丧失与氧气的结合能力,反应过程中Fe2+发生_______ 反应,说明亚硝酸钠具有_______ 性;误食亚硝酸钠中毒,可服维生素C缓解,说明维生素C具有_______ 性。
(6)二氧化氯(ClO2)是一种在水处理等方面有广泛应用的高效安全消毒剂。与Cl2相比,ClO2不但具有更显著的杀菌能力,而且不会产生对人体有潜在危害的有机氯代物。可以用下列方法制备ClO2:2NaClO3+H2O2+H2SO4=2ClO2↑+Na2SO4+O2↑+2H2O。被氧化的物质是_______ ,若反应中转移1个电子,则产生的ClO2分子的数目为_______ 。
①Cl2+2KI=2KCl+I2
②2FeCl2+Cl2=2FeCl3
③2FeCl3+2HI=2FeCl2+2HCl+I2
④H2S+I2=S+2HI
(1)反应①的反应类型为_______。
| A.置换反应 | B.复分解反应 | C.化合反应 | D.氧化还原反应 |
(3)对于反应③,当有1个Fe2+生成时,转移电子数目为
(4)根据上述四个反应可判断出Cl2、I2、Fe3+、H2S四种物质的氧化性强弱顺序为
Ⅱ.根据氧化还原反应的规律和概念填写:
(5)人体血红蛋白分子中含有Fe2+,正是这些Fe2+使血红蛋白分子具有载氧功能。亚硝酸钠(NaNO2)可将人体血红蛋白中的Fe2+转化为Fe3+,生成高铁血红蛋白而丧失与氧气的结合能力,反应过程中Fe2+发生
(6)二氧化氯(ClO2)是一种在水处理等方面有广泛应用的高效安全消毒剂。与Cl2相比,ClO2不但具有更显著的杀菌能力,而且不会产生对人体有潜在危害的有机氯代物。可以用下列方法制备ClO2:2NaClO3+H2O2+H2SO4=2ClO2↑+Na2SO4+O2↑+2H2O。被氧化的物质是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】氧化还原反应是一类重要的反应。
(1)已知反应Cu+2Fe3+=Cu2++2Fe2+,氧化性Fe3+____ Cu2+(填“<"或“> ")。
(2)已知钢在常温下能被HNO3溶解,反应方程式为: 3Cu+8HNO3= 3Cu(NO3)2+ 2NO↑+4H2O
①请将上述反应改成离子方程式,并用单线桥法表示电子得失的方向和数目__________
②若生成448mL的NO(标准状况下),则该过程中转移的电子是_______ mol
③被还原的硝酸占参加反应硝酸的比例为____________ 。
(3)在xR2++yH++O2=mR3++nH2O的离子方程式中,对系数m和R2+、R3+判断正确的是______ 。
A m=y,R3+是还原剂 B m=2y,R2+被氧化
C m=2,R3+是氧化剂 D m=4,R2+是还原剂
(4)实验室所用少量氯气是用下列方法制取的4HCl(浓)+MnO2 Cl2↑+MnCl2+2H2O其中氧化剂与还原剂的物质的量之比
Cl2↑+MnCl2+2H2O其中氧化剂与还原剂的物质的量之比_____ ,写出该反应的离子方程式__________
(1)已知反应Cu+2Fe3+=Cu2++2Fe2+,氧化性Fe3+
(2)已知钢在常温下能被HNO3溶解,反应方程式为: 3Cu+8HNO3= 3Cu(NO3)2+ 2NO↑+4H2O
①请将上述反应改成离子方程式,并用单线桥法表示电子得失的方向和数目
②若生成448mL的NO(标准状况下),则该过程中转移的电子是
③被还原的硝酸占参加反应硝酸的比例为
(3)在xR2++yH++O2=mR3++nH2O的离子方程式中,对系数m和R2+、R3+判断正确的是
A m=y,R3+是还原剂 B m=2y,R2+被氧化
C m=2,R3+是氧化剂 D m=4,R2+是还原剂
(4)实验室所用少量氯气是用下列方法制取的4HCl(浓)+MnO2
 Cl2↑+MnCl2+2H2O其中氧化剂与还原剂的物质的量之比
Cl2↑+MnCl2+2H2O其中氧化剂与还原剂的物质的量之比
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】Ⅰ.金属元素的原子结构决定了金属元素的性质、在自然界中的存在形式及冶炼方法。
(1)金属在自然界中大多以化合物的形式存在,在这些金属化合物中,金属元素都显___________ (填“正”或“负”)化合价。
(2)金属的冶炼方法可以分为:A.焦炭法;B.热分解法;C.活泼金属置换法;D.电解法。
请从上述四种方法中选择相应的序号填入表中空格:
(3)写出Al与Cr2O3反应的化学方程式:___________ 。
Ⅱ.以下为工业从海水中提取液溴的流程图:
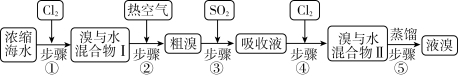
已知:溴的沸点为59℃,微溶于水,有毒性。请回答:
(4)用热空气能将溴单质吹出的原因是___________ 。
(5)从“溴与水混合物Ⅰ”到“溴与水混合物Ⅱ”的目的是___________ 。
(1)金属在自然界中大多以化合物的形式存在,在这些金属化合物中,金属元素都显
(2)金属的冶炼方法可以分为:A.焦炭法;B.热分解法;C.活泼金属置换法;D.电解法。
请从上述四种方法中选择相应的序号填入表中空格:
| 高炉炼铁 | 湿法炼铜 | 铝热法炼铬 | 工业上冶炼钾 |
| ① | ② | ③ | ④ |
Ⅱ.以下为工业从海水中提取液溴的流程图:

已知:溴的沸点为59℃,微溶于水,有毒性。请回答:
(4)用热空气能将溴单质吹出的原因是
(5)从“溴与水混合物Ⅰ”到“溴与水混合物Ⅱ”的目的是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】研究和开发海水及其综合利用关系到人类的可持续发展。甲、乙两实验小组分别探索从海水中制取金属镁和单质溴的实验。
(1)甲实验小组的流程如图1。
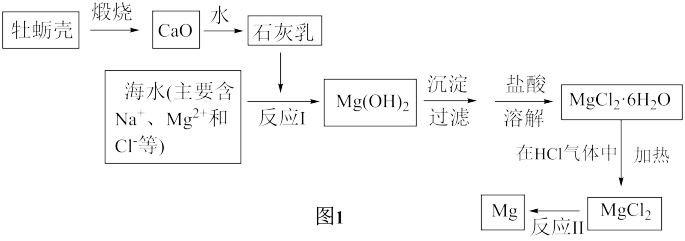
①制备石灰乳的化学反应方程式是___ 、___ 。
②写出反应Ⅰ的离子反应方程式___ 。
③反应Ⅱ是工业冶炼金属镁的反应原理,写出反应Ⅱ的化学反应方程式___ 。
(2)乙实验小组的流程如图2。

①分液漏斗使用前需检漏,检漏的方法为___ ,在步骤③中,萃取后分液漏斗内观察到的现象是___ 。
②写出步骤①发生反应的离子方程式___ ;写出步骤②发生反应的化学方程式___ 。
③在步骤③中,分离出溴单质的实验操作的名称是分液和___ ,后一实验操作用到的玻璃仪器有:___ 。
④在步骤①和步骤②之间设计了通入空气和水蒸气吹出的操作步骤的目的是___ 。
(3)图3各烧杯中盛有海水,铁在其中被腐蚀由快到慢的顺序为___ 。(填序号)

(1)甲实验小组的流程如图1。

①制备石灰乳的化学反应方程式是
②写出反应Ⅰ的离子反应方程式
③反应Ⅱ是工业冶炼金属镁的反应原理,写出反应Ⅱ的化学反应方程式
(2)乙实验小组的流程如图2。

①分液漏斗使用前需检漏,检漏的方法为
②写出步骤①发生反应的离子方程式
③在步骤③中,分离出溴单质的实验操作的名称是分液和
④在步骤①和步骤②之间设计了通入空气和水蒸气吹出的操作步骤的目的是
(3)图3各烧杯中盛有海水,铁在其中被腐蚀由快到慢的顺序为

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)海水淡化的方法主要有:__________ 、______________ 、_____________ 。
(2)金属冶炼的实质是金属化合物中的金属离子得电子被________ (填“氧化”或“还原”)为金属单质的过程,写出冶炼金属钠的化学方程式:_________________________ 。
(3)实验室里,常用加热铵盐和碱的混合物的方法制氨,写出实验室制氨的化学方程式:________ ;氨溶于水得氨水,氨水呈___________ 性(填“酸”或“碱”); 密度比水_______ ;(填“大”或“小”)写出向AlCl3溶液中滴加过量氨水的离子方程式:_________________________ 。
(4)溴主要以Br-形式存在于海水中,工业上制备的Br2的操作步骤为:
①一定条件下,将Cl2通入浓缩的海水中,生成Br2
②利用热空气将Br2吹出,并用浓Na2CO3溶液吸收,生成NaBr、NaBrO3等
③用硫酸酸化步骤②得到的混合物。
Br2可用热空气吹出,其原因是:_________ ;步骤③所发生的化学反应方程式为:_______________ 。
(2)金属冶炼的实质是金属化合物中的金属离子得电子被
(3)实验室里,常用加热铵盐和碱的混合物的方法制氨,写出实验室制氨的化学方程式:
(4)溴主要以Br-形式存在于海水中,工业上制备的Br2的操作步骤为:
①一定条件下,将Cl2通入浓缩的海水中,生成Br2
②利用热空气将Br2吹出,并用浓Na2CO3溶液吸收,生成NaBr、NaBrO3等
③用硫酸酸化步骤②得到的混合物。
Br2可用热空气吹出,其原因是:
您最近一年使用:0次



