2021年12月13日从天津市疫情防控指挥部获悉,中国内地首次发现新冠病毒“奥密克戎”变异株。当下疫情对生产生活仍然影响极大,人们认识到日常杀菌消毒的重要性,其中含氯消毒剂在生产生活中有着广泛的用途。回答下列问题:
(1)写出实验室中制取氯气的离子方程式:___________ 。
(2)已知 与浓盐酸反应的化学方程式:
与浓盐酸反应的化学方程式: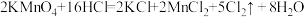 ,该反应也可以用来制取氯气,
,该反应也可以用来制取氯气,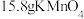 能和
能和___________ 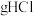 发生上述反应,其中有
发生上述反应,其中有___________ 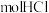 被氧化,产生的
被氧化,产生的 在标准状况下的体积为
在标准状况下的体积为___________ L。
(3)实验室还可以利用如下反应制取氯气: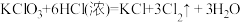 。若制取标准状况下
。若制取标准状况下 氯气,反应过程中转移电子的物质的量为
氯气,反应过程中转移电子的物质的量为___________ 。
(1)写出实验室中制取氯气的离子方程式:
(2)已知
 与浓盐酸反应的化学方程式:
与浓盐酸反应的化学方程式: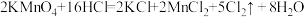 ,该反应也可以用来制取氯气,
,该反应也可以用来制取氯气,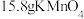 能和
能和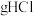 发生上述反应,其中有
发生上述反应,其中有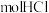 被氧化,产生的
被氧化,产生的 在标准状况下的体积为
在标准状况下的体积为(3)实验室还可以利用如下反应制取氯气:
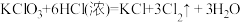 。若制取标准状况下
。若制取标准状况下 氯气,反应过程中转移电子的物质的量为
氯气,反应过程中转移电子的物质的量为
更新时间:2022/03/01 18:08:54
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】化工厂常用氨水检验管道是否漏氯气,其反应式为3Cl2+8NH3=6NH4Cl+N2,当有160.5gNH4Cl产生时,被氧化的氨气是_______ 。
您最近一年使用:0次
【推荐2】中国传统文化是人类文明的瑰宝,古代文献中记载了大量古代化学的研究成果。回答下面问题:
(1)我国最原始的陶瓷约出现在距今12000年前,制作瓷器所用的原料是高岭土,其晶体化学式是Al4[Si4O10](OH)8,用氧化物表示其组成为______________ 。
(2)《本草纲目》中记载:“(火药)乃焰消( KNO3)、硫磺、杉木炭所合,以为烽燧铳机诸药者。”反应原理为:S+2KNO3+3C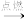 K2S+N2↑+3CO2↑,该反应的氧化剂是
K2S+N2↑+3CO2↑,该反应的氧化剂是_________ ,反应转移4mol电子时,被S氧化的C有____________ mol。
(3)我国古代中药学著作《新修本草》记载的药物有844种,其中有关“青矾”的描述为:“本来绿色,新出窟未见风者,正如瑁璃…烧之赤色…。”我国早期科技丛书《物理小适-金石类》 记载有加热青矾时的景象:“青矾厂气熏人,衣服当之易烂,载木不盛。”青矾就是绿矾( FeSO4·7H2O)。根据以上信息,写出“青矾”受热分解的化学方程式_____________________________________________________ 。
(1)我国最原始的陶瓷约出现在距今12000年前,制作瓷器所用的原料是高岭土,其晶体化学式是Al4[Si4O10](OH)8,用氧化物表示其组成为
(2)《本草纲目》中记载:“(火药)乃焰消( KNO3)、硫磺、杉木炭所合,以为烽燧铳机诸药者。”反应原理为:S+2KNO3+3C
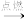 K2S+N2↑+3CO2↑,该反应的氧化剂是
K2S+N2↑+3CO2↑,该反应的氧化剂是(3)我国古代中药学著作《新修本草》记载的药物有844种,其中有关“青矾”的描述为:“本来绿色,新出窟未见风者,正如瑁璃…烧之赤色…。”我国早期科技丛书《物理小适-金石类》 记载有加热青矾时的景象:“青矾厂气熏人,衣服当之易烂,载木不盛。”青矾就是绿矾( FeSO4·7H2O)。根据以上信息,写出“青矾”受热分解的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】用电弧法合成碳纳米管,常伴有大量杂质——碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯,其反应的化学方程式为:
2K2Cr2O7+3C+8H2SO4=2Cr2(SO4)3+2K2SO4+8H2O+3CO2↑。
(1)用双线桥法表示出电子转移方向和数目___________ 。
(2)此反应的氧化产物和还原产物的物质的量之比为___________ 。
(3)要使10mL1.0mol·L-1K2Cr2O7溶液被还原,至少要加入___________ mL2.0mol·L-1的H2SO4溶液,消耗C的质量为___________ g。
(4)若产生6.72LCO2(标准状况下)气体,该反应转移电子的物质的量为___________ mol。
(5)H2SO4在上述反应中表现出来的性质是___________。
2K2Cr2O7+3C+8H2SO4=2Cr2(SO4)3+2K2SO4+8H2O+3CO2↑。
(1)用双线桥法表示出电子转移方向和数目
(2)此反应的氧化产物和还原产物的物质的量之比为
(3)要使10mL1.0mol·L-1K2Cr2O7溶液被还原,至少要加入
(4)若产生6.72LCO2(标准状况下)气体,该反应转移电子的物质的量为
(5)H2SO4在上述反应中表现出来的性质是___________。
| A.酸性 | B.氧化性 | C.吸水性 | D.脱水性 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】“价—类”二维图是预测物质性质的重要思维工具。下图为氯及其化合物的“价—类”二维图,回答下列问题:
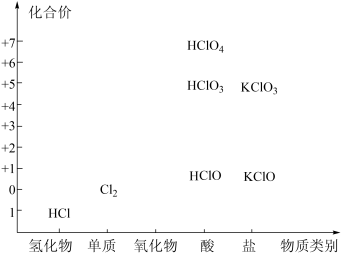
(1)上图HCl、 和HClO中,属于电解质的是
和HClO中,属于电解质的是_______ (填化学式)。
(2)写出 在水中的电离方程式
在水中的电离方程式_______ 。
(3)写出实验室用浓盐酸和 制取
制取 的化学方程式
的化学方程式_______ 。
(4)根据上图氯元素的化合价判断,HClO在反应中既可作氧化剂,又可作还原剂。当它作氧化剂时,理论上可能被还原为_______(填标号)。
(5) 和浓盐酸反应也可制得
和浓盐酸反应也可制得 ,该反应的化学方程式为:
,该反应的化学方程式为: 。
。
①该反应中参加反应的HCl和被氧化的HCl的物质的量之比为_______ 。
②请用“双线桥”法标明该反应电子转移的方向和数目_______ 。
(6)高铁酸钾 是一种水处理剂,易溶于水,可对水杀菌消毒。一定条件下,向KClO与KOH的混合溶液中加入
是一种水处理剂,易溶于水,可对水杀菌消毒。一定条件下,向KClO与KOH的混合溶液中加入 溶液,可得到
溶液,可得到 和KCl,该反应的离子方程式为
和KCl,该反应的离子方程式为_______ 。

(1)上图HCl、
 和HClO中,属于电解质的是
和HClO中,属于电解质的是(2)写出
 在水中的电离方程式
在水中的电离方程式(3)写出实验室用浓盐酸和
 制取
制取 的化学方程式
的化学方程式(4)根据上图氯元素的化合价判断,HClO在反应中既可作氧化剂,又可作还原剂。当它作氧化剂时,理论上可能被还原为_______(填标号)。
A. | B. | C.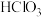 | D. |
 和浓盐酸反应也可制得
和浓盐酸反应也可制得 ,该反应的化学方程式为:
,该反应的化学方程式为: 。
。①该反应中参加反应的HCl和被氧化的HCl的物质的量之比为
②请用“双线桥”法标明该反应电子转移的方向和数目
(6)高铁酸钾
 是一种水处理剂,易溶于水,可对水杀菌消毒。一定条件下,向KClO与KOH的混合溶液中加入
是一种水处理剂,易溶于水,可对水杀菌消毒。一定条件下,向KClO与KOH的混合溶液中加入 溶液,可得到
溶液,可得到 和KCl,该反应的离子方程式为
和KCl,该反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】人们可以利用氧化还原反应研究物质的性质、实现物质的转化。
(1)过氧化钠可用于呼吸面具和潜水艇里的氧气供给_______ (用一个化学方程式表示)。
(2)实验室利用二氧化锰和浓盐酸反应制备Cl2的离子方程式为_______ ,此反应中浓盐酸体现了_______ 性质。
(3)浓硫酸与蔗糖进行“黑面包”实验时产生大量气体的化学方程式_______ 。
(4)将5%H2O2溶液滴入酸性KMnO4溶液中,观察到_______ ,此反应中H2O2做_______ 剂(填“氧化”或“还原)。若将5%H2O2溶液滴入FeCl2溶液中,则观察到_______ ,此反应中H2O2发生_______ 反应(填“氧化”或“还原”)。
(5)工业高炉炼铁时常以赤铁矿(主要成分为Fe2O3)和焦炭(主要成分为碳)为原料,而炼铁过程中实际起作用的是CO,请写出高炉炼铁的化学方程式_______ 。
(1)过氧化钠可用于呼吸面具和潜水艇里的氧气供给
(2)实验室利用二氧化锰和浓盐酸反应制备Cl2的离子方程式为
(3)浓硫酸与蔗糖进行“黑面包”实验时产生大量气体的化学方程式
(4)将5%H2O2溶液滴入酸性KMnO4溶液中,观察到
(5)工业高炉炼铁时常以赤铁矿(主要成分为Fe2O3)和焦炭(主要成分为碳)为原料,而炼铁过程中实际起作用的是CO,请写出高炉炼铁的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】实验室制备氯气的方法是用软锰矿(主要成分为MnO2)与浓盐酸在加热条件下反应制得,也可以用高锰酸钾、氯酸钾或是重铬酸钾(K2Cr2O7 )等与浓盐酸反应制得。
(1)实验室用软锰矿与浓盐酸加热制备氯气的反应的化学方程式为_______ 。
(2)若用足量浓盐酸与软锰矿共热制得0.15mol氯气,则在剩余溶液中加入足量AgNO3溶液得到的沉淀的物质的量_______ (填“大于”。“小于”或“等于”)0.3mol,请说明理由:_______ 。
(3)如果用重铬酸钾(K2Cr2O7)代替软锰矿与浓盐酸反应制备氯气,其化学方程式为K2Cr2O7 +14HCl(浓)=2KCl+ 2CrCl3+3Cl2↑+7H2O。该反应的离子方程式为_______ ,反应中被还原的元素是_______ (填元素符号),氧化性: K2Cr2O7_______ (填“>”、“<”或“=”)Cl2 ;该反应中作还原剂的HCl与表现酸性的HCl的物质的量之比为_______ 。
(1)实验室用软锰矿与浓盐酸加热制备氯气的反应的化学方程式为
(2)若用足量浓盐酸与软锰矿共热制得0.15mol氯气,则在剩余溶液中加入足量AgNO3溶液得到的沉淀的物质的量
(3)如果用重铬酸钾(K2Cr2O7)代替软锰矿与浓盐酸反应制备氯气,其化学方程式为K2Cr2O7 +14HCl(浓)=2KCl+ 2CrCl3+3Cl2↑+7H2O。该反应的离子方程式为
您最近一年使用:0次
【推荐1】运用化学反应原理研究硫单质及其化合物的反应,对生产、生活、环境保护等领域有着重要的意义。
(1)工业上采用 催化还原
催化还原 ,不仅可以消除
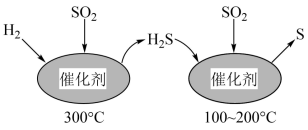
,不仅可以消除 污染,还可得到单质S。反应分两步完成,如图所示,
污染,还可得到单质S。反应分两步完成,如图所示, 催化还原
催化还原 第一步反应的化学方程式为
第一步反应的化学方程式为___________ 。
(2)工业上常用 溶液对燃煤烟气进行脱硫、脱硝。
溶液对燃煤烟气进行脱硫、脱硝。
已知 溶液具有强氧化性,酸性条件下
溶液具有强氧化性,酸性条件下 发生歧化反应生成
发生歧化反应生成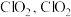 易溶于水,具有强氧化性,可氧化
易溶于水,具有强氧化性,可氧化 。
。
①实验室模拟脱硫过程:先加稀硫酸调节 吸收液的
吸收液的 为5,再向其中通入含
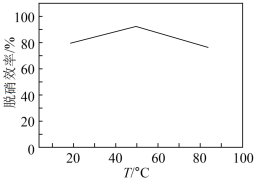
为5,再向其中通入含 的模拟烟气,测得脱硫效率(即
的模拟烟气,测得脱硫效率(即 的吸收率)随温度变化的曲线如图所示。结合已知信息分析,温度大于
的吸收率)随温度变化的曲线如图所示。结合已知信息分析,温度大于 时,随温度升高脱硫效率下降的原因是
时,随温度升高脱硫效率下降的原因是___________ 。
②煤燃烧排放的烟气含有 和
和 ,采用
,采用 溶液作为吸收剂可同时对烟气进行脱硫、脱硝。将含有
溶液作为吸收剂可同时对烟气进行脱硫、脱硝。将含有 和
和 的烟气通入盛有
的烟气通入盛有 溶液的反应器中,反应一段时间后,测得溶液中离子浓度的有关数据如表(其他离子忽略不计):
溶液的反应器中,反应一段时间后,测得溶液中离子浓度的有关数据如表(其他离子忽略不计):
表中y=_______ 。若该溶液为 (吸收前后溶液体积不变),该过程转移的电子数为
(吸收前后溶液体积不变),该过程转移的电子数为______ mol。(写出计算过程)。
(1)工业上采用
 催化还原
催化还原 ,不仅可以消除
,不仅可以消除 污染,还可得到单质S。反应分两步完成,如图所示,
污染,还可得到单质S。反应分两步完成,如图所示, 催化还原
催化还原 第一步反应的化学方程式为
第一步反应的化学方程式为
(2)工业上常用
 溶液对燃煤烟气进行脱硫、脱硝。
溶液对燃煤烟气进行脱硫、脱硝。已知
 溶液具有强氧化性,酸性条件下
溶液具有强氧化性,酸性条件下 发生歧化反应生成
发生歧化反应生成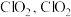 易溶于水,具有强氧化性,可氧化
易溶于水,具有强氧化性,可氧化 。
。①实验室模拟脱硫过程:先加稀硫酸调节
 吸收液的
吸收液的 为5,再向其中通入含
为5,再向其中通入含 的模拟烟气,测得脱硫效率(即
的模拟烟气,测得脱硫效率(即 的吸收率)随温度变化的曲线如图所示。结合已知信息分析,温度大于
的吸收率)随温度变化的曲线如图所示。结合已知信息分析,温度大于 时,随温度升高脱硫效率下降的原因是
时,随温度升高脱硫效率下降的原因是
②煤燃烧排放的烟气含有
 和
和 ,采用
,采用 溶液作为吸收剂可同时对烟气进行脱硫、脱硝。将含有
溶液作为吸收剂可同时对烟气进行脱硫、脱硝。将含有 和
和 的烟气通入盛有
的烟气通入盛有 溶液的反应器中,反应一段时间后,测得溶液中离子浓度的有关数据如表(其他离子忽略不计):
溶液的反应器中,反应一段时间后,测得溶液中离子浓度的有关数据如表(其他离子忽略不计):| 离子 |  |  |  |  |  |
浓度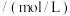 | 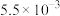 |  |  |  |  |
 (吸收前后溶液体积不变),该过程转移的电子数为
(吸收前后溶液体积不变),该过程转移的电子数为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】氧化还原反应知识的学习,为我们研究化学物质和化学反应提供了新的视角
(1)下列粒子中,只有还原性的是_______ 。①S2-②Fe2+③Fe3+④S⑤H+⑥Na+⑦Mg
(2)吸入人体内的氧有2%转化为氧化性极强的“活性氧”,它能加速人体衰老,被称为“生命杀手”,服用含硒元素(Se)的化合物亚硒酸钠(Na2SeO3),能消除人体内的活性氧,由此推断Na2SeO3的作用是_______ 。
(3)在Fe+4HNO3=Fe(NO3)3+NO↑+2H2O的反应中,HNO3表现了_______ 性,若生成的气体在标准状况下所占的体积为11.2L时,转移电子数为_______
(4)已知反应:①6HCl+KClO3=KCl+3H2O+3Cl2↑
②Cl2+2KI=2KCl+I2
③I2+Cl2+H2O→HIO3+HCl(未配平)
反应①中若有3mol盐酸参与反应,转移的电子数目为_______ ,对于反应③下列说法正确的是_______ 。
A.反应③中氧化剂和还原剂的物质的量之比为1∶5
B.结合反应②③,若将Cl2通入含有淀粉的KI溶液中,可能会观察到先变蓝后褪色
C.还原性由强到弱顺序:Cl->I-
D.氧化性由强到弱顺序:KClO3>Cl2>I2
(5)反应①是制取Cl2的方法,除此之外反应2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O也常用来制备Cl2,被氧化的HCl和参加反应的HCl的质量之比为_______ 。
(1)下列粒子中,只有还原性的是
(2)吸入人体内的氧有2%转化为氧化性极强的“活性氧”,它能加速人体衰老,被称为“生命杀手”,服用含硒元素(Se)的化合物亚硒酸钠(Na2SeO3),能消除人体内的活性氧,由此推断Na2SeO3的作用是
(3)在Fe+4HNO3=Fe(NO3)3+NO↑+2H2O的反应中,HNO3表现了
(4)已知反应:①6HCl+KClO3=KCl+3H2O+3Cl2↑
②Cl2+2KI=2KCl+I2
③I2+Cl2+H2O→HIO3+HCl(未配平)
反应①中若有3mol盐酸参与反应,转移的电子数目为
A.反应③中氧化剂和还原剂的物质的量之比为1∶5
B.结合反应②③,若将Cl2通入含有淀粉的KI溶液中,可能会观察到先变蓝后褪色
C.还原性由强到弱顺序:Cl->I-
D.氧化性由强到弱顺序:KClO3>Cl2>I2
(5)反应①是制取Cl2的方法,除此之外反应2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O也常用来制备Cl2,被氧化的HCl和参加反应的HCl的质量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】下面三个方法都可以用来制氯气:
①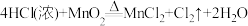
②
③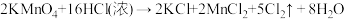
根据以上三个反应,回答下列有关问题:
(1)反应②的离子方程式为_______ 。
(2)反应②中,氧化产物与还原产物的质量比为_______ 。
(3)用双线桥法表示①中电子转移情况_______ 。
(4)若要制得相同质量的氯气,①②③反应中电子转移的数目之比为_______ 。
(5)已知反应④: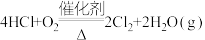 ,该反应也能制得氯气,则MnO2、O2、KMnO4三种物质氧化性由强到弱的顺序为
,该反应也能制得氯气,则MnO2、O2、KMnO4三种物质氧化性由强到弱的顺序为_______ 。
①
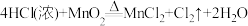
②

③
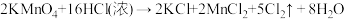
根据以上三个反应,回答下列有关问题:
(1)反应②的离子方程式为
(2)反应②中,氧化产物与还原产物的质量比为
(3)用双线桥法表示①中电子转移情况
(4)若要制得相同质量的氯气,①②③反应中电子转移的数目之比为
(5)已知反应④:
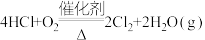 ,该反应也能制得氯气,则MnO2、O2、KMnO4三种物质氧化性由强到弱的顺序为
,该反应也能制得氯气,则MnO2、O2、KMnO4三种物质氧化性由强到弱的顺序为
您最近一年使用:0次



