人们可以利用氧化还原反应研究物质的性质、实现物质的转化。
(1)过氧化钠可用于呼吸面具和潜水艇里的氧气供给_______ (用一个化学方程式表示)。
(2)实验室利用二氧化锰和浓盐酸反应制备Cl2的离子方程式为_______ ,此反应中浓盐酸体现了_______ 性质。
(3)浓硫酸与蔗糖进行“黑面包”实验时产生大量气体的化学方程式_______ 。
(4)将5%H2O2溶液滴入酸性KMnO4溶液中,观察到_______ ,此反应中H2O2做_______ 剂(填“氧化”或“还原)。若将5%H2O2溶液滴入FeCl2溶液中,则观察到_______ ,此反应中H2O2发生_______ 反应(填“氧化”或“还原”)。
(5)工业高炉炼铁时常以赤铁矿(主要成分为Fe2O3)和焦炭(主要成分为碳)为原料,而炼铁过程中实际起作用的是CO,请写出高炉炼铁的化学方程式_______ 。
(1)过氧化钠可用于呼吸面具和潜水艇里的氧气供给
(2)实验室利用二氧化锰和浓盐酸反应制备Cl2的离子方程式为
(3)浓硫酸与蔗糖进行“黑面包”实验时产生大量气体的化学方程式
(4)将5%H2O2溶液滴入酸性KMnO4溶液中,观察到
(5)工业高炉炼铁时常以赤铁矿(主要成分为Fe2O3)和焦炭(主要成分为碳)为原料,而炼铁过程中实际起作用的是CO,请写出高炉炼铁的化学方程式
更新时间:2021-12-30 21:17:56
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】氯在饮用水处理中常用作杀菌剂,且HClO的杀菌能力比ClO-强。
(1)写出实验室制取氯气的离子方程式___________ ,并标出电子转移的数目和方向_______ 。
(2)氯水中Cl2(aq)、HClO和ClO-分别在三者中所占分数(α)随pH变化的关系如图所示。

①用氯处理饮用水,pH=7.5时的杀菌效果比pH=6.5时的杀菌效果_______ (填“好”或“差”)。
②已知:Cl2、HClO和ClO-均可被FeCl2、H2O2等物质还原成Cl-。一种测定氯水中氯元素总量的实验步骤如下,请补充所缺的试剂(写化学式):
步骤1:取一定量的试样,加入足量的___________ 溶液,充分反应。
步骤2:加热。
步骤3:再冷却,加入足量的___________ 溶液。
步骤4:过滤、洗涤、干燥、称量沉淀质量。
步骤5:将实验步骤1~4重复2次。
(3)HClO不稳定,见光遇热均易分解。其分解的化学方程式为___________ 。
(1)写出实验室制取氯气的离子方程式
(2)氯水中Cl2(aq)、HClO和ClO-分别在三者中所占分数(α)随pH变化的关系如图所示。

①用氯处理饮用水,pH=7.5时的杀菌效果比pH=6.5时的杀菌效果
②已知:Cl2、HClO和ClO-均可被FeCl2、H2O2等物质还原成Cl-。一种测定氯水中氯元素总量的实验步骤如下,请补充所缺的试剂(写化学式):
步骤1:取一定量的试样,加入足量的
步骤2:加热。
步骤3:再冷却,加入足量的
步骤4:过滤、洗涤、干燥、称量沉淀质量。
步骤5:将实验步骤1~4重复2次。
(3)HClO不稳定,见光遇热均易分解。其分解的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】含氯物质在日常生活中具有许多重要用途,回答下列问题:
(1)亚氯酸钠(NaClO2)较稳定,但加热或敲击亚氯酸钠固体时立即爆炸,爆炸后的产物可能为___________(填标号)。
(2)我国从2000年起逐步用ClO2替代氯气进行消毒,工业上常利用反应 制备ClO2,
制备ClO2,___________ 是还原剂,___________ 是还原产物,用单线桥法表示反应中电子得失的方向和数目:___________ 。
(3)工业上可利用ClO2制备亚氯酸钠(NaClO2),反应体系中涉及下列物质:NaClO2、ClO2、H2O2、NaOH、H2O、O2写出反应的化学方程式:___________ 。
(4)某温度下将Cl2通入KOH溶液里,反应后得到KCl、KClO、KClO3的混合溶液,其中 与
与 的个数之比为11∶1,则Cl2与KOH反应时,被还原的氯原子和被氧化的氯原子的个数之比为
的个数之比为11∶1,则Cl2与KOH反应时,被还原的氯原子和被氧化的氯原子的个数之比为____ 。
(5)已知氧化性: ,写出少量氯气通入到碘化亚铁溶液中的离子方程式:
,写出少量氯气通入到碘化亚铁溶液中的离子方程式:_____ 。
(6)实验室用下列方法均可制取氯气
①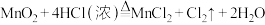
②
③
④
若各反应转移的电子数相同,①②③④生成的氯气质量比为___________ 。
(1)亚氯酸钠(NaClO2)较稳定,但加热或敲击亚氯酸钠固体时立即爆炸,爆炸后的产物可能为___________(填标号)。
| A.NaCl、Cl2 | B.NaCl、NaClO | C.NaClO3、NaClO4 | D.NaCl、NaClO3 |
 制备ClO2,
制备ClO2,(3)工业上可利用ClO2制备亚氯酸钠(NaClO2),反应体系中涉及下列物质:NaClO2、ClO2、H2O2、NaOH、H2O、O2写出反应的化学方程式:
(4)某温度下将Cl2通入KOH溶液里,反应后得到KCl、KClO、KClO3的混合溶液,其中
 与
与 的个数之比为11∶1,则Cl2与KOH反应时,被还原的氯原子和被氧化的氯原子的个数之比为
的个数之比为11∶1,则Cl2与KOH反应时,被还原的氯原子和被氧化的氯原子的个数之比为(5)已知氧化性:
 ,写出少量氯气通入到碘化亚铁溶液中的离子方程式:
,写出少量氯气通入到碘化亚铁溶液中的离子方程式:(6)实验室用下列方法均可制取氯气
①
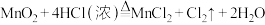
②

③

④

若各反应转移的电子数相同,①②③④生成的氯气质量比为
您最近一年使用:0次
【推荐3】请按要求回答下列问题:
(1)实验室二氧化锰和浓盐酸在加热条件下制取Cl2,其中 MnO2 是__________ 剂;反应中氯化氢体现了_____________ 性和 _______________ 性。
(2)室温下KClO3 与浓盐酸反应制取氯气的化学方程式:KClO3+6HCl(浓)=KCl+3Cl2+3H2O请在上式中用单线桥法表示出得失电子的情况。___
(3)用CuCl2作催化剂,在450℃时用空气中的O2 跟 HCl 反应也能制得氯气,其化学方程式:4HCl+O2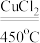 2H2O+2Cl2,从以上3种制备的方法中,可以认为氧化剂的氧化能力从强到弱的顺序为
2H2O+2Cl2,从以上3种制备的方法中,可以认为氧化剂的氧化能力从强到弱的顺序为________ 。
(4)把 Cl2 通入浓氨水中,发生如下反应:3Cl2+8NH3=6NH4Cl+N2请在上式用双线桥表示反应的电子转移方向和数目___ ;反应中氧化剂与还原剂分子数之比为 ___ 。若反应中有 6.8 g NH3 发生氧化反应,则反应中生成的 N2 质量为 __________ g。
(1)实验室二氧化锰和浓盐酸在加热条件下制取Cl2,其中 MnO2 是
(2)室温下KClO3 与浓盐酸反应制取氯气的化学方程式:KClO3+6HCl(浓)=KCl+3Cl2+3H2O请在上式中用单线桥法表示出得失电子的情况。
(3)用CuCl2作催化剂,在450℃时用空气中的O2 跟 HCl 反应也能制得氯气,其化学方程式:4HCl+O2
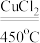 2H2O+2Cl2,从以上3种制备的方法中,可以认为氧化剂的氧化能力从强到弱的顺序为
2H2O+2Cl2,从以上3种制备的方法中,可以认为氧化剂的氧化能力从强到弱的顺序为(4)把 Cl2 通入浓氨水中,发生如下反应:3Cl2+8NH3=6NH4Cl+N2请在上式用双线桥表示反应的电子转移方向和数目
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】I.某同学设计实验探究Cu与98%浓 的反应,装置如图所示,回答下列问题:
的反应,装置如图所示,回答下列问题:___________ 。
(2)试管②用来检验生成的 ,下列试剂中利用
,下列试剂中利用 的还原性进行检验的是___________。
的还原性进行检验的是___________。
(3)试管③中盛放___________ ,用来吸收 ,防止污染空气。
,防止污染空气。
II.如图是硫元素的常见化合价与部分物质类别的对应关系。请回答下列问题:___________ mol。
(5)将Z通入X的水溶液中,发生反应的化学方程式为___________ 。
(6)碳和M的浓溶液的反应中,氧化剂与还原剂物质的量之比为___________ 。
 的反应,装置如图所示,回答下列问题:
的反应,装置如图所示,回答下列问题:
(2)试管②用来检验生成的
 ,下列试剂中利用
,下列试剂中利用 的还原性进行检验的是___________。
的还原性进行检验的是___________。A.酸性 | B.品红溶液 | C.溴水 | D. 溶液 溶液 |
 ,防止污染空气。
,防止污染空气。II.如图是硫元素的常见化合价与部分物质类别的对应关系。请回答下列问题:

(5)将Z通入X的水溶液中,发生反应的化学方程式为
(6)碳和M的浓溶液的反应中,氧化剂与还原剂物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氨基磺酸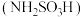 可用于合成除草剂、防火剂、甜味剂、防腐剂、金属清洗剂等,是一种常见的化工原料。
可用于合成除草剂、防火剂、甜味剂、防腐剂、金属清洗剂等,是一种常见的化工原料。
(1)由尿素 与发烟硫酸(用
与发烟硫酸(用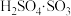 表示,)在40~70℃下进行磺化反应生成氨基磺酸,则该反应的化学方程式为
表示,)在40~70℃下进行磺化反应生成氨基磺酸,则该反应的化学方程式为_______ 。
(2)氨基磺酸在高温时的分解反应为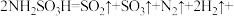
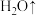 。
。
①检验该混合产物中含有 的试剂是
的试剂是_______ (填序号)。
A.品红溶液 B. 溶液 C.溴水 D.碳酸氢钠溶液
溶液 C.溴水 D.碳酸氢钠溶液
②高温时,该反应中转移2mol电子时,生成气体的总物质的量是_______ mol。
(3)硝酸与氨基磺酸能反应生成硫酸、水和一种氮氧化合物。
①0.5mol该氮氧化合物中氮元素的质量比氧元素的多6g,则该氮氧化合物的化学式为_______ 。
②下列有关浓硫酸和浓硝酸的说法正确的是_______ (填序号)。
A.浓硫酸可用于干燥 、
、 、HI
、HI
B.常温下,浓硫酸和浓硝酸均能将铝“钝化”,均体现其强氧化性
C.浓硫酸和浓硝酸分别长期露置在空气中,两者浓度变小的原理不同
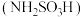 可用于合成除草剂、防火剂、甜味剂、防腐剂、金属清洗剂等,是一种常见的化工原料。
可用于合成除草剂、防火剂、甜味剂、防腐剂、金属清洗剂等,是一种常见的化工原料。(1)由尿素
 与发烟硫酸(用
与发烟硫酸(用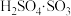 表示,)在40~70℃下进行磺化反应生成氨基磺酸,则该反应的化学方程式为
表示,)在40~70℃下进行磺化反应生成氨基磺酸,则该反应的化学方程式为(2)氨基磺酸在高温时的分解反应为
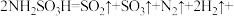
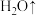 。
。①检验该混合产物中含有
 的试剂是
的试剂是A.品红溶液 B.
 溶液 C.溴水 D.碳酸氢钠溶液
溶液 C.溴水 D.碳酸氢钠溶液②高温时,该反应中转移2mol电子时,生成气体的总物质的量是
(3)硝酸与氨基磺酸能反应生成硫酸、水和一种氮氧化合物。
①0.5mol该氮氧化合物中氮元素的质量比氧元素的多6g,则该氮氧化合物的化学式为
②下列有关浓硫酸和浓硝酸的说法正确的是
A.浓硫酸可用于干燥
 、
、 、HI
、HIB.常温下,浓硫酸和浓硝酸均能将铝“钝化”,均体现其强氧化性
C.浓硫酸和浓硝酸分别长期露置在空气中,两者浓度变小的原理不同
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】盐酸、硫酸和硝酸都是重要的化工原料,也是化学实验室必备的重要试剂
(1)常温下,可用铁、铝制的容器盛放浓硫酸,说明浓硫酸具有___________ 性;硝酸应保存在棕色瓶中,这是因为硝酸具有___________ 性。
(2)如图是硫酸试剂瓶标签上的部分内容,该硫酸的浓度是___________ ;实验人员操作时不必需穿戴的安全用具是___________ 。
A.防护手套 B.实验服 C.防毒面具 D.护目镜
(3)在稀硝酸溶液中加入铜片使之充分反应,写出反应的离子方程式_________________ 。
(4)实验室中向烧杯内加入约20g蔗糖,向其中插入玻璃棒,滴加几滴蒸馏水,再加入适量浓硫酸。白色的蔗糖变为疏松多孔的黑色物质,放出大量的热使烧杯壁发烫。验证产生的气体有SO2的方法是___________________ ,验证该气体中还含有CO2的方法是_______________________ 。
(1)常温下,可用铁、铝制的容器盛放浓硫酸,说明浓硫酸具有
(2)如图是硫酸试剂瓶标签上的部分内容,该硫酸的浓度是
| 化学纯(CP)(500mL) 品名:硫酸 化学式:H2SO4 相对分子质量:98 密度:1.84g/cm3 质量分数: 98.9% |
(3)在稀硝酸溶液中加入铜片使之充分反应,写出反应的离子方程式
(4)实验室中向烧杯内加入约20g蔗糖,向其中插入玻璃棒,滴加几滴蒸馏水,再加入适量浓硫酸。白色的蔗糖变为疏松多孔的黑色物质,放出大量的热使烧杯壁发烫。验证产生的气体有SO2的方法是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】按如图所示装置进行实验,回答下列问题(假设各装置中的反应均为完全反应)。

(1)D中的现象是_______ ;E处集气瓶内收集到气体的检验方法是_______ 。
(2)A中发生反应的化学方程式为_______ 。
(3)C中发生反应的化学方程式为_______ 。
(4)装置A试管内的NaHCO3有8.4克,若反应生成的气体能全部通过后面的装置,则理论上装置C能增重_______ 克。

(1)D中的现象是
(2)A中发生反应的化学方程式为
(3)C中发生反应的化学方程式为
(4)装置A试管内的NaHCO3有8.4克,若反应生成的气体能全部通过后面的装置,则理论上装置C能增重
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】钠元素在自然界都以化合物的形式存在。
(1)过氧化钠中氧元素的化合价为_______ 价,焰色试验为_______ 色。
(2)过氧化钠用于呼吸面具的反应方程式为_______ ,若有2mol的过氧化钠参与反应,转移的电子的物质的量为_______ mol。假设每分钟消耗标准状况下的氧气1.12L,若佩戴呼吸面具1小时,需要消耗过氧化钠的质量_______ g。
(3)利用下图比较碳酸钠和碳酸氢钠的热稳定性,则物质甲的化学式为_______ 。

(4)若要除去碳酸氢钠溶液中的碳酸钠,发生反应的化学方程式为_______ 。
(1)过氧化钠中氧元素的化合价为
(2)过氧化钠用于呼吸面具的反应方程式为
(3)利用下图比较碳酸钠和碳酸氢钠的热稳定性,则物质甲的化学式为

(4)若要除去碳酸氢钠溶液中的碳酸钠,发生反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】钢铁是应用广泛的金属材料。
(1)英国学者R•坦普尔论证了我国古代冶铁技术世界第一。早在公元前4世纪,中国已广泛利用铁矿石与木炭生产生铁,并加入“黑土”以降低生铁的熔化温度。
①“黑土”含有磷酸铁(FePO4),其中磷元素的化合价为____ 。
②古法炼铁的原理包含一氧化碳与氧化铁在高温下反应,反应的化学方程式是____ 。
③生铁和钢是两种含碳量____ 的铁合金(填“相同”或“不同”)。
(2)铁锈成分中含有氧化铁(Fe2O3),写出氧化铁与稀硫酸反应的化学方程式____ 。
(1)英国学者R•坦普尔论证了我国古代冶铁技术世界第一。早在公元前4世纪,中国已广泛利用铁矿石与木炭生产生铁,并加入“黑土”以降低生铁的熔化温度。
①“黑土”含有磷酸铁(FePO4),其中磷元素的化合价为
②古法炼铁的原理包含一氧化碳与氧化铁在高温下反应,反应的化学方程式是
③生铁和钢是两种含碳量
(2)铁锈成分中含有氧化铁(Fe2O3),写出氧化铁与稀硫酸反应的化学方程式
您最近一年使用:0次
【推荐2】化学研究源于实验与理论的结合,得益于科学的推断与探究。
(1)一个体重 的健康人含铁
的健康人含铁 ,这
,这 铁在人体中以
铁在人体中以 和
和 的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。
的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。
①服用维生素C,可使食物中的铁离子还原成亚铁离子,有利于铁的吸收,以下为常见铁元素的几种微粒,其中既有氧化性又有还原性的是___________ 。
A. B.
B. C.
C.
②工业盐的主要成分是 ,曾多次发生过因误食
,曾多次发生过因误食 而中毒的事件,其原因是将人体内的
而中毒的事件,其原因是将人体内的 转化为
转化为 而失去了与
而失去了与 结合的能力,这说明
结合的能力,这说明 具有
具有___________ 性。
③工业盐中毒后,可服用维生素C来缓解中毒症状,这说明维生素C具有___________ 性。
(2)常见的食品脱氧剂多为无机铁系脱氧剂,其主要成分为活性铁粉。脱氧中的一步主要反应为: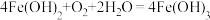 ,该脱氧反应中还原剂是
,该脱氧反应中还原剂是___________ 。
(3)某化学兴趣小组用食品脱氧剂( 铁粉、
铁粉、 活性炭、
活性炭、 氯化钠)进行如图两个实验。
氯化钠)进行如图两个实验。
实验Ⅰ:

请回答:
①溶液丙中一定含有的金属阳离子是___________ (写离子符号)。
②检验溶液丙中 的方案是
的方案是___________ 。
③实验Ⅱ:将乙烘干后进行如图实验,物质之间的转化关系如图(部分产物路法)
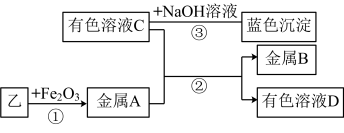
写出反应②的离子方程式___________ ,若反应消耗 金属A,转移电子的数目为
金属A,转移电子的数目为___________ 。
(1)一个体重
 的健康人含铁
的健康人含铁 ,这
,这 铁在人体中以
铁在人体中以 和
和 的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。
的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。①服用维生素C,可使食物中的铁离子还原成亚铁离子,有利于铁的吸收,以下为常见铁元素的几种微粒,其中既有氧化性又有还原性的是
A.
 B.
B. C.
C.
②工业盐的主要成分是
 ,曾多次发生过因误食
,曾多次发生过因误食 而中毒的事件,其原因是将人体内的
而中毒的事件,其原因是将人体内的 转化为
转化为 而失去了与
而失去了与 结合的能力,这说明
结合的能力,这说明 具有
具有③工业盐中毒后,可服用维生素C来缓解中毒症状,这说明维生素C具有
(2)常见的食品脱氧剂多为无机铁系脱氧剂,其主要成分为活性铁粉。脱氧中的一步主要反应为:
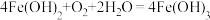 ,该脱氧反应中还原剂是
,该脱氧反应中还原剂是(3)某化学兴趣小组用食品脱氧剂(
 铁粉、
铁粉、 活性炭、
活性炭、 氯化钠)进行如图两个实验。
氯化钠)进行如图两个实验。实验Ⅰ:

请回答:
①溶液丙中一定含有的金属阳离子是
②检验溶液丙中
 的方案是
的方案是③实验Ⅱ:将乙烘干后进行如图实验,物质之间的转化关系如图(部分产物路法)

写出反应②的离子方程式
 金属A,转移电子的数目为
金属A,转移电子的数目为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】填写下列空白:
(1)FeCl3溶液中加入铁粉,溶液由___ 色变为___ 色,该反应的离子方程式为______ ;
(2)除去FeCl3溶液中混有的FeCl2需向溶液中通入______ (填物质名称),该反应的离子方程式为______ ;
(3)在Fe3O4 +4CO 3Fe+4CO 2的反应中,
3Fe+4CO 2的反应中,_____ 是氧化剂,被氧化的元素为____ ,氧化产物是________ ,若有11.6g Fe3O4参加反应则转移电子的物质的量为__________ 。
(1)FeCl3溶液中加入铁粉,溶液由
(2)除去FeCl3溶液中混有的FeCl2需向溶液中通入
(3)在Fe3O4 +4CO
 3Fe+4CO 2的反应中,
3Fe+4CO 2的反应中,
您最近一年使用:0次



