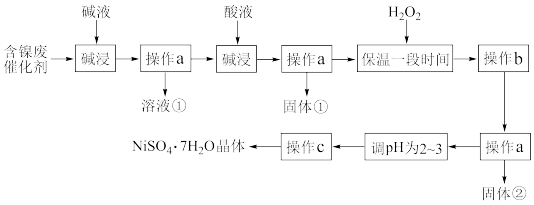
某化工厂的含镍催化剂中主要含有Ni,还含有Al(31%)、Fe(1.3%)的单质及氧化物、及其他不溶性杂质(3.3%)。某化学研究性学习小组通过查阅资料,设计如图所示方法以含镍废催化剂为原料制备NiSO4·7H2O。
【查阅资料】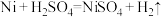 ;部分阳离子以氢氧化物形式沉淀时的
;部分阳离子以氢氧化物形式沉淀时的 如下:
如下:
回答下列问题:
(1)操作a、c应分别选用下列装置中的______________(填字母)。
(2)“碱浸”过程中发生反应的离子方程式为_______________ 、______________ 。
(3)“酸浸”时加入的酸是_____________ (填化学式),酸浸后,经操作a分离出固体①后,溶液中一定含有的金属离子是______________________ .
(4)操作b为调节溶液的pH,pH的最佳调控范围是___________________ .
(5)产品晶体中有时会混有少量绿矾 ,其原因可能是
,其原因可能是___________________ .
(6)现有100 kg含镍催化剂,若酸浸步骤镍浸出率为a%,其它物质全部参与反应,且假定镍在酸浸后续步骤无损失,操作c后粗晶体中含绿矾b%,则最终能得到粗晶体的质量为___________ kg。(只写出计算表达式)

【查阅资料】
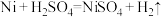 ;部分阳离子以氢氧化物形式沉淀时的
;部分阳离子以氢氧化物形式沉淀时的 如下:
如下:| 沉淀物 |  |  |  |  |
| 开始沉淀 | 3.8 | 2.7 | 7.6 | 7.1 |
| 完全沉淀 | 5.2 | 3.2 | 9.7 | 9.2 |
回答下列问题:
(1)操作a、c应分别选用下列装置中的______________(填字母)。
A. | B. | C.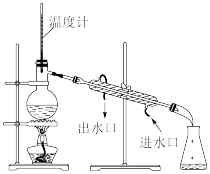 | D.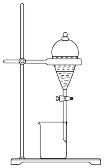 |
(3)“酸浸”时加入的酸是
(4)操作b为调节溶液的pH,pH的最佳调控范围是
(5)产品晶体中有时会混有少量绿矾
 ,其原因可能是
,其原因可能是(6)现有100 kg含镍催化剂,若酸浸步骤镍浸出率为a%,其它物质全部参与反应,且假定镍在酸浸后续步骤无损失,操作c后粗晶体中含绿矾b%,则最终能得到粗晶体的质量为
更新时间:2022-02-16 17:48:25
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】工业上利用硫铁矿烧渣(主要成分为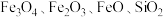 )为原料制备高档颜料——铁红
)为原料制备高档颜料——铁红 ,具体生产流程如下:
,具体生产流程如下:
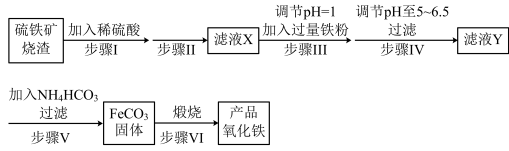
回答下列问题:
(1)为提高酸浸的效率,可采取的措施有___________ (任写一种)。
(2)实验室实现“步骤Ⅱ”中分离操作所用的玻璃仪器有___________ 、玻璃棒和烧杯等,该步骤是为了除去___________ (填相关物质的化学式)。
(3)检验步骤Ⅲ已经进行完全,可用的试剂是___________ 。
(4)步骤V的反应温度一般需控制在 以下,其目的是
以下,其目的是___________ ;该步骤中反应生成 的同时有气泡产生,该反应的离子方程式为
的同时有气泡产生,该反应的离子方程式为___________ 。
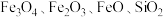 )为原料制备高档颜料——铁红
)为原料制备高档颜料——铁红 ,具体生产流程如下:
,具体生产流程如下:
回答下列问题:
(1)为提高酸浸的效率,可采取的措施有
(2)实验室实现“步骤Ⅱ”中分离操作所用的玻璃仪器有
(3)检验步骤Ⅲ已经进行完全,可用的试剂是
(4)步骤V的反应温度一般需控制在
 以下,其目的是
以下,其目的是 的同时有气泡产生,该反应的离子方程式为
的同时有气泡产生,该反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】铁及其化合物在生产和生活中有着广泛的应用。制备纳米铁粉,其流程如下:
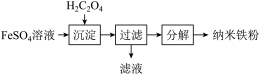
(1)沉淀时通常滴加稍过量的 ,过滤得
,过滤得 。写出沉淀反应的离子方程式为
。写出沉淀反应的离子方程式为___________ 。
(2)过滤所得到的晶体 在
在 时分解:
时分解: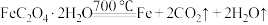 。由于生成
。由于生成 ,该反应成为制备纳米铁粉的重要方法。
,该反应成为制备纳米铁粉的重要方法。 的作用是
的作用是___________ 。
(3)用纳米铁粉处理废水中的 :酸性条件下,纳米铁粉与废水中
:酸性条件下,纳米铁粉与废水中 反应生成
反应生成 与
与 ,其反应的离子方程式是
,其反应的离子方程式是___________ 。

(1)沉淀时通常滴加稍过量的
 ,过滤得
,过滤得 。写出沉淀反应的离子方程式为
。写出沉淀反应的离子方程式为(2)过滤所得到的晶体
 在
在 时分解:
时分解: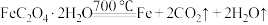 。由于生成
。由于生成 ,该反应成为制备纳米铁粉的重要方法。
,该反应成为制备纳米铁粉的重要方法。 的作用是
的作用是(3)用纳米铁粉处理废水中的
 :酸性条件下,纳米铁粉与废水中
:酸性条件下,纳米铁粉与废水中 反应生成
反应生成 与
与 ,其反应的离子方程式是
,其反应的离子方程式是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】为探索工业废料的再利用,某化学兴趣小组设计了如下实验流程,用含有铝、铁和铜的合金废料制取氯化铝、绿矾晶体(FeSO4·7H2O)和胆矾晶体。

请回答:
(1)写出步骤Ⅰ反应的离子方程式:_________________________ 。
(2)试剂X是______ 。步骤Ⅰ、Ⅱ、Ⅲ中均需进行的实验操作是________ 。
(3)用固体F制备CuSO4溶液,可设计以下三种途径:

写出途径①中反应的离子方程式_______________________________ ,请选出你认为的最佳途径并说明选择的理由______________________________ 。

请回答:
(1)写出步骤Ⅰ反应的离子方程式:
(2)试剂X是
(3)用固体F制备CuSO4溶液,可设计以下三种途径:

写出途径①中反应的离子方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】十九大报告中提到"必须树立和践行绿水青山就是金山银山的理念,坚持节约资源和保护环境是我国的基本国策。"
Ⅰ.某工厂为从镀银废玻璃表面回收金属银,并重新获得洗银试剂Fe(NO3)3溶液,设计如下路线∶

(1)过程①中反应的离子方程式为___________ 。
(2)过程②中所用试剂A为___________ (填化学式),过程③的操作名称为___________ 。
(3)过程④中试剂 C最佳选择___________ (填序号)。
a.氯气 b.H2O2 c. SO2 d. KMnO4
(4)检验溶液1中金属阳离子的实验方法为∶取少量溶液 1于洁净的试管中,___________ ,溶液迅速变为红色,即可验证。
Ⅱ.目前氨氮废水处理方法主要有吹脱法、化学沉淀法、生物硝化反硝化法等。某氮肥厂的氨氮废水中氮元素多以 和NH3·H2O的形式存在。该厂技术团队设计该废水处理方案流程如下∶
和NH3·H2O的形式存在。该厂技术团队设计该废水处理方案流程如下∶

(1)过程①∶加入NaOH溶液,调节PH至9后,升温至30℃,通入空气将氨赶出并回收。请用离子方程式表示加 NaOH 溶液时所发生的反应___________ 。
(2)过程②、③∶在微生物亚硝酸菌和硝酸菌作用下实现 →
→ →
→ 的转化,称为硝化反应。1 mol
的转化,称为硝化反应。1 mol  可被
可被___________ L(标准状况)O2 最终氧化成 。
。
(3)过程④∶在一定条件下向废水中加入甲醇(CH3OH)实现 HNO3→N2转化,称为反硝化反应。此过程中甲醇(C元素-2 价)转化为CO2,写出此过程的化学方程式___________ 。
Ⅰ.某工厂为从镀银废玻璃表面回收金属银,并重新获得洗银试剂Fe(NO3)3溶液,设计如下路线∶

(1)过程①中反应的离子方程式为
(2)过程②中所用试剂A为
(3)过程④中试剂 C最佳选择
a.氯气 b.H2O2 c. SO2 d. KMnO4
(4)检验溶液1中金属阳离子的实验方法为∶取少量溶液 1于洁净的试管中,
Ⅱ.目前氨氮废水处理方法主要有吹脱法、化学沉淀法、生物硝化反硝化法等。某氮肥厂的氨氮废水中氮元素多以
 和NH3·H2O的形式存在。该厂技术团队设计该废水处理方案流程如下∶
和NH3·H2O的形式存在。该厂技术团队设计该废水处理方案流程如下∶
(1)过程①∶加入NaOH溶液,调节PH至9后,升温至30℃,通入空气将氨赶出并回收。请用离子方程式表示加 NaOH 溶液时所发生的反应
(2)过程②、③∶在微生物亚硝酸菌和硝酸菌作用下实现
 →
→ →
→ 的转化,称为硝化反应。1 mol
的转化,称为硝化反应。1 mol  可被
可被 。
。(3)过程④∶在一定条件下向废水中加入甲醇(CH3OH)实现 HNO3→N2转化,称为反硝化反应。此过程中甲醇(C元素-2 价)转化为CO2,写出此过程的化学方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】青花瓷胎体的原料——高岭土[Al2Si2O5(OH)x],可掺进瓷石制胎,青花瓷釉料的成分主要是钾长石(KAlSi3O8),在1300℃左右一次烧成的釉可形成精美的青花瓷。
(1)下列说法正确的是___ (填选项字母)。
(2)在“南澳一号”考古直播过程中,需用高纯度SiO2制造的光纤。如图是用海边的石英砂(含氯化钠、氧化铝等杂质)制备二氧化硅粗产品的工艺流程。

①洗涤石英砂的目的是___ 。
②在以上流程中,要将洗净的石英砂研磨成粉末,目的是___ 。
③工业上常用纯净石英砂与C在高温下发生反应制造粗硅,粗硅中含有SiC,其中Si和SiC的物质的量之比为1∶1。下列说法正确的是___ (填选项字母)。
A.SiC性质稳定,能用于制造抗高温水泥
B.制造粗硅时的反应为2SiO2+5C Si+SiC+4CO↑
Si+SiC+4CO↑
C.在以上流程中,将盐酸改为NaOH溶液,也可达到目的
D.纯净的SiO2只能用于制造光导纤维
(1)下列说法正确的是
| A.高岭土分子中x=2 |
| B.钾长石能完全溶解在盐酸中形成澄清的溶液 |
| C.烧制青花瓷过程中发生了复杂的物理变化和化学变化 |
| D.青花瓷、玻璃、水泥都属于硅酸盐产品 |

①洗涤石英砂的目的是
②在以上流程中,要将洗净的石英砂研磨成粉末,目的是
③工业上常用纯净石英砂与C在高温下发生反应制造粗硅,粗硅中含有SiC,其中Si和SiC的物质的量之比为1∶1。下列说法正确的是
A.SiC性质稳定,能用于制造抗高温水泥
B.制造粗硅时的反应为2SiO2+5C
 Si+SiC+4CO↑
Si+SiC+4CO↑C.在以上流程中,将盐酸改为NaOH溶液,也可达到目的
D.纯净的SiO2只能用于制造光导纤维
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】HDS催化剂广泛用于石油炼制和化学工业生产中,通常利用加碱焙烧——水浸取法从HDS废催化剂(主要成分为MoS、NiS、V2O5、Al2O3)中提取贵重金属钒和钼,其工艺流程如图所示。
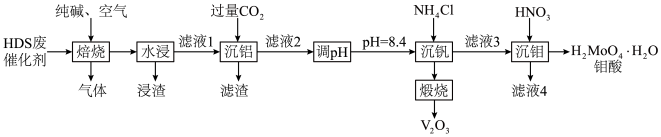
已知:I.MoO3、V2O5、Al2O3均可与纯碱反应生成对应的钠盐,而NiO不行。
II.高温下,NH4VO3易分解产生N2和一种含氮元素的气体。
III.Ksp(CuS)=6×10-36;K1(H2S)=1×10-7、K2(H2S)=6×10-15。
回答下列问题:
(1)“浸渣”的成分为_______ (填化学式);“滤液2”中的成分除了Na2MoO4外,还含有_______ (填化学式)。
(2)请写出“焙烧”过程中MoS及Al2O3分别与纯碱反应的化学方程式:_______ ,_______ 。
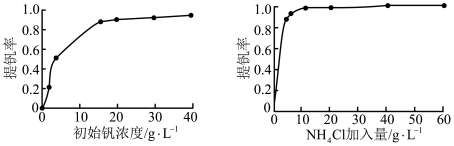
(3)“沉钒”时提钒率随初始钒的浓度及氯化铵的加入量的关系如图所示,则选择的初始钒的浓度和NH4Cl的加入量分别为_______ 、_______ 。
(4)“沉钒”时生成NH4VO3沉淀,请写出“煅烧”后生成氧化产物和还原产物的物质的量之比_______ 。
(5)在实际的工业生产中,“沉钼”前要加入NH4HS进行“除杂”,除掉溶液中微量的Cu2+,则反应Cu2++HS-=CuS↓+H+的K=_______ 。

已知:I.MoO3、V2O5、Al2O3均可与纯碱反应生成对应的钠盐,而NiO不行。
II.高温下,NH4VO3易分解产生N2和一种含氮元素的气体。
III.Ksp(CuS)=6×10-36;K1(H2S)=1×10-7、K2(H2S)=6×10-15。
回答下列问题:
(1)“浸渣”的成分为
(2)请写出“焙烧”过程中MoS及Al2O3分别与纯碱反应的化学方程式:
(3)“沉钒”时提钒率随初始钒的浓度及氯化铵的加入量的关系如图所示,则选择的初始钒的浓度和NH4Cl的加入量分别为

(4)“沉钒”时生成NH4VO3沉淀,请写出“煅烧”后生成氧化产物和还原产物的物质的量之比
(5)在实际的工业生产中,“沉钼”前要加入NH4HS进行“除杂”,除掉溶液中微量的Cu2+,则反应Cu2++HS-=CuS↓+H+的K=
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某化学兴趣小组拟探究锡及锡的化合物的部分性质。经查阅资料知:Sn的熔点231℃;SnCl2易被氧化,且易水解;Sn(OH)2常温下易分解,SnCl4常温下为无色液体,熔点-33℃,沸点114.1℃,请回答下列问题:
(1)该小组用以下流程制备SnSO4晶体:

①操作Ⅱ所需的实验仪器为______________________________________________ 。
②过滤操作中玻璃棒使用的注意事项为____________________________ 。
③操作Ⅰ为沉淀的洗涤。请简述如何判断沉淀是否洗涤干净:____________________ 。
(2)用熔融的锡与干燥的氯气制备SnCl4,提供的装置如下:
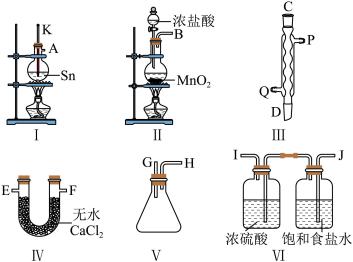
①装置Ⅲ为冷凝管,则水流从________ 进入。
②请用大写英文字母按从左到右顺序连接组装仪器_________________________________________ 。
③有同学指出②中连接的实验装置存在不足,不足之处为______________________ 。
(3)测定锡粉质量分数的步骤:取锡粉1.226g溶于盐酸中,加入过量的FeCl3溶液,再用0.1000mol·L−1 K2Cr2O7溶液滴定Fe2+,消耗K2Cr2O7溶液32.00mL,发生的反应:6FeCl2+K2Cr2O7+14HCl===6FeCl3+2KCl+2CrCl3+7H2O。则锡粉的质量分数为(杂质不参与反应)____________ 。
(1)该小组用以下流程制备SnSO4晶体:

①操作Ⅱ所需的实验仪器为
②过滤操作中玻璃棒使用的注意事项为
③操作Ⅰ为沉淀的洗涤。请简述如何判断沉淀是否洗涤干净:
(2)用熔融的锡与干燥的氯气制备SnCl4,提供的装置如下:

①装置Ⅲ为冷凝管,则水流从
②请用大写英文字母按从左到右顺序连接组装仪器
③有同学指出②中连接的实验装置存在不足,不足之处为
(3)测定锡粉质量分数的步骤:取锡粉1.226g溶于盐酸中,加入过量的FeCl3溶液,再用0.1000mol·L−1 K2Cr2O7溶液滴定Fe2+,消耗K2Cr2O7溶液32.00mL,发生的反应:6FeCl2+K2Cr2O7+14HCl===6FeCl3+2KCl+2CrCl3+7H2O。则锡粉的质量分数为(杂质不参与反应)
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】石河子一中强基计划化学学科实验小组同学查阅资料,发现硫脲[CS(NH2)2]是用于制造药物、染料、金属矿物的浮选剂等的原料,同学们用Ca(HS)2与CaCN2(石灰氮)合成硫脲并测定产品纯度。
已知:①硫脲是白色、有光泽的晶体,相对分子质量76,溶于水,20℃时溶解度为13.6g;在150℃时转变成NH4SCN。②酸性:H2CO3>H2S。
(1)制备Ca(HS)2溶液:所用装置如图所示。

①装置a的名称为____ 。
②装置b中盛放的试剂____ 。
③装置c中的长直导管的作用是____ ,三颈烧瓶中通入CO2不能过量,原因是____ 。
(2)制备硫脲:将CaCN2与Ca(HS)2溶液混合,加热至80℃时,可合成硫脲,同时生成一种常见强碱,该反应的化学方程式为____ 。
(3)产品纯度的测定。
称取ag粗产品,配制成100mL溶液,量取20.00mL该溶液,用bmol/L的酸性KMnO4溶液滴定,滴至终点时平均消耗酸性KMnO4溶液的体积为VmL。
已知:5CS(NH2)2+14MnO +32H+=14Mn2++5CO2↑+5N2↑+5SO
+32H+=14Mn2++5CO2↑+5N2↑+5SO +26H2O。
+26H2O。
①滴定至终点时的现象是____ 。
②该产品的纯度为____ (写出表达式即可)。
已知:①硫脲是白色、有光泽的晶体,相对分子质量76,溶于水,20℃时溶解度为13.6g;在150℃时转变成NH4SCN。②酸性:H2CO3>H2S。
(1)制备Ca(HS)2溶液:所用装置如图所示。

①装置a的名称为
②装置b中盛放的试剂
③装置c中的长直导管的作用是
(2)制备硫脲:将CaCN2与Ca(HS)2溶液混合,加热至80℃时,可合成硫脲,同时生成一种常见强碱,该反应的化学方程式为
(3)产品纯度的测定。
称取ag粗产品,配制成100mL溶液,量取20.00mL该溶液,用bmol/L的酸性KMnO4溶液滴定,滴至终点时平均消耗酸性KMnO4溶液的体积为VmL。
已知:5CS(NH2)2+14MnO
 +32H+=14Mn2++5CO2↑+5N2↑+5SO
+32H+=14Mn2++5CO2↑+5N2↑+5SO +26H2O。
+26H2O。①滴定至终点时的现象是
②该产品的纯度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】冰晶石又名六氟铝酸钠(Na3AlF6),白色固体,微溶于水,常用作电解铝工业的助熔剂。工业上用萤石(主要成分是CaF2)、浓硫酸、氢氧化铝和碳酸钠溶液通过湿法制备冰晶石,某化学实验小组模拟工业上制取Na3AlF6的装置图如图(该装置均由聚四氟乙烯仪器组装而成)。
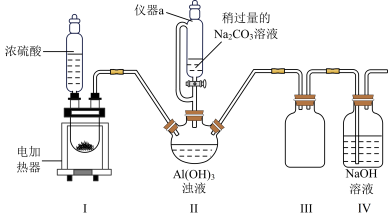
已知:CaF2+H2SO4 CaSO4+2HF↑
CaSO4+2HF↑
(1)装置Ⅲ的作用为__ 。
(2)在实验过程中,装置Ⅱ中有CO2气体逸出,同时观察到有白色固体析出,请写出该反应的离子方程式:__ 。
(3)在实验过程中,先向装置Ⅱ中通入HF气体,然后再滴加Na2CO3溶液,而不是先将Na2CO3和Al(OH)3混合后再通入HF气体,其原因是__ 。
(4)装置Ⅱ反应后的混合液经过过滤可得到Na3AlF6晶体,在过滤操作中确定沉淀已经洗涤干净的方法是__ 。
(5)萤石中含有少量的Fe2O3杂质,可用装置Ⅰ反应后的溶液来测定氟化钙的含量。具体操作如下:取8.0g萤石加入装置Ⅰ中,完全反应后,将混合液加水稀释,然后加入足量的KI固体,再以淀粉为指示剂,用0.1000mol·L-1 Na2S2O3标准溶液滴定,当出现__ 现象时,到达滴定终点,消耗Na2S2O3标准溶液40.00mL,则萤石中氟化钙的百分含量为__ 。(已知:I2+2 =
= +2I-)
+2I-)

已知:CaF2+H2SO4
 CaSO4+2HF↑
CaSO4+2HF↑(1)装置Ⅲ的作用为
(2)在实验过程中,装置Ⅱ中有CO2气体逸出,同时观察到有白色固体析出,请写出该反应的离子方程式:
(3)在实验过程中,先向装置Ⅱ中通入HF气体,然后再滴加Na2CO3溶液,而不是先将Na2CO3和Al(OH)3混合后再通入HF气体,其原因是
(4)装置Ⅱ反应后的混合液经过过滤可得到Na3AlF6晶体,在过滤操作中确定沉淀已经洗涤干净的方法是
(5)萤石中含有少量的Fe2O3杂质,可用装置Ⅰ反应后的溶液来测定氟化钙的含量。具体操作如下:取8.0g萤石加入装置Ⅰ中,完全反应后,将混合液加水稀释,然后加入足量的KI固体,再以淀粉为指示剂,用0.1000mol·L-1 Na2S2O3标准溶液滴定,当出现
 =
= +2I-)
+2I-)
您最近一年使用:0次



